Clear Sky Science · nl
Oorzaken en gevolgen van experimentele variatie in tijdelijke expressie in Nicotiana benthamiana
Waarom kleine plantexperimenten ertoe doen
Veel doorbraken in plantkunde en bio-gebaseerde productie beginnen met een eenvoudige truc: bladweefsel kort veranderen in miniatuurtestfabriekjes. Bij de soort Nicotiana benthamiana kunnen wetenschappers snel nieuw DNA inbrengen en binnen enkele dagen zien wat er gebeurt. Die snelheid maakte de plant tot een werkpaard voor het testen van genen, het bouwen van metabole paden en het prototypen van nieuwe biologische ontwerpen. Maar net als bij hetzelfde recept in verschillende ovens kunnen de resultaten van run tot run variëren. Deze studie stelt een bedrieglijk eenvoudige vraag met grote gevolgen: hoe consistent zijn deze snelle planttesten, en wat kunnen onderzoekers doen om de ruis te temmen zodat ze subtiele verschillen in hun gegevens kunnen vertrouwen?
Hoe een favoriete testplant verschillende antwoorden kan geven
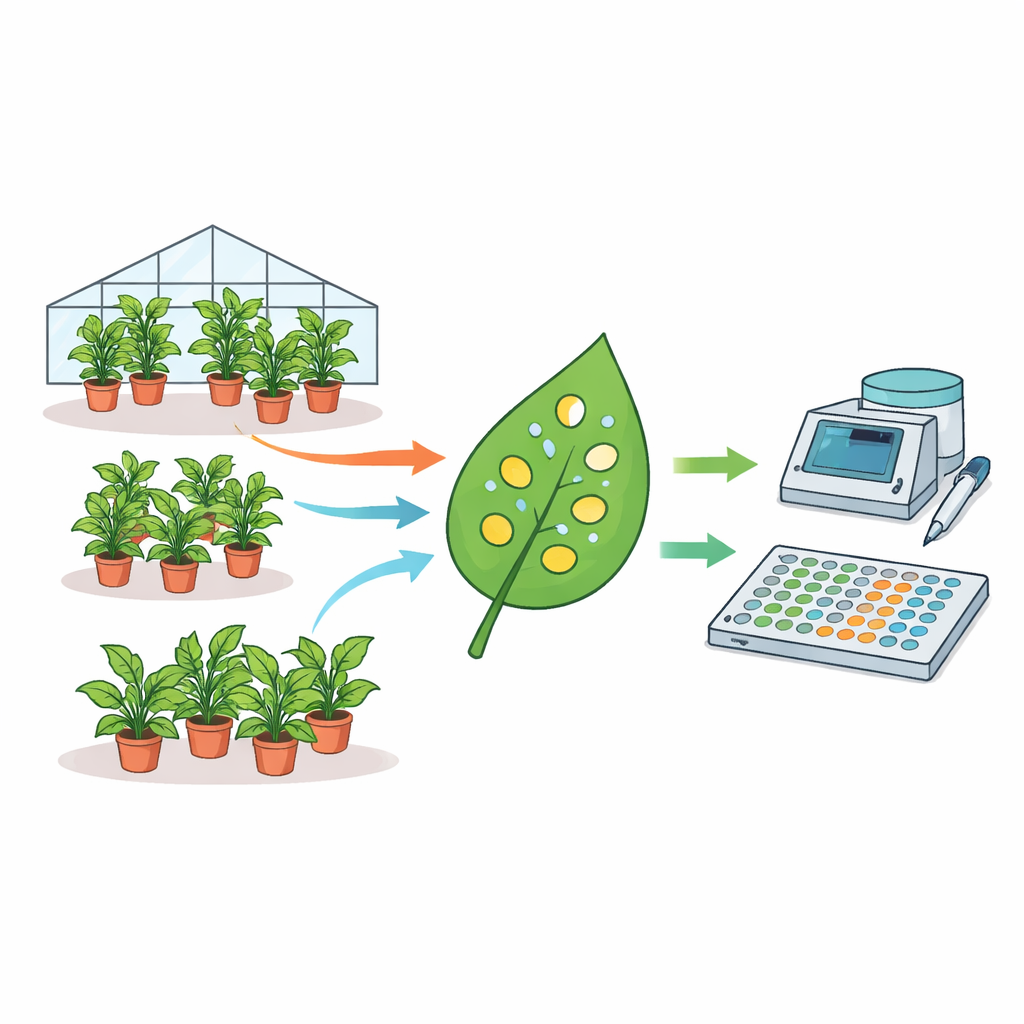
De auteurs stelden een ongebruikelijk grote dataset samen: metingen van 1915 individuele N. benthamiana-planten verzameld over bijna drie jaar. Elke plant werd geïnfiltreerd met Agrobacterium-bacteriën die een fluorescerend reporter-gen droegen, en er werden kleine schijfjes uit bladeren geponst die op een plaatlezer werden uitgelezen. Met statistische modellen splitsten ze op waar variabiliteit vandaan komt. Ze vonden dat verschillen tussen plant-batches, tussen planten binnen een batch en zelfs tussen schijfjes van hetzelfde blad substantieel bijdroegen aan de totale spreiding in fluorescentie. Gemiddelde expressieniveaus konden zelfs tot vier keer verschillen tussen ogenschijnlijk identieke experimenten die op verschillende dagen werden uitgevoerd. Factoren zoals plantleeftijd en hoeveelheid water beïnvloeden ook de signaalsterkte, terwijl het tijdstip van monstername dat niet deed.
Trucs testen om de ruis gelijk te trekken
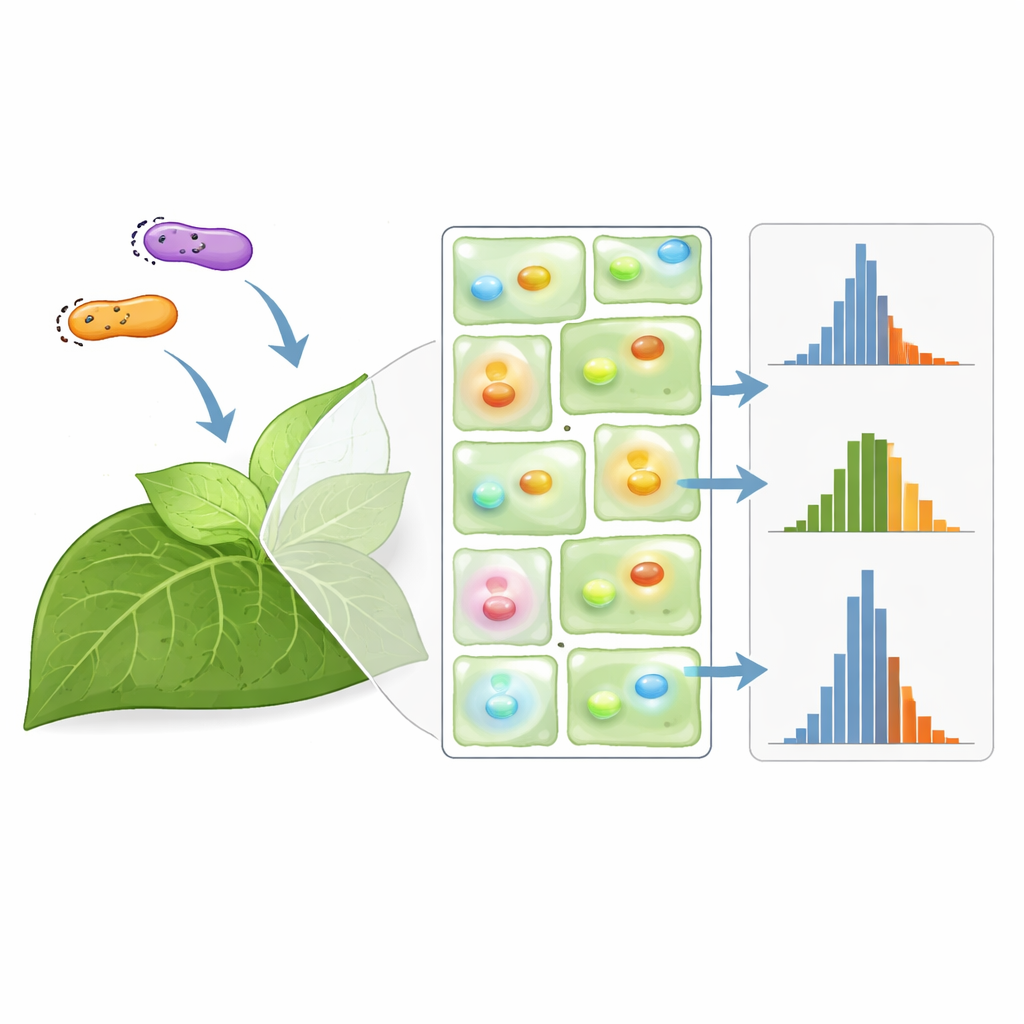
Om deze spreiding te verkleinen gebruiken veel labs een “normaliseergen”: ze leveren twee fluorescerende reporters tegelijk en analyseren de verhouding van hun signalen in de hoop dat gedeelde bronnen van ruis elkaar opheffen. Het team vergeleek systematisch 17 manieren om deze dubbele reporters mee te leveren, inclusief het mengen van aparte bacteriestammen, het stapelen van beide genen op hetzelfde DNA-fragment en het gebruik van enkele stammen die twee plasmiden dragen. Ze lieten zien dat al deze strategieën basale expressieniveaus kunnen veranderen, soms drastisch, afhankelijk van genoriëntatie en plasmide-kopieaantal. Belangrijk is dat de meeste—maar niet alle—normalisatieschema’s de variatie verminderden vergeleken met het meten van één reporter alleen, waarbij een eenvoudige co-infiltratie van twee vergelijkbare plasmiden naar voren kwam als een van de meest effectieve opties.
Wanneer behulpzame correcties tegenwerken
Het verhaal bleek genuanceerder toen het team naar promotoren keek—de DNA-schakelaars die bepalen hoe sterk elk gen wordt aangezet. Ze probeerden combinaties van zwakke, middelmatige en sterke promotoren die de twee fluorescerende eiwitten aanstuurden. Normalisatie werkte het beste wanneer beide reporters precies dezelfde promotor gebruikten; onder die voorwaarden toonde de verhouding veel minder spreiding. Maar wanneer promotoren verschilden, werd de verhouding soms onregelmatiger dan het ruwe signaal van één gen, waardoor de statistische kracht juist verslechterde. De auteurs vonden ook dat het aanpassen van de dichtheid van de bacteriestammen voornamelijk veranderde hoe fel de signalen waren, niet hoe variabel ze waren. Over het geheel genomen toont het werk aan dat normalisatie geen universele oplossing is: het succes hangt sterk af van de details van het constructontwerp.
Hoeveel planten zijn genoeg?
Gewapend met hun grote dataset bouwden de onderzoekers een Monte Carlo-simulatie om te modelleren hoe variabiliteit zich door typische experimenten heen voortplant. Ze gebruikten die om een vraag te beantwoorden waar elke experimentalist mee te maken heeft: gegeven een bepaald ruisniveau, hoeveel planten heb je nodig om betrouwbaar een echt verschil tussen twee constructen te detecteren? Voor gangbare Agrobacterium-stammen vonden ze dat effecten groter dan ongeveer 50 procent met slechts een paar planten gedetecteerd kunnen worden, terwijl het uit elkaar halen van verschillen kleiner dan 20 procent tientallen planten kan vereisen, soms meer dan praktisch haalbaar is. Zorgvuldig gekozen normalisatie kan deze aantallen enigszins verkleinen, vooral wanneer identieke promotoren worden gebruikt en maar een paar planten beschikbaar zijn, maar in sommige ontwerpen biedt het weinig voordeel.
Wat dit betekent voor toekomstige plantenengineering
Voor niet-specialisten is de kernboodschap dat zelfs in een geliefd, zeer handig plantsysteem experimentele ruis zowel substantieel als beheersbaar is. De studie brengt in kaart waar variatie vandaan komt, toont dat populaire correctiemethoden kunnen helpen of schaden afhankelijk van hoe ze zijn opgebouwd, en biedt eenvoudige richtlijnen voor power-analyse bij het plannen van experimenten. In gewone bewoordingen vertelt het plantenbiologen hoe ze hun studies moeten dimensioneren zodat ze toevallige fluctuaties niet verwarren met echte biologische effecten, en hoe ze reporter-constructen ontwerpen die betrouwbaardere vergelijkingen opleveren. Deze inzichten zouden N. benthamiana tot een nog betrouwbaarder platform moeten maken voor het snel testen van genen, het samenstellen van nieuwe metabole paden en het verder brengen van synthetische biologie naar meer voorspelbare engineering van levende systemen.
Bronvermelding: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Trefwoorden: Nicotiana benthamiana, tijdelijke expressie, synthetische biologie, experimentele variabiliteit, Agrobacterium