Clear Sky Science · fr
Causes et conséquences de la variation expérimentale dans l’expression transitoire de Nicotiana benthamiana
Pourquoi de petites expériences sur les plantes comptent
Beauxoup de percées en science végétale et en production bio‑basée commencent par une astuce simple : transformer brièvement des feuilles en mini‑usines d’essai. Chez l’espèce Nicotiana benthamiana, les chercheurs peuvent introduire rapidement un ADN nouveau et observer les effets en quelques jours. Cette rapidité a fait de la plante un outil de travail pour tester des gènes, construire des voies métaboliques et prototyper de nouveaux dispositifs biologiques. Mais, comme lorsqu’on cuit la même recette dans des fours différents, les résultats peuvent varier d’une expérience à l’autre. Cette étude pose une question apparemment simple mais aux grandes conséquences : dans quelle mesure ces tests rapides sur plantes sont‑ils reproductibles, et que peuvent faire les chercheurs pour maîtriser le bruit afin de pouvoir faire confiance à des différences subtiles dans leurs données ?
Comment une plante favorite peut donner des réponses différentes
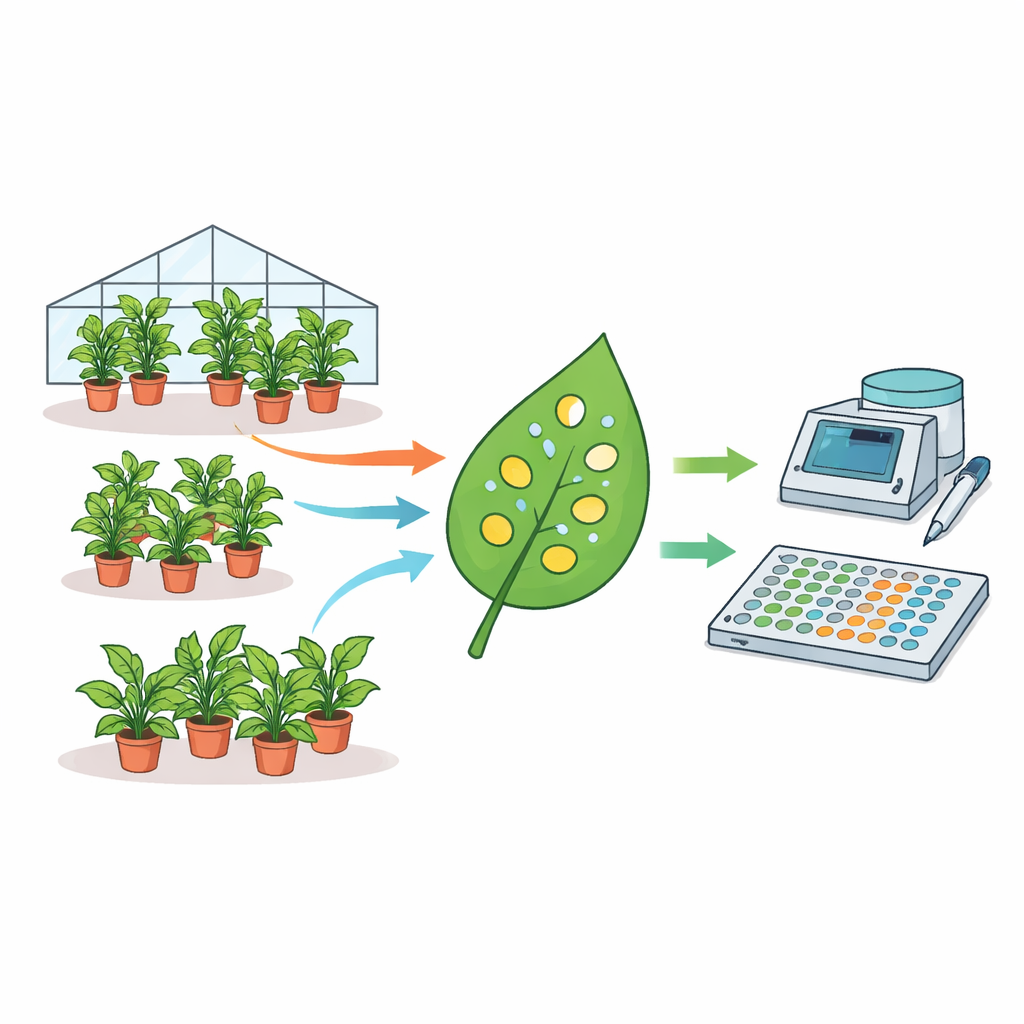
Les auteurs ont réuni un jeu de données exceptionnellement large : des mesures issues de 1 915 plants de N. benthamiana individuels collectées sur près de trois ans. Chaque plante a été infiltrée avec des bactéries Agrobacterium portant un gène rapporteur fluorescent, et de petits disques ont été percutés sur les feuilles puis lus sur un lecteur de plaque. À l’aide de modèles statistiques, ils ont décomposé l’origine de la variabilité. Ils ont constaté que les différences entre lots de plantes, entre plantes au sein d’un même lot, et même entre disques prélevés sur la même feuille contribuaient de manière substantielle à la dispersion globale de la fluorescence. En fait, les niveaux d’expression moyens pouvaient varier jusqu’à quatre fois entre des expériences nominalement identiques réalisées à des jours différents. Des facteurs tels que l’âge des plantes et le volume d’arrosage influençaient aussi l’intensité du signal, tandis que l’heure de la journée du prélèvement n’avait pas d’effet.
Tester des astuces pour réduire le bruit
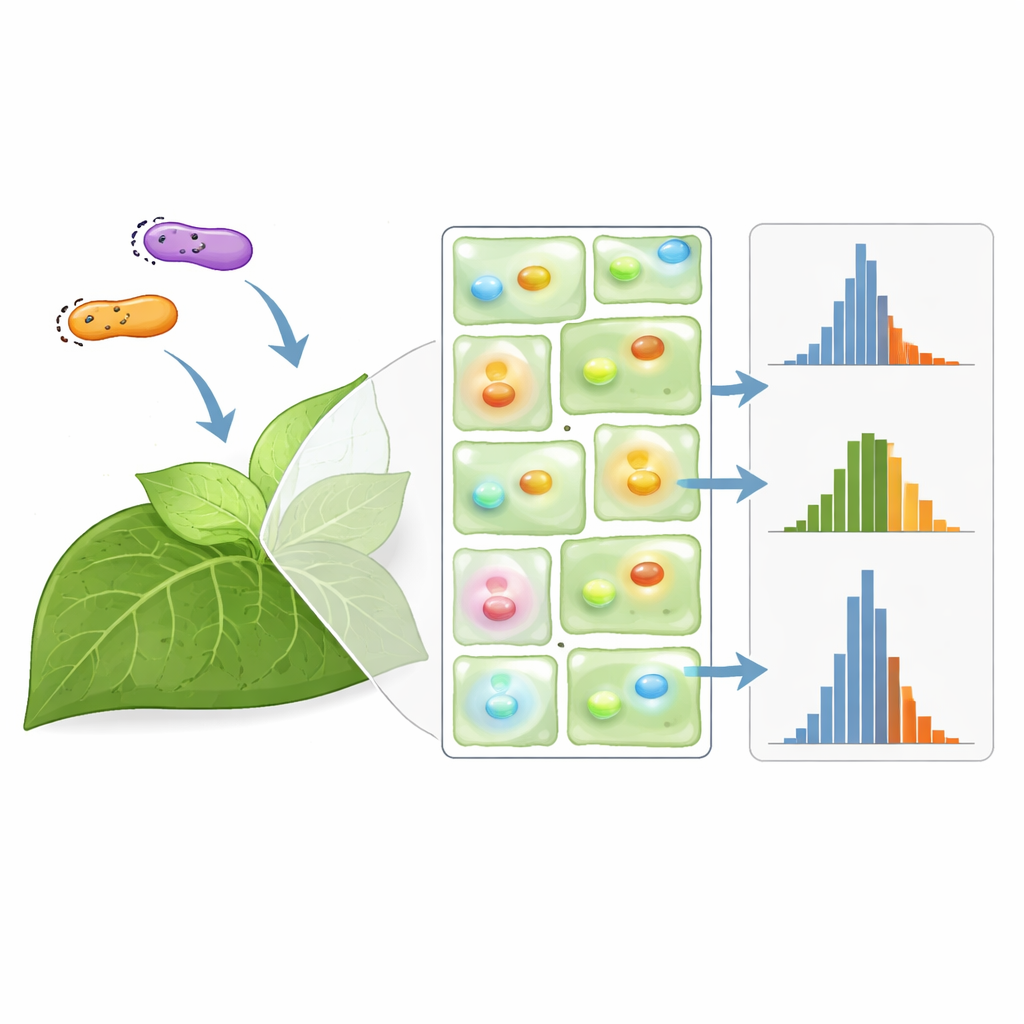
Pour diminuer cette dispersion, beaucoup de laboratoires utilisent un gène « normalisateur » : ils délivrent deux reporters fluorescents à la fois et analysent le rapport de leurs signaux, en espérant que les sources de bruit communes se compensent. L’équipe a comparé systématiquement 17 façons de co‑fournir ces double reporters, incluant le mélange de souches bactériennes séparées, l’empilement des deux gènes sur le même segment d’ADN, et l’usage de souches uniques portant deux plasmides. Ils ont montré que toutes ces stratégies peuvent modifier les niveaux d’expression de base, parfois de façon spectaculaire, selon l’orientation des gènes et le nombre de copies plasmidiques. De manière importante, la plupart — mais pas toutes — des méthodes de normalisation ont réduit la variation comparé à la mesure d’un seul reporter, l’infiltration conjointe de deux plasmides similaires s’avérant l’une des options les plus efficaces.
Quand des corrections utiles se retournent contre vous
L’histoire s’est avérée plus nuancée lorsque l’équipe a examiné les promoteurs — ces interrupteurs d’ADN qui contrôlent l’intensité d’expression des gènes. Ils ont testé des combinaisons de promoteurs faibles, moyens et forts pilotant les deux protéines fluorescentes. La normalisation fonctionnait le mieux lorsque les deux reporters utilisaient exactement le même promoteur ; dans ces conditions, le rapport présentait une dispersion beaucoup plus faible. Mais lorsque les promoteurs différaient, le rapport devenait parfois plus erratique que le signal brut d’un seul gène, détériorant en fait la puissance statistique. Les auteurs ont également constaté que l’ajustement de la densité des souches bactériennes modifiait principalement la luminosité des signaux, pas leur variabilité. Globalement, le travail montre que la normalisation n’est pas une solution universelle : son succès dépend fortement des détails de conception des montages.
Combien de plantes faut‑il ?
Fort de leur large jeu de données, les chercheurs ont construit une simulation de Monte Carlo pour modéliser la propagation de la variabilité dans des expériences typiques. Ils l’ont utilisée pour poser une question que tout expérimentateur se pose : compte tenu d’un certain niveau de bruit, combien de plantes faut‑il pour détecter de manière fiable une vraie différence entre deux montages ? Pour les souches d’Agrobacterium courantes, ils ont trouvé que des effets supérieurs à environ 50 % peuvent être détectés avec seulement quelques plantes, tandis que distinguer des différences inférieures à 20 % peut nécessiter des dizaines d’échantillons, parfois plus que ce qui est pratique. Une normalisation soigneusement choisie peut réduire légèrement ces besoins, en particulier lorsque des promoteurs identiques sont utilisés et que le nombre de plantes est limité, mais dans certains montages elle offre peu d’avantage.
Ce que cela signifie pour l’ingénierie végétale à venir
Pour les non‑spécialistes, le message clé est que même dans un système végétal apprécié et très pratique, le bruit expérimental est à la fois substantiel et maîtrisable. L’étude cartographie les sources de variation, montre que les méthodes de correction populaires peuvent aider ou nuire selon leur conception, et fournit des lignes directrices simples d’analyse de puissance pour planifier des expériences. En termes concrets, elle indique aux biologistes végétaux comment dimensionner leurs études pour ne pas confondre fluctuations aléatoires et effets biologiques réels, et comment concevoir des montages rapporteurs qui fournissent des comparaisons plus fiables. Ces enseignements devraient rendre N. benthamiana encore plus fiable comme plateforme pour tester rapidement des gènes, assembler de nouvelles voies métaboliques et faire progresser la biologie synthétique vers une ingénierie des systèmes vivants plus prévisible.
Citation: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Mots-clés: Nicotiana benthamiana, expression transitoire, biologie synthétique, variabilité expérimentale, Agrobacterium