Clear Sky Science · ru
Причины и последствия экспериментальной вариабельности при транзиентной экспрессии в Nicotiana benthamiana
Почему важны небольшие растительные эксперименты
Многие прорывы в растительной науке и биопроизводстве начинаются с простого приема: кратковременного превращения листьев в миниатюрные фабрики для тестирования. У вида Nicotiana benthamiana ученые могут быстро вводить новую ДНК и наблюдать результат в течение нескольких дней. Такая скорость сделала этот вид незаменимым для тестирования генов, построения метаболических путей и прототипирования биологических конструкций. Но как и при выпечке одного и того же рецепта в разных духовках, результаты могут отличаться от прогона к прогону. В этом исследовании ставится на первый взгляд простая, но важная задача: насколько воспроизводимы эти быстрые растительные тесты и что могут сделать исследователи, чтобы укротить шум и доверять тонким различиям в данных?
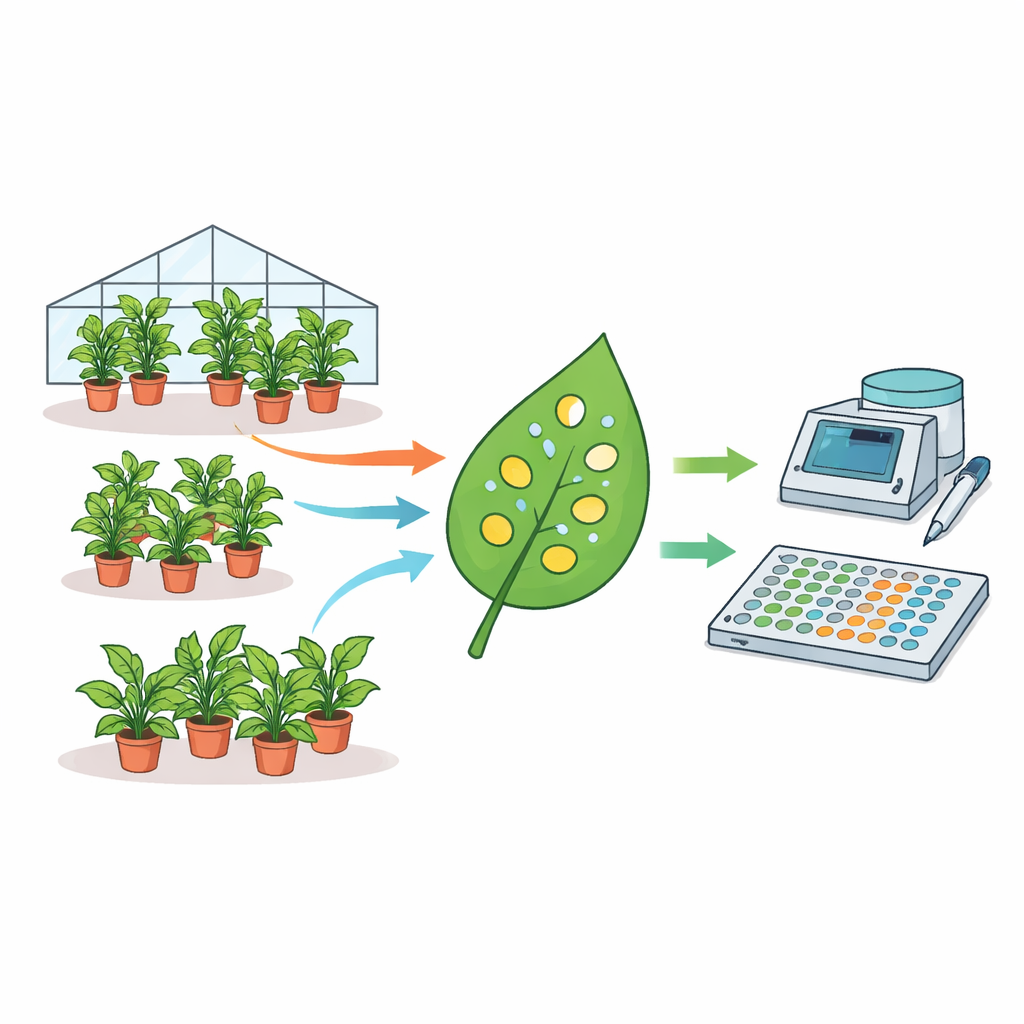
Почему любимый тестовый растение даёт разные ответы
Авторы собрали необычно большой набор данных: измерения с 1915 отдельных растений N. benthamiana, собранные в течение почти трех лет. Каждое растение инфильтрировали бактериями Agrobacterium, несущими флуоресцентный репортер, затем из листьев вырезали маленькие диски и считывали сигнал на планшетном ридере. С помощью статистических моделей они разложили, откуда берется вариабельность. Оказалось, что вклад в разброс флуоресценции вносят различия между сериями растений, между растениями внутри одной серии и даже между дисками с одного листа. Фактически средние уровни экспрессии могли отличаться до четырехкратного значения в номинально одинаковых экспериментах, выполненных в разные дни. На силу сигнала влияли такие факторы, как возраст растения и объем полива, тогда как время суток отбора проб влияния не показало.
Проверка трюков для выравнивания шума
Чтобы уменьшить этот разброс, многие лаборатории используют «нормализаторный» ген: вводят одновременно два флуоресцентных репортера и анализируют отношение их сигналов, рассчитывая, что общие источники шума компенсируются. Команда систематически сравнила 17 способов совместной доставки этих двойных репортеров, включая смешивание отдельных штаммов бактерий, размещение обоих генов на одном участке ДНК и использование одиночных штаммов с двумя плазмидами. Они показали, что все эти стратегии могут изменять базовые уровни экспрессии, иногда существенно, в зависимости от ориентации генов и копийности плазмид. Важно, что большинство — но не все — схемы нормализации действительно снижали вариативность по сравнению с измерением одного репортера, при этом простая совместная инфильтрация двух похожих плазмид оказалась одним из наиболее эффективных вариантов.
Когда полезные коррекции дают обратный эффект
Картина оказалась более сложной при изучении промоторов — переключателей на ДНК, контролирующих силу включения каждого гена. Они пробовали сочетания слабых, средних и сильных промоторов для управления двумя флуоресцентными белками. Нормализация работала лучше всего, когда оба репортера использовали точно один и тот же промотор; в этих условиях отношение сигналов демонстрировало гораздо меньший разброс. Но когда промоторы различались, отношение иногда становилось менее устойчивым, чем исходный сигнал одного гена, фактически уменьшая статистическую мощность. Авторы также выяснили, что изменение плотности бактериальных штаммов в основном меняло яркость сигналов, но не их вариабельность. В целом работа показывает, что нормализация не является универсальным решением: её успех во многом зависит от деталей конструкции.
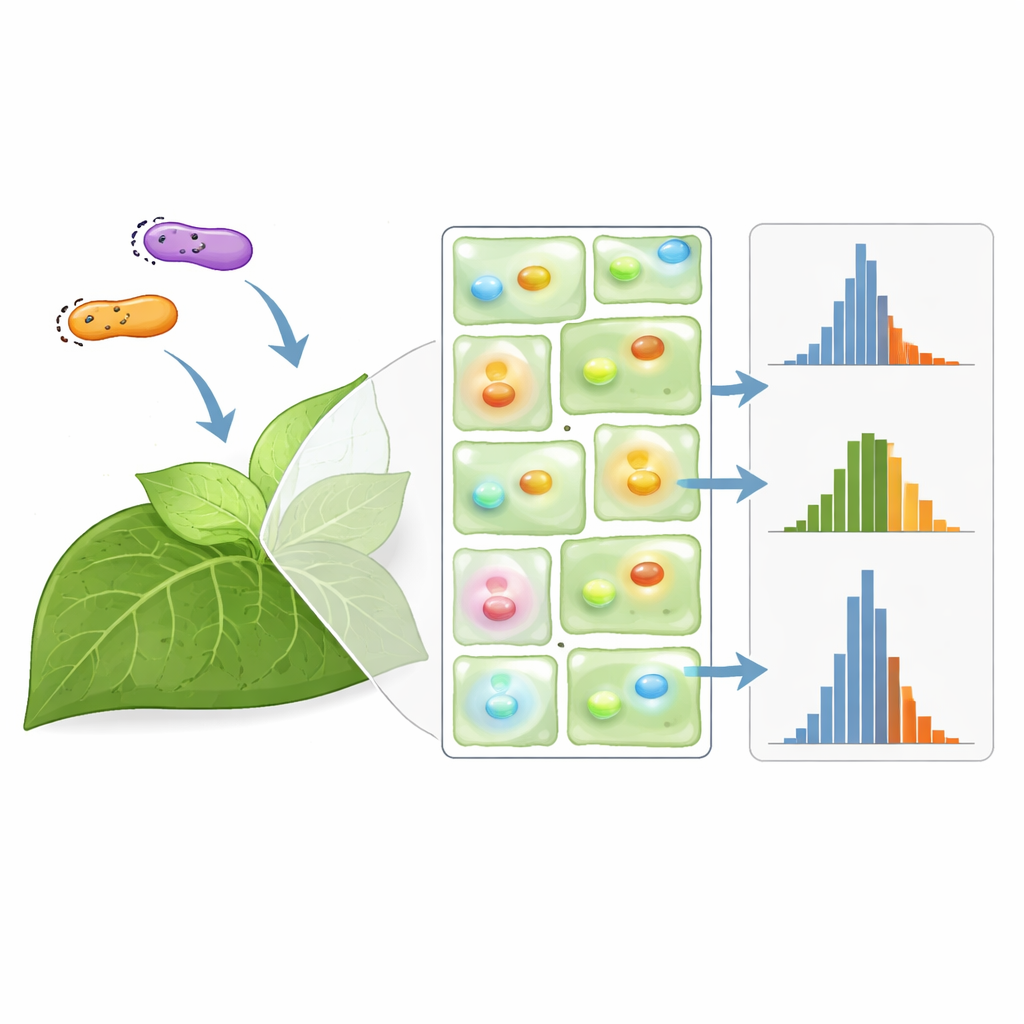
Сколько растений достаточно?
Опираясь на большой набор данных, исследователи построили модель методом Монте‑Карло, чтобы смоделировать, как вариабельность распространяется в типичных экспериментах. Они использовали её, чтобы ответить на вопрос, с которым сталкивается каждый экспериментатор: при данном уровне шума сколько растений нужно, чтобы надежно обнаружить реальную разницу между двумя конструкциями? Для распространенных штаммов Agrobacterium они обнаружили, что эффекты, превышающие примерно 50%, можно обнаружить с помощью всего нескольких растений, тогда как различение эффектов меньше 20% может потребовать десятков растений, порой больше, чем практически возможно. Тщательно подобранная нормализация немного сокращает эти числа, особенно когда используются одинаковые промоторы и доступно мало растений, но в некоторых конструкциях она почти не даёт преимущества.
Что это значит для будущей инженерии растений
Для неспециалистов главный вывод таков: даже в популярной и удобной растительной системе экспериментальный шум существенен, но с ним можно справиться. Исследование картирует источники вариации, показывает, что популярные методы коррекции могут помочь или навредить в зависимости от конструкции, и предоставляет простые рекомендации по анализу мощности для планирования экспериментов. Проще говоря, оно подсказывает растительным биологам, как рассчитать размер исследования, чтобы не принять случайные флуктуации за истинные биологические эффекты, и как проектировать репортерные конструкции для более надежных сравнений. Эти выводы должны сделать N. benthamiana еще более надежной платформой для быстрого тестирования генов, сборки новых метаболических путей и продвижения синтетической биологии к более предсказуемому инженерному управлению живыми системами.
Цитирование: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Ключевые слова: Nicotiana benthamiana, транзиентная экспрессия, синтетическая биология, экспериментальная вариабельность, Agrobacterium