Clear Sky Science · pt
Causas e consequências da variação experimental na expressão transitória de Nicotiana benthamiana
Por que experimentos pequenos com plantas importam
Muitas descobertas em ciência vegetal e manufatura baseada em biologia começam com um truque simples: transformar brevemente folhas em mini-fábricas de teste. Em Nicotiana benthamiana, pesquisadores podem introduzir novo DNA rapidamente e observar os resultados em poucos dias. Essa velocidade fez da planta uma ferramenta essencial para testar genes, construir vias metabólicas e prototipar novos projetos biológicos. Mas, como assar a mesma receita em fornos diferentes, os resultados podem variar de uma execução para outra. Este estudo faz uma pergunta aparentemente simples, com grandes consequências: quão consistentes são esses testes rápidos em plantas, e o que os pesquisadores podem fazer para domar o ruído e confiar em diferenças sutis nos dados?
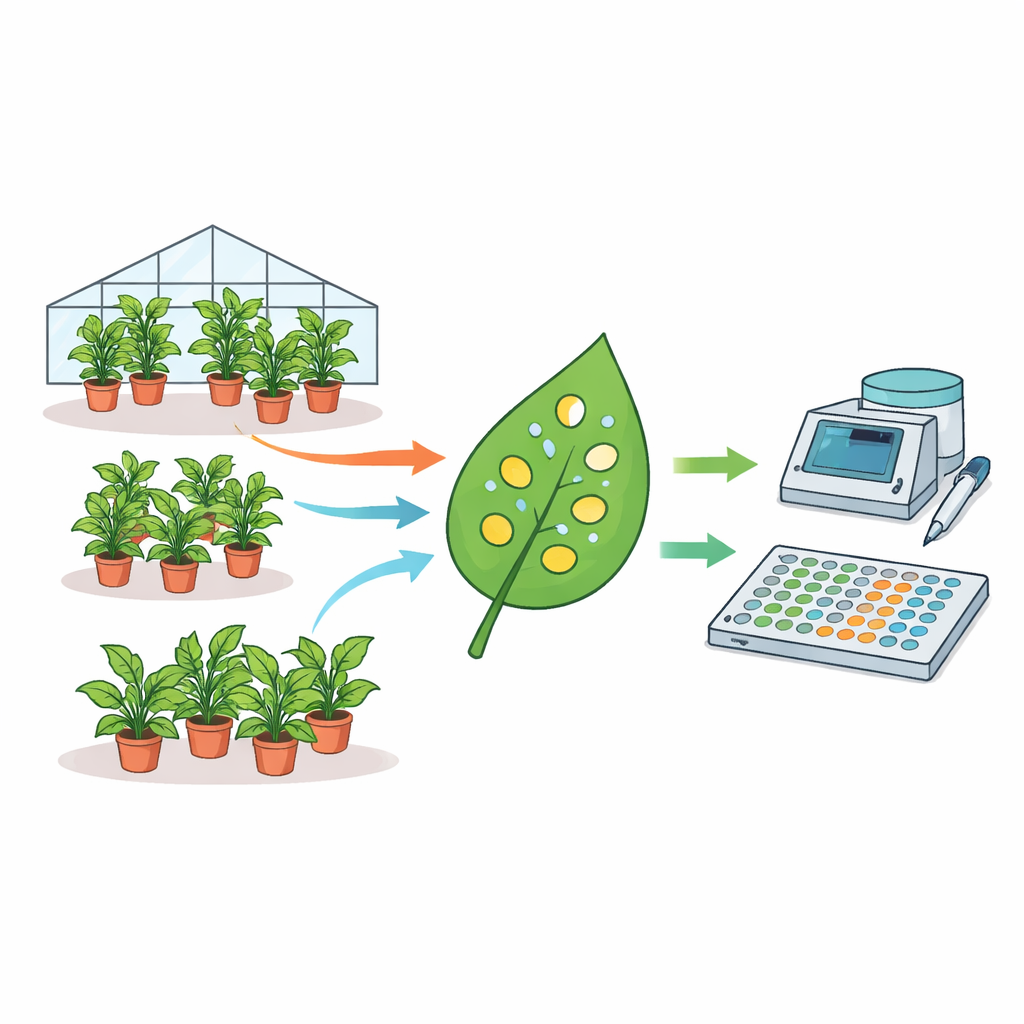
Como uma planta de teste favorita pode dar respostas diferentes
Os autores reuniram um conjunto de dados incomumente grande: medições de 1.915 plantas individuais de N. benthamiana coletadas ao longo de quase três anos. Cada planta foi infiltrada com bactérias Agrobacterium carregando um gene repórter fluorescente, e pequenos discos foram perfurados das folhas para leitura em um leitor de placas. Usando modelos estatísticos, eles decomporam de onde vem a variabilidade. Verificaram que diferenças entre lotes de plantas, entre plantas dentro de um mesmo lote e até entre discos retirados da mesma folha contribuíram substancialmente para a dispersão geral da fluorescência. De fato, níveis médios de expressão puderam variar em até quatro vezes entre experimentos nominalmente idênticos realizados em dias diferentes. Fatores como a idade da planta e o volume de rega também influenciaram a intensidade do sinal, enquanto a hora do dia da amostragem não teve efeito.
Testando truques para reduzir o ruído
Para reduzir essa dispersão, muitos laboratórios usam um gene “normalizador”: entregam dois repórteres fluorescentes ao mesmo tempo e analisam a razão entre seus sinais, esperando que fontes de ruído compartilhadas se cancelem. A equipe comparou sistematicamente 17 formas de co-entregar esses repórteres duplos, incluindo mistura de cepas bacterianas separadas, empilhar ambos os genes no mesmo segmento de DNA e usar cepas únicas que carregam dois plasmídeos. Demonstraram que todas essas estratégias podem alterar os níveis de expressão de linha de base, às vezes dramaticamente, dependendo da orientação dos genes e do número de cópias do plasmídeo. Importante: a maioria — mas não todas — das estratégias de normalização reduziu a variação em comparação com medir um único repórter, sendo a co-infiltração simples de dois plasmídeos semelhantes uma das opções mais eficazes.
Quando correções úteis atrapalham
A história mostrou-se mais sutil quando a equipe examinou promotores — os interruptores de DNA que controlam a intensidade de ativação de cada gene. Eles testaram combinações de promotores fracos, médios e fortes dirigindo as duas proteínas fluorescentes. A normalização funcionou melhor quando ambos os repórteres usavam exatamente o mesmo promotor; nessas condições, a razão apresentou muito menos dispersão. Mas quando os promotores diferiam, a razão às vezes tornou-se mais errática do que o sinal bruto de um único gene, na verdade piorando o poder estatístico. Os autores também descobriram que ajustar a densidade das cepas bacterianas mudou principalmente o brilho dos sinais, não sua variabilidade. No geral, o trabalho mostra que a normalização não é uma solução universal: seu sucesso depende fortemente dos detalhes do desenho do construto.
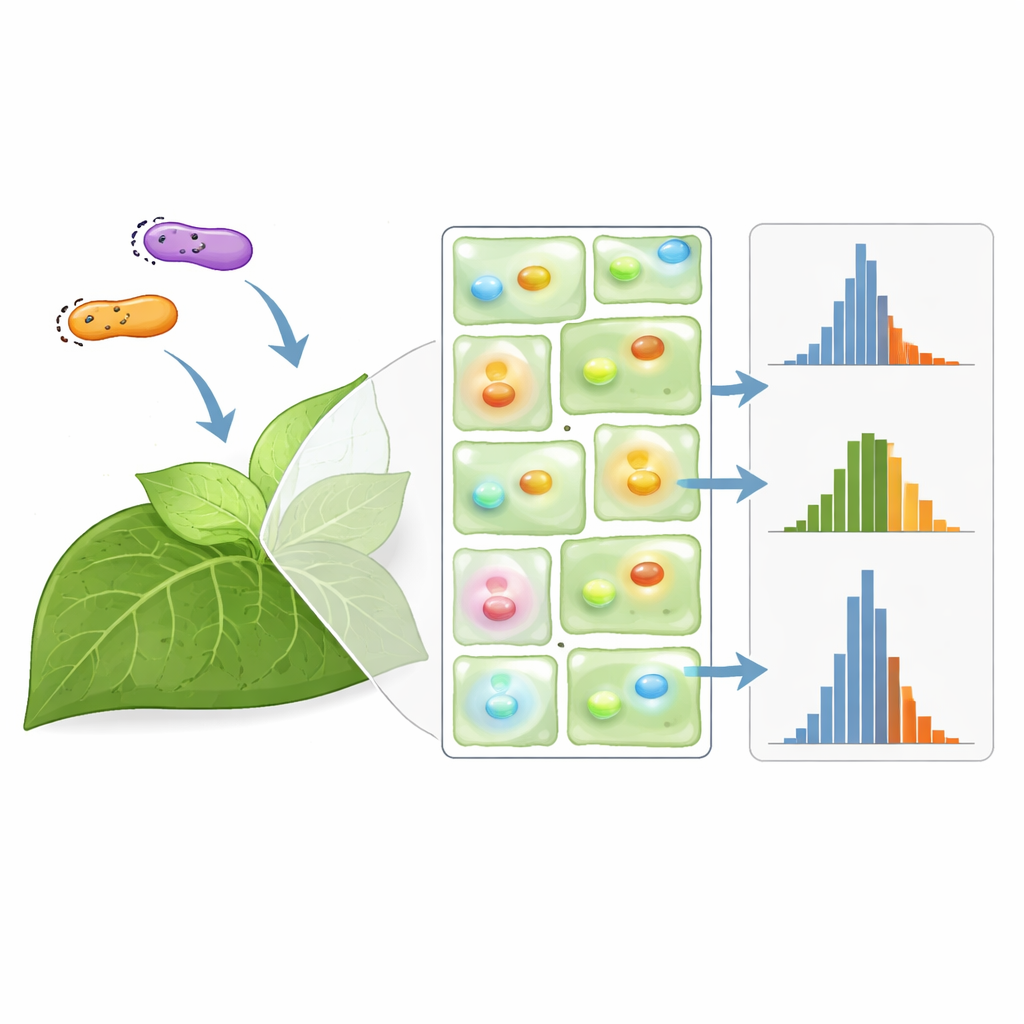
Quantas plantas são suficientes?
Munidos de seu grande conjunto de dados, os pesquisadores construíram uma simulação de Monte Carlo para modelar como a variabilidade se propaga em experimentos típicos. Usaram-na para responder a uma pergunta que todo experimentalista enfrenta: dado um certo nível de ruído, quantas plantas são necessárias para detectar de forma confiável uma diferença real entre dois construtos? Para cepas de Agrobacterium comuns, descobriram que efeitos maiores que cerca de 50% podem ser detectados com apenas algumas plantas, enquanto distinguir diferenças menores que 20% pode exigir dezenas, às vezes mais do que é prático. Normalizações escolhidas com cuidado podem reduzir esses números ligeiramente, particularmente quando promotores idênticos são usados e há poucas plantas disponíveis, mas em alguns desenhos oferecem pouca vantagem.
O que isso significa para o futuro da engenharia vegetal
Para não especialistas, a mensagem-chave é que mesmo em um sistema vegetal amplamente usado e muito conveniente, o ruído experimental é substancial, porém manejável. O estudo mapeia de onde vem a variação, mostra que métodos de correção populares podem ajudar ou atrapalhar dependendo de como são construídos, e fornece diretrizes simples de análise de poder para planejar experimentos. Em termos práticos, orienta os biólogos de plantas sobre como dimensionar seus estudos para não confundir flutuações aleatórias com efeitos biológicos reais e como projetar construtos repórteres que ofereçam comparações mais confiáveis. Esses insights devem tornar N. benthamiana uma plataforma ainda mais confiável para testar genes rapidamente, montar novas vias metabólicas e avançar a biologia sintética rumo a uma engenharia de sistemas vivos mais previsível.
Citação: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Palavras-chave: Nicotiana benthamiana, expressão transitória, biologia sintética, variabilidade experimental, Agrobacterium