Clear Sky Science · it
Cause e conseguenze della variabilità sperimentale nell’espressione transitoria di Nicotiana benthamiana
Perché contano gli esperimenti vegetali in piccolo
Molte scoperte nella ricerca sulle piante e nella produzione bio-based nascono da un trucco semplice: trasformare temporaneamente foglie di piante in piccole fabbriche di prova. Nella specie Nicotiana benthamiana, i ricercatori possono introdurre rapidamente nuovo DNA e osservare gli esiti nell’arco di pochi giorni. Questa velocità ha reso la pianta uno strumento prezioso per testare geni, costruire percorsi metabolici e prototipare nuovi progetti biologici. Ma come accade cuocendo la stessa ricetta in forni diversi, i risultati possono variare da esperimento a esperimento. Questo studio pone una domanda apparentemente semplice ma di grande impatto: quanto sono coerenti questi test rapidi su piante e cosa possono fare i ricercatori per domare il rumore e fidarsi di differenze sottili nei loro dati?
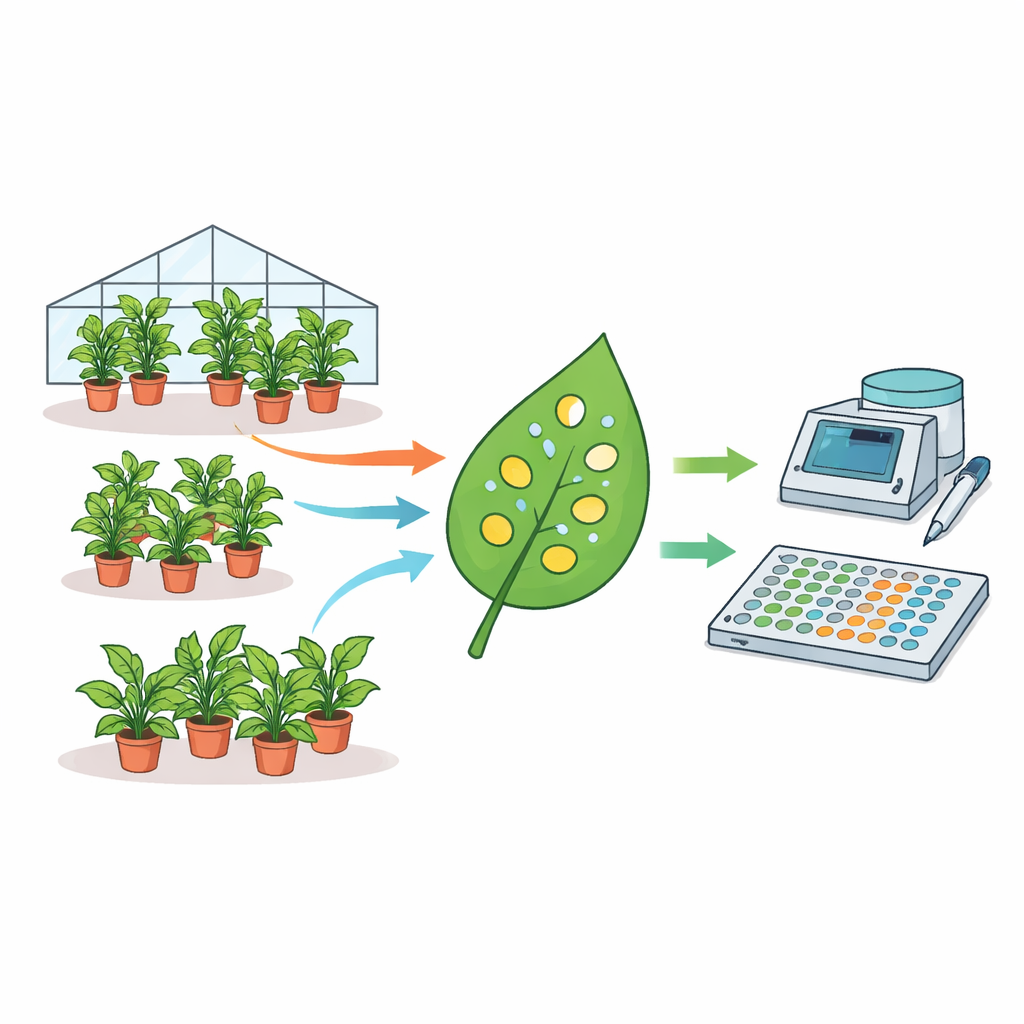
Come una pianta di laboratorio molto usata può dare risposte diverse
Gli autori hanno raccolto un dataset insolitamente ampio: misurazioni provenienti da 1915 piante individuali di N. benthamiana raccolte in quasi tre anni. Ogni pianta è stata infiltrata con batteri Agrobacterium che trasportavano un gene reporter fluorescente, e da ciascuna foglia sono stati prelevati piccoli dischi analizzati con un lettore di piastre. Con modelli statistici hanno scomposto le fonti di variabilità. Hanno trovato che le differenze tra lotti di piante, tra piante dello stesso lotto e persino tra dischi prelevati dalla stessa foglia contribuiscono in modo sostanziale alla dispersione complessiva della fluorescenza. In effetti, i livelli medi di espressione potevano variare fino a quattro volte tra esperimenti nominalmente identici svolti in giorni diversi. Fattori come l’età delle piante e il volume d’irrigazione hanno influenzato l’intensità del segnale, mentre l’ora del giorno in cui è stato effettuato il campionamento non lo ha fatto.
Provare stratagemmi per livellare il rumore
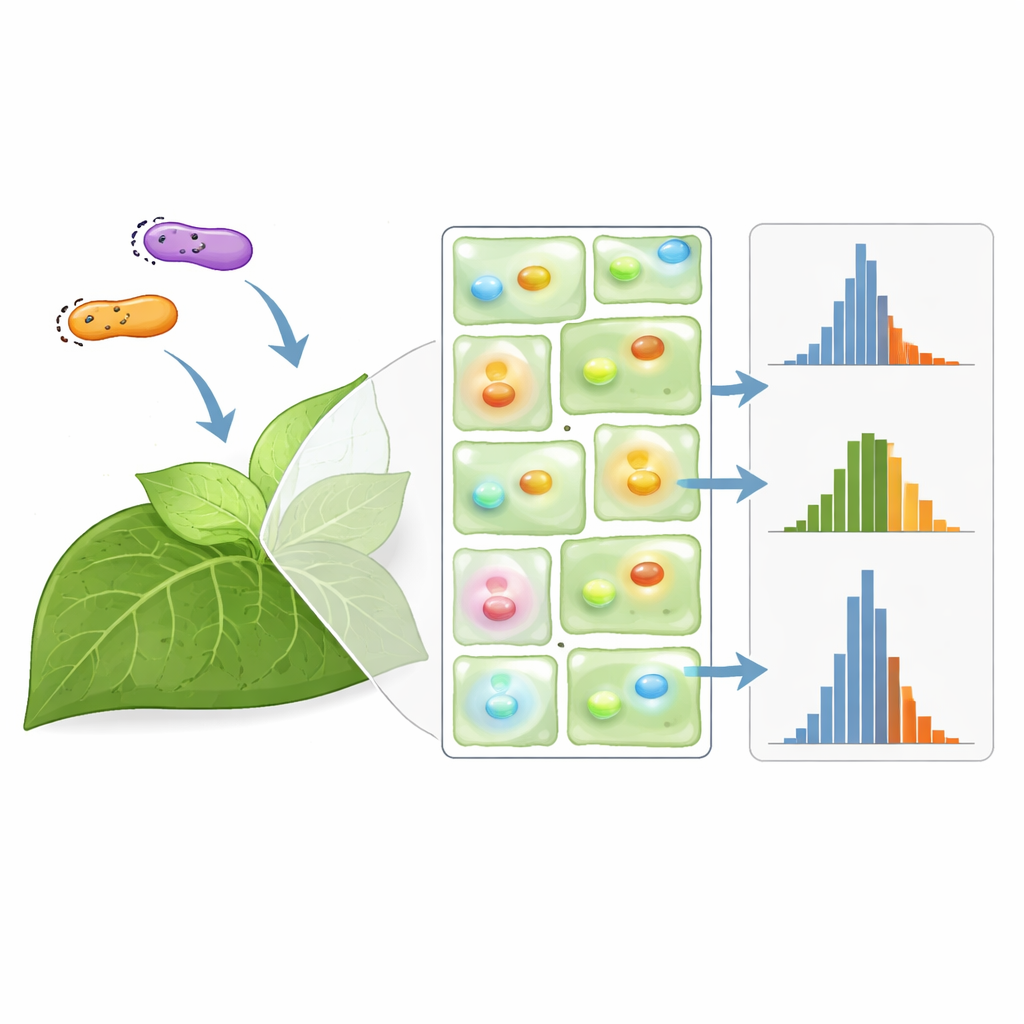
Per ridurre questa dispersione, molti laboratori usano un gene “normalizzatore”: vengono consegnati due reporter fluorescenti contemporaneamente e si analizza il rapporto tra i loro segnali, sperando che le fonti di rumore comuni si annullino. Il team ha confrontato sistematicamente 17 modi diversi di co-consegnare questi doppî reporter, tra cui miscelare ceppi batterici separati, impilare entrambi i geni sullo stesso segmento di DNA e usare ceppi singoli che portano due plasmidi. Hanno dimostrato che tutte queste strategie possono modificare i livelli di espressione di base, talvolta in modo drammatico, a seconda dell’orientamento del gene e del numero di copie del plasmide. È importante che la maggior parte — ma non tutte — le strategie di normalizzazione abbiano ridotto la variabilità rispetto alla misurazione di un singolo reporter: una semplice co-infiltrazione di due plasmidi simili è emersa come una delle opzioni più efficaci.
Quando le correzioni utili si ritorcono contro
La storia è risultata più sfumata quando il team ha esaminato i promotori — gli interruttori di DNA che controllano quanto intensamente viene attivato ogni gene. Hanno provato combinazioni di promotori deboli, medi e forti che guidavano le due proteine fluorescenti. La normalizzazione funzionava meglio quando entrambi i reporter usavano esattamente lo stesso promotore; in quelle condizioni il rapporto mostrava una dispersione molto minore. Ma quando i promotori differivano, il rapporto talvolta diventava più erratico del segnale grezzo di un singolo gene, peggiorando effettivamente la potenza statistica. Gli autori hanno anche riscontrato che modificare la densità dei ceppi batterici cambiava principalmente la luminosità dei segnali, non la loro variabilità. Nel complesso, il lavoro mostra che la normalizzazione non è una soluzione valida per tutte le situazioni: il suo successo dipende fortemente dai dettagli del design del costrutto.
Quante piante servono?
Muniti del loro ampio dataset, i ricercatori hanno costruito una simulazione Monte Carlo per modellare come la variabilità si propaga attraverso gli esperimenti tipici. L’hanno usata per porsi una domanda che ogni sperimentatore si trova ad affrontare: dato un certo livello di rumore, quante piante servono per rilevare in modo affidabile una differenza reale tra due costrutti? Per ceppi comuni di Agrobacterium hanno scoperto che effetti superiori a circa il 50% possono essere rilevati con poche piante, mentre distinguere differenze inferiori al 20% può richiedere decine di piante, talvolta più di quanto sia pratico. Una normalizzazione scelta con cura può ridurre leggermente questi numeri, soprattutto quando si usano promotori identici e si dispone solo di poche piante, ma in alcuni design offre poco vantaggio.
Cosa significa per l’ingegneria vegetale futura
Per i non specialisti, il messaggio chiave è che anche in un sistema vegetale molto diffuso e comodo, il rumore sperimentale è sia consistente sia gestibile. Lo studio mappa le sorgenti di variazione, mostra che i metodi di correzione popolari possono aiutare o danneggiare a seconda del loro design, e fornisce linee guida semplici di analisi della potenza per pianificare gli esperimenti. In termini pratici, indica ai biologi vegetali come dimensionare i loro studi per non confondere fluttuazioni casuali con effetti biologici reali e come progettare costrutti reporter che offrano confronti più affidabili. Queste intuizioni dovrebbero rendere N. benthamiana una piattaforma ancora più attendibile per testare rapidamente geni, assemblare nuovi percorsi metabolici e far progredire la biologia sintetica verso un’ingegneria dei sistemi viventi più prevedibile.
Citazione: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Parole chiave: Nicotiana benthamiana, espressione transitoria, biologia sintetica, variabilità sperimentale, Agrobacterium