Clear Sky Science · pl
Przyczyny i konsekwencje zmienności eksperymentalnej w przejściowej ekspresji u Nicotiana benthamiana
Dlaczego małe eksperymenty na roślinach mają znaczenie
Wiele przełomów w naukach o roślinach i produkcji opartej na biologii zaczyna się od prostego triku: krótkotrwałego przekształcenia liści roślin w miniaturowe fabryki testowe. W gatunku Nicotiana benthamiana naukowcy mogą szybko wprowadzić nowy DNA i zobaczyć efekty w ciągu kilku dni. Ta szybkość uczyniła roślinę narzędziem do testowania genów, budowania szlaków metabolicznych i prototypowania nowych projektów biologicznych. Jednak podobnie jak pieczenie tego samego przepisu w różnych piekarnikach, wyniki mogą się różnić między seriami. Badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach: jak spójne są te szybkie testy na roślinach i co badacze mogą zrobić, by okiełznać szum i zaufać subtelnym różnicom w danych?
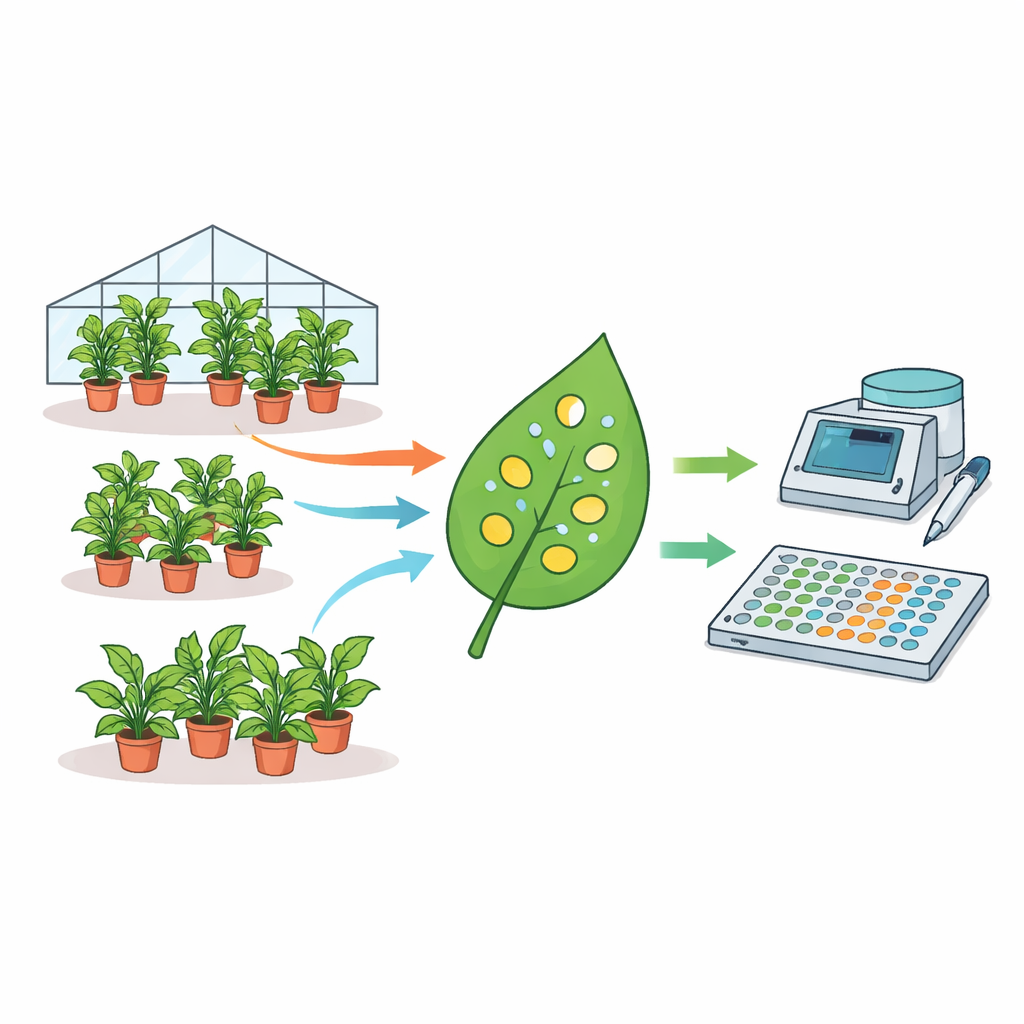
Dlaczego ulubiona roślina testowa może dawać różne odpowiedzi
Autorzy zebrali niezwykle dużą bazę danych: pomiary z 1915 pojedynczych roślin N. benthamiana zebrane w ciągu prawie trzech lat. Każdą roślinę zainfiltrowano bakteriami Agrobacterium niosącymi gen reporterowy kodujący fluorescencję, a z liści wycinano małe dyski, które następnie odczytywano w czytniku mikropłytek. Korzystając z modeli statystycznych, rozdzielili źródła zmienności. Stwierdzili, że różnice między partiami roślin, między roślinami w obrębie partii, a nawet między dyskami pobranymi z tego samego liścia miały znaczący wkład w ogólny rozrzut wartości fluorescencji. W rzeczywistości średnie poziomy ekspresji mogły różnić się nawet czterokrotnie między nominalnie identycznymi eksperymentami przeprowadzonymi w różne dni. Czynniki takie jak wiek rośliny i ilość podlewania wpływały na siłę sygnału, podczas gdy pora dnia pobrania próbek nie miała znaczącego wpływu.
Sprawdzanie sposobów na wyrównanie szumu
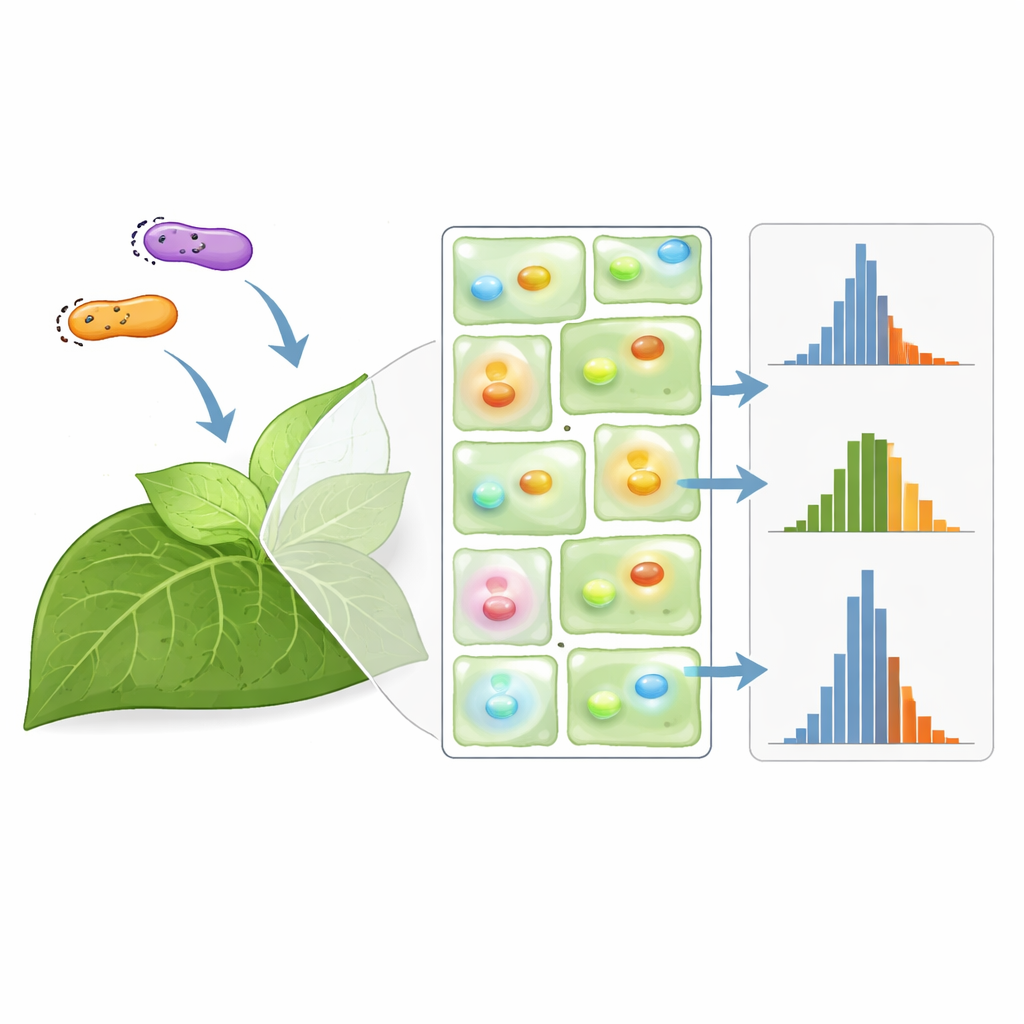
Aby zmniejszyć ten rozrzut, wiele laboratoriów stosuje gen „normalizujący”: dostarczają dwa reportery fluorescencyjne jednocześnie i analizują stosunek ich sygnałów, licząc na to, że wspólne źródła szumu się znoszą. Zespół systematycznie porównał 17 sposobów wspólnego dostarczania tych podwójnych reporterów, w tym mieszanie oddzielnych szczepów bakteryjnych, łączenie obu genów na tym samym fragmencie DNA oraz użycie pojedynczych szczepów niosących dwa plazmidy. Pokażali, że wszystkie te strategie mogą zmieniać poziomy ekspresji bazowej, czasem dramatycznie, w zależności od orientacji genów i liczby kopii plazmidu. Co ważne, większość — lecz nie wszystkie — schematy normalizacji zmniejszały zmienność w porównaniu z pomiarem pojedynczego reportera, przy czym prosty współinfiltracja dwóch podobnych plazmidów okazała się jednym z najskuteczniejszych rozwiązań.
Kiedy pomocne korekty zawodzą
Obraz stał się bardziej zniuansowany, gdy zespół przyjrzał się promotorom — przełącznikom DNA kontrolującym, jak silnie każdy gen jest włączany. Przetestowali kombinacje słabych, średnich i silnych promotorów napędzających dwa białka fluorescencyjne. Normalizacja działała najlepiej, gdy obie reportery używały dokładnie tego samego promotora; w takich warunkach stosunek sygnałów wykazywał znacznie mniejszy rozrzut. Jednak gdy promotory się różniły, stosunek czasami stawał się bardziej nieregularny niż surowy sygnał z pojedynczego genu, rzeczywiście pogarszając moc statystyczną. Autorzy zauważyli również, że zmiana gęstości szczepów bakteryjnych głównie zmieniała jasność sygnałów, a nie ich zmienność. Ogólnie praca pokazuje, że normalizacja nie jest uniwersalnym lekarstwem: jej skuteczność zależy w dużym stopniu od szczegółów konstrukcji.
Ile roślin to wystarczająco?
Posiadając dużą bazę danych, badacze zbudowali symulację Monte Carlo, by modelować, jak zmienność propaguje się przez typowe eksperymenty. Użyli jej, by odpowiedzieć na pytanie, z którym mierzy się każdy eksperymentator: przy danym poziomie szumu, ile roślin potrzeba, by wiarygodnie wykryć rzeczywistą różnicę między dwoma konstrukcjami? Dla powszechnych szczepów Agrobacterium stwierdzili, że efekty większe niż około 50 procent można wykryć przy zaledwie kilku roślinach, podczas gdy rozróżnienie różnic mniejszych niż 20 procent może wymagać dziesiątek, czasem więcej niż praktyczne. Starannie dobrana normalizacja może nieco zmniejszyć te liczby, szczególnie gdy używane są identyczne promotory i dostępnych jest tylko kilka roślin, ale w niektórych projektach oferuje niewielką korzyść.
Co to oznacza dla przyszłego inżynierstwa roślin
Dla osób spoza specjalności kluczowy przekaz jest taki, że nawet w chętnie używanym, bardzo wygodnym systemie roślinnym szum eksperymentalny jest zarówno znaczący, jak i możliwy do opanowania. Badanie mapuje źródła zmienności, pokazuje, że popularne metody korekcyjne mogą pomagać lub szkodzić w zależności od ich konstrukcji, i dostarcza prostych wskazówek dotyczących analizy mocy do planowania eksperymentów. W praktycznym wymiarze informuje biologów roślin, jak dobierać rozmiar badań, by nie mylić losowych fluktuacji z rzeczywistymi efektami biologicznymi, oraz jak projektować konstrukty reporterowe, które umożliwiają bardziej wiarygodne porównania. Te wnioski powinny uczynić N. benthamiana jeszcze bardziej niezawodną platformą do szybkiego testowania genów, składania nowych szlaków metabolicznych i przesuwania biologii syntetycznej w kierunku bardziej przewidywalnego inżynierowania systemów żywych.
Cytowanie: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Słowa kluczowe: Nicotiana benthamiana, przejściowa ekspresja, biologia syntetyczna, zmienność eksperymentalna, Agrobacterium