Clear Sky Science · sv
CSF1R T567M-mutation orsakar mikroglial dysfunktion och synaptisk försämring i patient‑iPSC‑härledda cerebrala organoider vid CSF1R-relaterad sjukdom
När hjärnans vårdare börjar fungera fel
Vissa sällsynta hjärnsjukdomar drabbar vuxna i livets mitt och tar gradvis minne, humör och rörelseförmåga — samtidigt som hjärnavbildning visar mystiska skador i vit substans, ledningarna som kopplar ihop hjärnregioner. Denna studie undersöker en sådan sjukdom kopplad till genen CSF1R, som styr hjärnans immunceller, mikroglia. Genom att odla små laboratorietillverkade hjärnmodeller från patientceller visar forskarna hur en enda genetisk förändring kan rubba dessa vårdare, störa hjärnans utveckling och försvaga de förbindelser mellan nervceller som ligger till grund för tanke och beteende.
En sällsynt men avslöjande hjärnsjukdom
CSF1R‑relaterad sjukdom är ett ärftligt, progressivt tillstånd som vanligen visar sig i vuxen ålder och ger kognitiv försämring, rörelsestörningar och psykiatriska symtom. Det är nära besläktat med en sjukdom som historiskt kallats ALSP, kännetecknad av skador i hjärnans vita substans. Många olika fel i CSF1R‑genen har identifierats, de flesta påverkar en region som fungerar som genens huvudsakliga på/av‑omkopplare. Det nya arbetet fokuserar på en nyligen upptäckt mutation, kallad T567M, som sitter utanför denna klassiska kontrollregion. Eftersom denna plats inte tidigare kopplats till sjukdom visste forskarna inte om eller hur den kunde orsaka så allvarliga hjärnskador.
Bygga mini‑hjärnor från patientceller
För att undersöka frågan tog teamet blodceller från en person med T567M‑mutationen och omprogrammerade dem till inducerade pluripotenta stamceller — en mångsidig celltyp som kan styras att bli olika vävnader. Från dessa skapade de två matchade cellsett: ett som behöll patientens mutation och ett annat som noggrant ”reparerades” med genredigeringsverktyg och fungerade som en frisk jämförelse. De odlade sedan tre viktiga hjärnkomponenter: mikroglia, nervceller och tredimensionella cerebrala organoider, små förenklade modeller av den utvecklande mänskliga hjärnan. Denna uppställning gjorde det möjligt att parallellt observera hur mutationen omformar hjärnceller och deras samspel.
Överaktiva mikroglia och stressat hjärnkopplingsnät
Mutationen försvagade CSF1R‑proteinet och förändrade dess kemiska aktivering vid en avgörande plats, vilket lämnade mikroglia delvis utan normal signalering. I odling blev de mutanta mikroglia mindre och mindre förgrenade, en form som förknippas med ett aktiverat, stressat tillstånd. De utsöndrade inflammatoriska molekyler och migrerade dåligt mot signaler som normalt skulle dra dem till skadade områden. Samtidigt visade de ett ökat intresse för att fagocytera omkringliggande material, inklusive myelin och pärlformiga partiklar som efterliknar cellulärt skräp. Genaktivitetsprofilering visade en förskjutning bort från program som stödjer nervcellstillväxt och synapser, och mot banor kopplade till immunaktivering. Tillsammans skapar dessa förändringar bilden av mikroglia som är överreaktiva men funktionellt komprometterade — dåligt rustade att stödja hälsosamma hjärnkretsar.
Stagnanta neuroner och försvagade signaler i mini‑hjärnor
Mutationen störde också nervcellernas egen utveckling. Tidiga prekursorceller delade sig mer än normalt, men färre mognade till fullutvecklade neuroner med långa, komplexa utskott. I cerebrala organoider odlade från mutanta celler minskade markörer för mogna neuroner, och elektriska inspelningar visade att neuronerna var mindre, avfyrade färre elektriska impulser och utbytte svagare signaler med sina grannar. Både excitatorisk och inhibitorisk kommunikation mellan celler sjönk kraftigt, vilket indikerar en bred försämring av synaptisk funktion. När mutanta mikroglia tillsattes till mutanta organoider föll nivåerna av viktiga synaptiska proteiner vid neuronernas kontaktpunkter ytterligare, medan friska mikroglia ökade dessa proteiner i normala organoider. Detta tyder på att felaktiga mikroglia och sårbara neuroner samverkar för att undergräva hjärnans kopplingar.
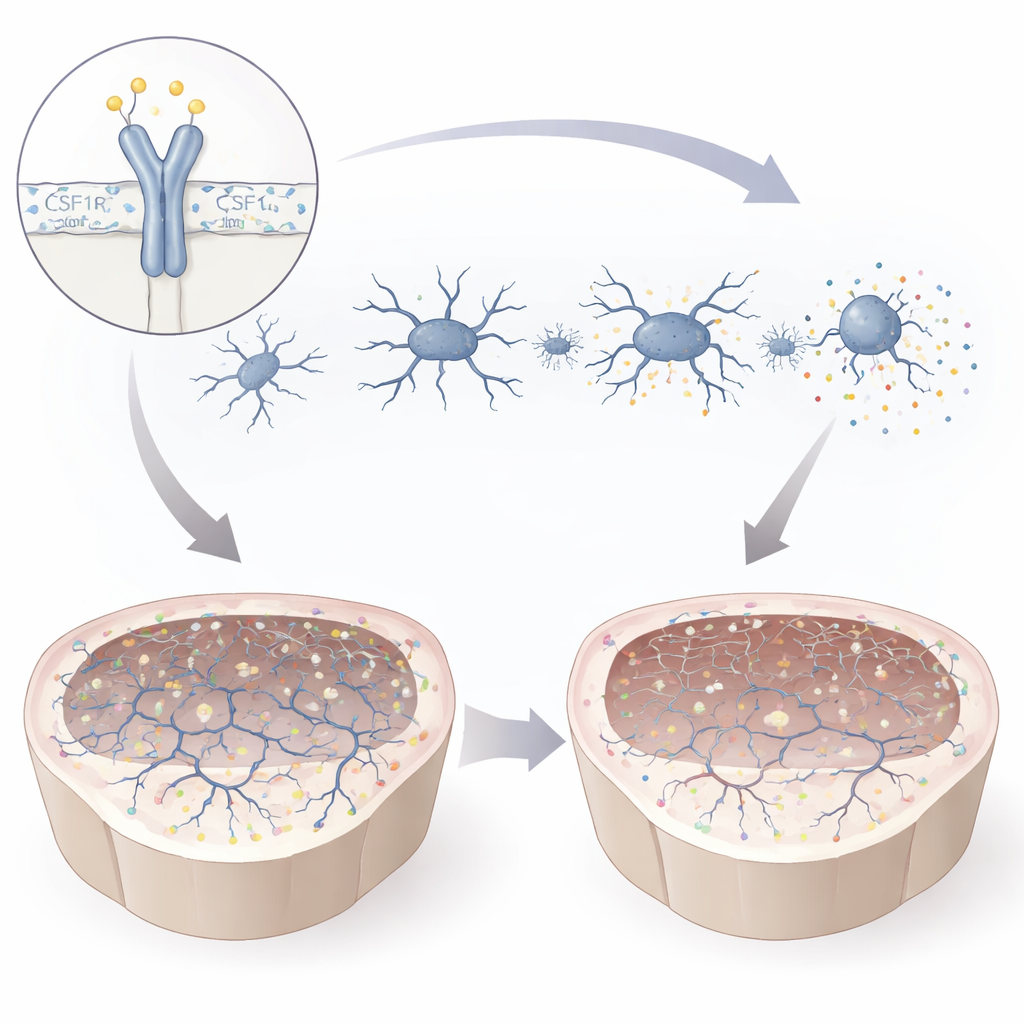
Vad detta betyder för patienter och framtida behandlingar
Genom att följa effekterna av T567M‑mutationen från gen till cell till mini‑hjärna visar studien att även en subtil förändring i CSF1R utanför dess huvudsakliga kontrollregion kan destabilisera mikroglia, sabotera hjärnans utveckling och försvaga synapser — vilket ger en rimlig förklaring till minnes‑ och rörelseproblemen hos patienter. Arbetet framhäver CSF1R‑signalering som en central väktare av "neural homeostas" — balansen som håller hjärnceller i flytande kommunikation. Lika viktigt är att de patient‑härledda två‑ och tredimensionella modellerna erbjuder en kraftfull testbädd för framtida terapier, från läkemedel som modulerar mikroglia till cellersättningsstrategier, vilket väcker hopp om att personanpassade behandlingar för CSF1R‑relaterade sjukdomar så småningom kan bli verklighet.
Citering: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
Nyckelord: CSF1R-relaterad sjukdom, mikroglia, cerebrala organoider, synaptisk dysfunktion, neurodegeneration