Clear Sky Science · fr
La mutation CSF1R T567M induit une dysfonction microgliale et un déficit synaptique dans des organoïdes cérébraux dérivés de cellules iPSC de patients atteints de trouble lié à CSF1R
Quand les gardiens du cerveau déraillent
Certaines maladies cérébrales rares frappent des adultes en pleine vie, privant progressivement de mémoire, d’humeur et de mobilité, tandis que les imageries cérébrales révèlent des lésions mystérieuses de la substance blanche — le câblage qui relie les régions du cerveau. Cette étude examine l’un de ces troubles lié au gène CSF1R, qui régule les cellules immunitaires du cerveau, appelées microglies. En cultivant de petits modèles cérébraux fabriqués en laboratoire à partir de cellules de patients, les chercheurs montrent comment un seul changement génétique peut déséquilibrer ces gardiens, perturber le développement du cerveau et affaiblir les connexions entre les neurones qui sous-tendent la pensée et le comportement.
Une maladie cérébrale rare mais révélatrice
Le trouble lié à CSF1R est une affection héréditaire et progressive qui apparaît généralement à l’âge adulte et provoque un déclin cognitif, des troubles du mouvement et des symptômes psychiatriques. Il est étroitement apparenté à une maladie historiquement appelée ALSP, caractérisée par des lésions de la substance blanche cérébrale. De nombreuses altérations du gène CSF1R ont été identifiées, la plupart touchant une région qui agit comme l’interrupteur principal du gène. Les travaux récents se concentrent sur une mutation découverte récemment, nommée T567M, qui se situe en dehors de cette région de contrôle classique. Comme ce site n’avait pas été associé à la maladie auparavant, les scientifiques ignoraient si et comment il pouvait provoquer de telles lésions cérébrales graves.
Construire des mini-cerveaux à partir de cellules de patients
Pour explorer cette question, l’équipe a prélevé des cellules sanguines d’une personne porteuse de la mutation T567M et les a reprogrammées en cellules souches pluripotentes induites — un type cellulaire polyvalent pouvant être dirigé vers de nombreux tissus. À partir de celles-ci, ils ont créé deux ensembles appariés de cellules : l’un conservait la mutation du patient, l’autre était « réparé » avec précision à l’aide d’outils d’édition génétique, servant de témoin sain. Ils ont ensuite développé trois composants cérébraux clés : des microglies, des neurones et des organoïdes cérébraux tridimensionnels, petits modèles simplifiés du cerveau humain en développement. Ce dispositif leur a permis d’observer, côte à côte, comment la mutation remodelait les cellules cérébrales et leurs interactions.
Microglies hyperactives et câblage cérébral en détresse
La mutation affaiblissait la protéine CSF1R et modifiait son activation chimique à un site crucial, laissant la microglie partiellement privée de son signal. En culture, les microglies mutantes devenaient plus petites et moins ramifiées, une morphologie associée à un état activé et stressé. Elles produisaient des molécules inflammatoires et migrèrent moins bien vers des signaux qui les attireraient normalement vers des zones lésées. Parallèlement, elles étaient plus enclines à engloutir le matériel environnant, y compris la myéline et des particules sphériques imitant des débris cellulaires. Le profilage de l’activité génique a révélé un déplacement loin des programmes favorisant la croissance neuronale et les synapses, et vers des voies liées à l’activation immunitaire. Pris ensemble, ces changements dessinent le portrait de microglies à la fois hyperréactives et fonctionnellement compromises — mal équipées pour soutenir des circuits cérébraux sains.
Neurones bloqués et signaux affaiblis dans les mini-cerveaux
La mutation perturbait aussi le développement des neurones eux-mêmes. Les précurseurs précoces se divisaient davantage que d’habitude, mais moins se différenciaient en neurones matures dotés de longues branches complexes. Dans les organoïdes cérébraux issus de cellules mutantes, les marqueurs de neurones matures étaient réduits, et les enregistrements électriques montraient que les neurones étaient plus petits, déclenchaient moins d’impulsions électriques et échangeaient des signaux plus faibles avec leurs voisins. Les communications excitatrices et inhibitrices entre cellules chutaient fortement, indiquant un déclin généralisé de la fonction synaptique. Lorsque des microglies mutantes étaient ajoutées à des organoïdes mutants, les niveaux de protéines synaptiques clés aux jonctions neuronales diminuaient encore plus, tandis que des microglies saines augmentaient ces mêmes protéines dans des organoïdes normaux. Cela suggère que des microglies défaillantes et des neurones vulnérables agissent de concert pour saper la connectivité cérébrale.
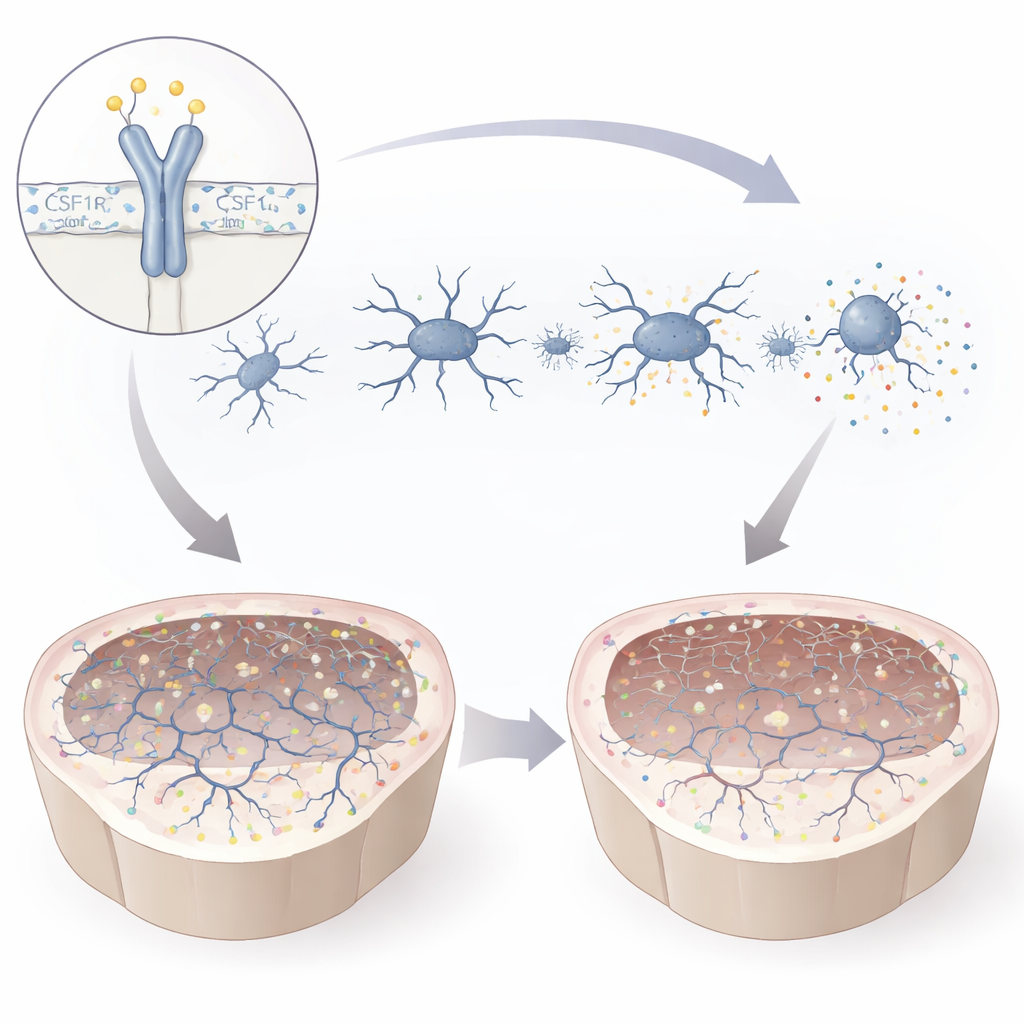
Ce que cela signifie pour les patients et les traitements futurs
En retraçant les effets de la mutation T567M du gène à la cellule puis au mini-cerveau, l’étude montre que même un changement subtil dans CSF1R, en dehors de sa principale région de contrôle, peut déstabiliser la microglie, faire dérailler le développement cérébral et affaiblir les synapses, offrant une explication plausible aux troubles de la mémoire et du mouvement observés chez les patients. Ces travaux mettent en lumière la signalisation CSF1R comme gardien central de l’« homéostasie neuronale » — l’équilibre qui permet aux cellules cérébrales de communiquer harmonieusement. Tout aussi important, les modèles patients en deux et trois dimensions offrent un terrain d’essai puissant pour de futurs traitements, des médicaments modulant la microglie aux stratégies de remplacement cellulaire, faisant naître l’espoir que des thérapies personnalisées pour les troubles liés à CSF1R puissent un jour voir le jour.
Citation: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
Mots-clés: trouble lié à CSF1R, microglie, organoïdes cérébraux, dysfonction synaptique, neurodégénérescence