Clear Sky Science · de
CSF1R T567M-Mutation verursacht Mikroglia-Dysfunktion und synaptische Beeinträchtigung in patientenabgeleiteten iPSC-Zerebraloiden bei CSF1R-assoziierter Erkrankung
Wenn die Pfleger des Gehirns aus dem Tritt geraten
Einige seltene Hirnerkrankungen treffen Erwachsene in der Blüte ihres Lebens, rauben Erinnerung, Stimmung und Bewegung, während Bildgebungen rätselhafte Schäden der weißen Substanz — der Leitungen zwischen den Hirnregionen — zeigen. Diese Studie untersucht eine solche Erkrankung, die mit dem Gen CSF1R verknüpft ist, das die Immunzellen des Gehirns, die Mikroglia, reguliert. Indem die Forschenden winzige, im Labor gezüchtete Gehirnmodelle aus Patientenzellen herstellen, zeigen sie, wie eine einzige genetische Veränderung diese Pfleger aus dem Gleichgewicht bringen, die Gehirnentwicklung stören und die Verbindungen zwischen Nervenzellen schwächen kann, die dem Denken und Verhalten zugrunde liegen.
Eine seltene, aber aufschlussreiche Hirnerkrankung
Die CSF1R-assoziierte Erkrankung ist eine vererbte, fortschreitende Störung, die typischerweise im Erwachsenenalter auftritt und zu kognitivem Abbau, Bewegungsstörungen und psychiatrischen Symptomen führt. Sie steht in engem Zusammenhang mit einer historisch als ALSP bezeichneten Krankheit, die durch Schäden an der weißen Substanz gekennzeichnet ist. Viele verschiedene Fehler im CSF1R-Gen wurden beschrieben, die meisten betreffen eine Region, die wie ein zentraler Ein-/Ausschalter des Gens wirkt. Die neue Arbeit konzentriert sich auf eine kürzlich entdeckte Mutation, T567M, die außerhalb dieser klassischen Kontrollregion liegt. Da dieser Punkt zuvor nicht mit Krankheit assoziiert war, war unklar, ob und wie er so schwere Hirnschäden verursachen könnte.
Mini-Gehirne aus Patientenzellen erzeugen
Um diese Frage zu untersuchen, entnahm das Team Blutzellen von einer Person mit der T567M-Mutation und reprogrammierte sie zu induzierten pluripotenten Stammzellen — einer vielseitigen Zellart, die zu vielen Geweben differenziert werden kann. Daraus erzeugten sie zwei matched Sets: eines behielt die Patientenmutation, das andere wurde mithilfe von Geneditierung präzise „repariert“ und diente als gesunder Vergleich. Anschließend züchteten sie drei zentrale Hirnkomponenten: Mikroglia, Nervenzellen und dreidimensionale zerebrale Organoide, kleine vereinfachte Modelle des sich entwickelnden menschlichen Gehirns. Dieses System ermöglichte es ihnen, nebeneinander zu beobachten, wie die Mutation Hirnzellen und deren Wechselwirkungen umgestaltet.
Überaktive Mikroglia und gestresste Leitungen des Gehirns
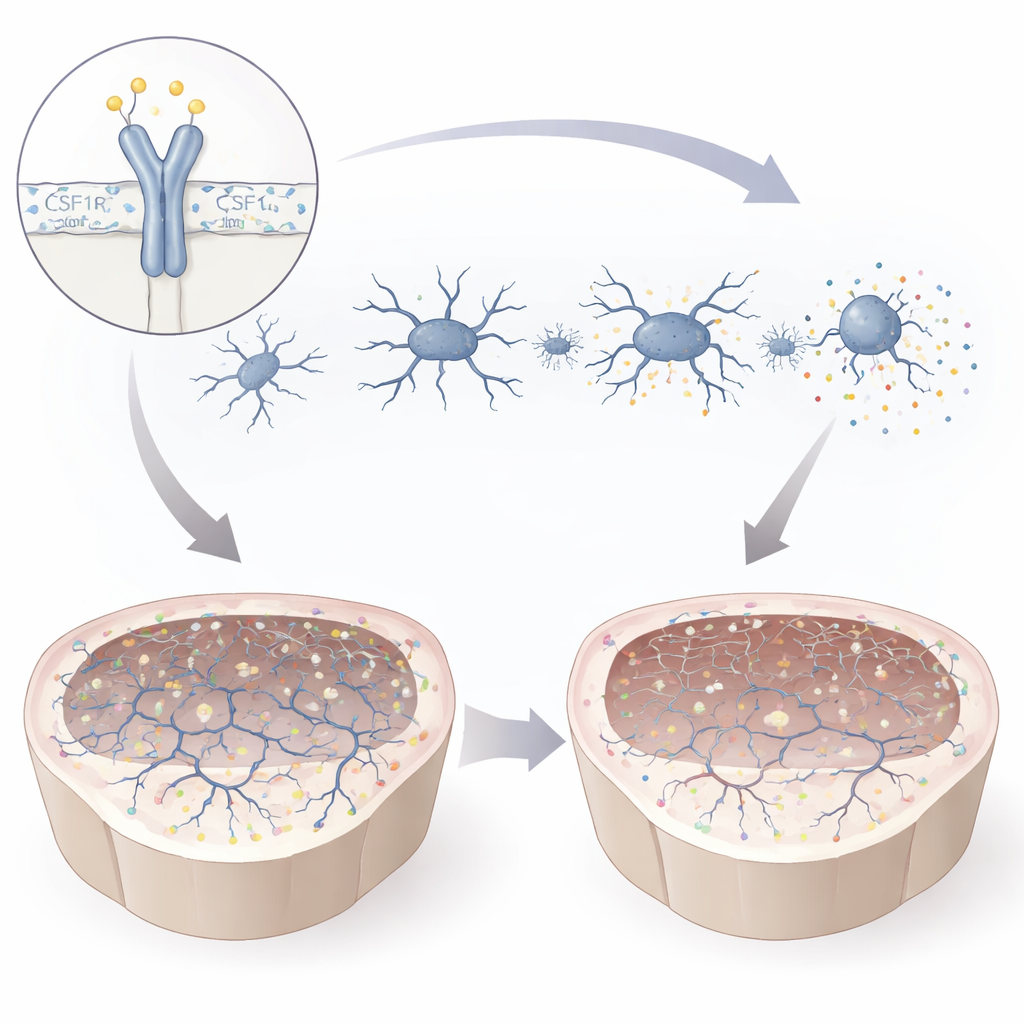
Die Mutation schwächte das CSF1R-Protein und veränderte dessen chemische Aktivierung an einer kritischen Stelle, sodass den Mikroglia Signal teilweise fehlte. In der Kultur wurden die mutierten Mikroglia kleiner und weniger verzweigt, eine Gestalt, die mit einem aktivierten, gestressten Zustand assoziiert ist. Sie schütteten entzündliche Moleküle aus und wanderten schlecht zu Reizen hin, die sie normalerweise zu verletzten Stellen locken würden. Gleichzeitig waren sie eifriger beim Aufnehmen von Umgebungsmaterial, einschließlich Myelin und perlenförmigen Partikeln, die zellulärem Schutt ähneln. Die Analyse der Genaktivität zeigte eine Verschiebung weg von Programmen, die das Wachstum von Nervenzellen und Synapsen unterstützen, hin zu Signalwegen, die mit Immunaktivierung verknüpft sind. Zusammengenommen zeichnen diese Veränderungen das Bild von Mikroglia, die sowohl überreagieren als auch funktionell beeinträchtigt sind — nur eingeschränkt in der Lage, gesunde neuronale Netzwerke zu unterstützen.
Gestörte Neuronen und abgeschwächte Signale in Mini-Gehirnen
Die Mutation beeinträchtigte auch die Entwicklung der Nervenzellen selbst. Frühe Vorläuferzellen teilten sich häufiger als üblich, aber weniger reiften zu voll ausgebildeten Neuronen mit langen, komplexen Verästelungen heran. In aus mutierten Zellen gezogenen zerebralen Organoiden waren Marker reifer Neuronen reduziert, und elektrische Aufzeichnungen zeigten, dass Neuronen kleiner waren, weniger elektrische Impulse feuerten und schwächere Signale an ihre Nachbarn übertrugen. Sowohl exzitatorische als auch inhibitorische Kommunikation zwischen Zellen nahm stark ab, was auf einen breiten Rückgang der synaptischen Funktion hinweist. Wenn mutierte Mikroglia in mutierte Organoide eingebracht wurden, fielen die Spiegel wichtiger synaptischer Proteine an den Verbindungsstellen noch stärker, während gesunde Mikroglia diese Proteine in normalen Organoiden verstärkten. Das deutet darauf hin, dass fehlerhafte Mikroglia und verwundbare Neuronen gemeinsam die Konnektivität des Gehirns untergraben.
Was das für Patienten und künftige Therapien bedeutet
Indem die Studie die Auswirkungen der T567M-Mutation vom Gen über die Zelle bis zum Mini-Gehirn nachzeichnet, zeigt sie, dass schon eine subtile Veränderung in CSF1R außerhalb seiner Hauptkontrollregion Mikroglia destabilisieren, die Gehirnentwicklung entgleisen und Synapsen schwächen kann — eine plausible Erklärung für die Gedächtnis- und Bewegungsstörungen bei Patienten. Die Arbeit hebt die CSF1R-Signalgebung als zentralen Wächter der „neuronal(en) Homöostase“ hervor — des Gleichgewichts, das die reibungslose Kommunikation der Gehirnzellen sicherstellt. Ebenso wichtig sind die patientenabgeleiteten zwei- und dreidimensionalen Modelle als mächtiger Prüfstand für künftige Therapien, von Wirkstoffen, die Mikroglia modulieren, bis hin zu Zellersatzstrategien, und wecken die Hoffnung, dass personalisierte Behandlungen für CSF1R-assoziierte Erkrankungen eines Tages erreichbar sein könnten.
Zitation: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
Schlüsselwörter: CSF1R-assoziierte Erkrankung, Mikroglia, zerebrale Organoide, synaptische Dysfunktion, Neurodegeneration