Clear Sky Science · es
La mutación CSF1R T567M induce disfunción microglial y deterioro sináptico en organoides cerebrales derivados de iPSC de pacientes con trastorno relacionado con CSF1R
Cuando los cuidadores del cerebro fallan
Algunas enfermedades cerebrales raras atacan a adultos en la plenitud de su vida, robando memoria, estado de ánimo y movimiento mientras las exploraciones muestran daño misterioso en la sustancia blanca: el cableado que conecta las regiones del cerebro. Este estudio investiga uno de esos trastornos ligado a un gen llamado CSF1R, que regula las células inmunitarias del cerebro, conocidas como microglía. Al cultivar diminutos modelos cerebrales en el laboratorio a partir de células de pacientes, los investigadores muestran cómo un único cambio genético puede desestabilizar a estos cuidadores, alterar el desarrollo cerebral y debilitar las conexiones entre las neuronas que sustentan el pensamiento y el comportamiento.
Una enfermedad cerebral rara pero reveladora
El trastorno relacionado con CSF1R es una condición hereditaria y progresiva que suele aparecer en la edad adulta y provoca deterioro cognitivo, problemas de movimiento y síntomas psiquiátricos. Está estrechamente vinculado a una enfermedad históricamente llamada ALSP, caracterizada por daño en la sustancia blanca del cerebro. Se han encontrado muchos errores distintos en el gen CSF1R, la mayoría de ellos afectan una región que actúa como el interruptor principal de encendido y apagado del gen. El trabajo nuevo se centra en una mutación descubierta recientemente, denominada T567M, que se sitúa fuera de esa región clásica de control. Como ese punto no se había relacionado antes con la enfermedad, los científicos no sabían si ni cómo podía causar un daño cerebral tan grave.
Construir mini-cerebros a partir de células de pacientes
Para explorar la cuestión, el equipo tomó células sanguíneas de una persona portadora de la mutación T567M y las reprogramó en células madre pluripotentes inducidas—un tipo celular versátil que puede dirigirse a muchos tejidos. A partir de ellas crearon dos juegos emparejados de células: uno conservó la mutación del paciente y el otro fue “reparado” con precisión mediante herramientas de edición génica, sirviendo como comparación sana. Luego desarrollaron tres componentes cerebrales clave: microglía, neuronas y organoides cerebrales tridimensionales, que son modelos pequeños y simplificados del cerebro humano en desarrollo. Este diseño les permitió observar, lado a lado, cómo la mutación remodelaba las células cerebrales y sus interacciones.
Microglía hiperactiva y cableado cerebral estresado
La mutación debilitó la proteína CSF1R y alteró su activación química en un sitio crucial, dejando a la microglía parcialmente sin la señal. En cultivo, la microglía mutante se volvió más pequeña y menos ramificada, una morfología asociada a un estado activado y estresado. Liberaron moléculas inflamatorias y migraron con dificultad hacia señales que normalmente las atraerían a zonas lesionadas. Al mismo tiempo, mostraron mayor tendencia a fagocitar material circundante, incluida la mielina y partículas esféricas que imitan restos celulares. El perfil de actividad génica reveló un desplazamiento desde programas que apoyan el crecimiento neuronal y las sinapsis hacia vías vinculadas a la activación inmune. En conjunto, estos cambios dibujan el retrato de una microglía tanto hiperreactiva como funcionalmente comprometida—poco equipada para sostener circuitos cerebrales sanos.
Neuronas estancadas y señales debilitadas en los mini-cerebros
La mutación también alteró el desarrollo de las propias neuronas. Las células precursoras tempranas se dividieron más de lo habitual, pero menos evolucionaron hasta convertirse en neuronas maduras con ramas largas y complejas. En los organoides cerebrales derivados de células mutantes, los marcadores de neuronas maduras se redujeron y los registros eléctricos mostraron que las neuronas eran más pequeñas, disparaban menos impulsos eléctricos e intercambiaban señales más débiles con sus vecinas. Tanto la comunicación excitatoria como la inhibitoria entre células cayó drásticamente, lo que indica un declive amplio en la función sináptica. Cuando se añadieron microglías mutantes a organoides mutantes, los niveles de proteínas sinápticas clave en las uniones entre neuronas disminuyeron aún más, mientras que la microglía sana aumentó estas mismas proteínas en organoides normales. Esto sugiere que la microglía defectuosa y las neuronas vulnerables actúan conjuntamente para socavar la conectividad cerebral.
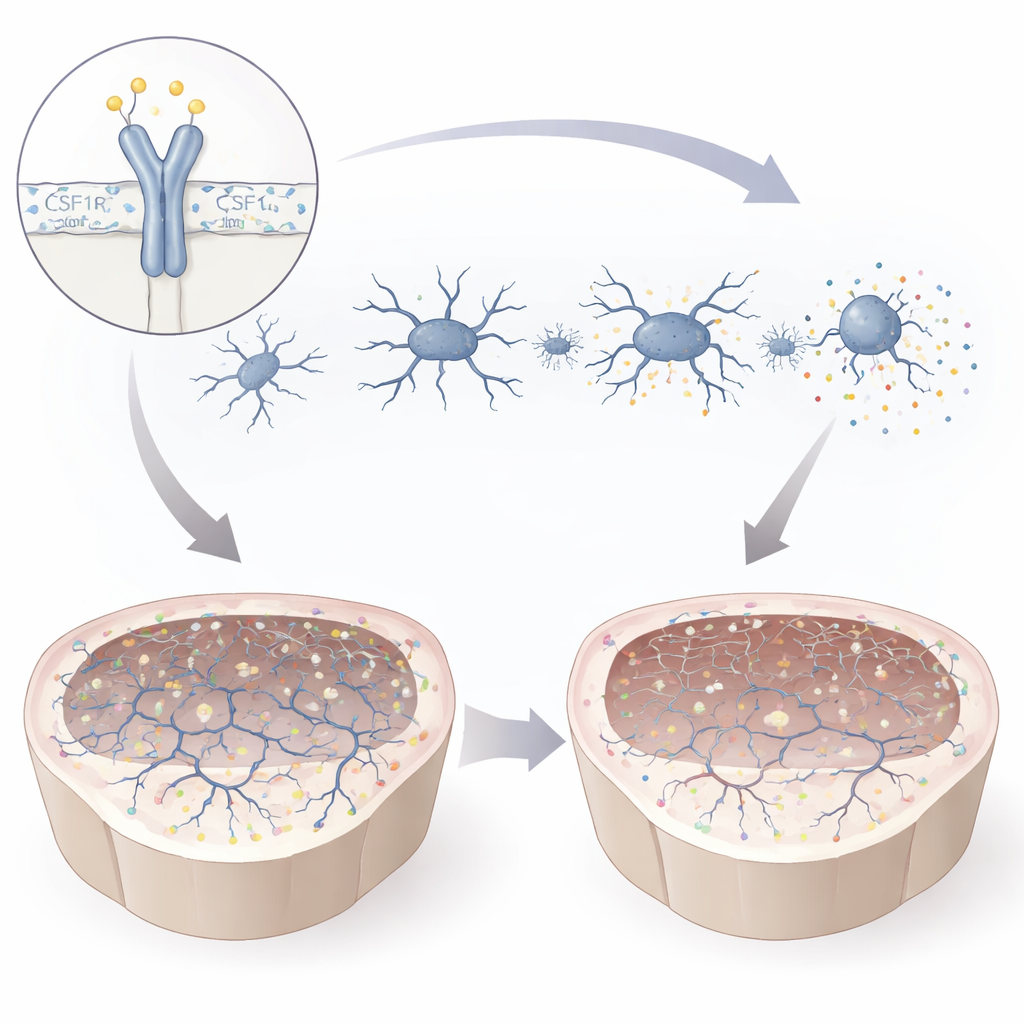
Qué significa esto para los pacientes y los tratamientos futuros
Al trazar los efectos de la mutación T567M desde el gen hasta la célula y el mini-cerebro, el estudio demuestra que incluso un cambio sutil en CSF1R fuera de su región de control principal puede desestabilizar la microglía, desviar el desarrollo cerebral y debilitar las sinapsis, ofreciendo una explicación plausible para los problemas de memoria y movimiento observados en pacientes. El trabajo pone de relieve la señalización de CSF1R como un guardián central de la «homeostasis neural»: el equilibrio que mantiene la comunicación fluida entre las células cerebrales. Igualmente importante, los modelos derivados del paciente en dos y tres dimensiones proporcionan un terreno de ensayo potente para futuras terapias, desde fármacos que modulen la microglía hasta estrategias de reemplazo celular, y abren la esperanza de que tratamientos personalizados para los trastornos relacionados con CSF1R puedan estar al alcance en el futuro.
Cita: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
Palabras clave: trastorno relacionado con CSF1R, microglía, organoides cerebrales, disfunción sináptica, neurodegeneración