Clear Sky Science · nl
CSF1R T567M-mutatie veroorzaakt microgliale disfunctie en synaptische aantasting in door iPSC afgeleide cerebrale organoïden van patiënten met CSF1R-gerelateerde aandoening
Wanneer de verzorgers van de hersenen ontsporen
Sommige zeldzame hersenaandoeningen treffen volwassenen op het hoogtepunt van hun leven, waarbij geheugen, stemming en beweging worden aangetast en hersenscans mysterieus letsel aan de witte stof laten zien — de bedrading die hersengebieden verbindt. Deze studie onderzoekt een van die aandoeningen die gekoppeld is aan het gen CSF1R, dat de immuuncellen van de hersenen, de microglia, helpt reguleren. Door kleine in het laboratorium gekweekte hersenmodellen uit cellen van patiënten te maken, laten de onderzoekers zien hoe één enkele genetische verandering deze verzorgers uit balans kan brengen, de hersenontwikkeling verstoort en de verbindingen tussen zenuwcellen die denken en gedrag ondersteunen, verzwakt.
Een zeldzame maar onthullende hersenaandoening
CSF1R-gerelateerde aandoening is een erfelijke, progressieve aandoening die gewoonlijk in de volwassenheid begint en cognitieve achteruitgang, bewegingsstoornissen en psychiatrische klachten veroorzaakt. Ze is nauw verwant aan een ziekte die historisch ALSP werd genoemd en die wordt gekenmerkt door schade aan de witte stof van de hersenen. Er zijn veel verschillende fouten in het CSF1R-gen gevonden, de meesten beïnvloeden een regio die fungeert als de belangrijkste aan/uit-schakelaar van het gen. Het nieuwe werk concentreert zich op een recent ontdekte mutatie, T567M, die buiten deze klassieke regelregio ligt. Omdat deze plek eerder niet aan ziekte was gekoppeld, wisten wetenschappers niet of en hoe hij zulke ernstige hersenschade kon veroorzaken.
Mini-hersen bouwen uit cellen van patiënten
Om deze vraag te onderzoeken, namen de onderzoekers bloedcellen van een persoon met de T567M-mutatie en programmeerden die terug tot geïnduceerde pluripotente stamcellen — een veelzijdig celtype dat kan worden gedifferentieerd naar veel weefsels. Hiervan creëerden ze twee overeenkomende sets cellen: één behield de mutatie van de patiënt en de andere werd nauwkeurig “gerepareerd” met genbewerkingstools en diende als een gezond vergelijk. Vervolgens kweekten ze drie belangrijke hersencomponenten: microglia, zenuwcellen en driedimensionale cerebrale organoïden, kleine vereenvoudigde modellen van het zich ontwikkelende menselijk brein. Deze opzet maakte het mogelijk om zij-aan-zij te observeren hoe de mutatie hersencellen en hun interacties herschikte.
Overactieve microglia en gestreste hersenbedrading
De mutatie verzwakte het CSF1R-eiwit en veranderde zijn chemische activering op een cruciale plaats, waardoor microglia gedeeltelijk tekort kwamen aan dat signaal. In kweek werden de mutante microglia kleiner en minder vertakt, een vorm die geassocieerd is met een geactiveerde, gestresseerde toestand. Ze produceerden ontstekingsmoleculen en migreerden slecht naar signalen die hen normaal naar beschadigde gebieden zouden lokken. Tegelijkertijd waren ze gretiger om omringend materiaal te fagocyteren, waaronder myeline en kralige deeltjes die cellulair puin nabootsen. Profilering van genactiviteit toonde een verschuiving weg van programma’s die zenuwcelgroei en synapsen ondersteunen, en naar routes gekoppeld aan immuunactivatie. Samen schetsen deze veranderingen een beeld van microglia die zowel overactief als functioneel aangetast zijn — slecht uitgerust om gezonde hersencircuits te ondersteunen.
Gestagneerde neuronen en verzwakte signalen in mini-hersen
De mutatie verstoorde ook de ontwikkeling van de zenuwcellen zelf. Vroege voorlopercellen deelden meer dan gebruikelijk, maar minder rijpten uit tot volledig ontwikkelde neuronen met lange, complexe uitlopers. In cerebrale organoïden gekweekt uit mutante cellen waren merkers van rijpe neuronen verminderd, en elektrische opnames toonden aan dat neuronen kleiner waren, minder elektrische impulsen produceerden en zwakkere signalen met hun buren uitwisselden. Zowel exciterende als inhiberende communicatie tussen cellen daalden sterk, wat wijst op een brede achteruitgang van de synaptische functie. Wanneer mutante microglia aan mutante organoïden werden toegevoegd, daalden de niveaus van belangrijke synaptische eiwitten op de verbindingen tussen neuronen nog verder, terwijl gezonde microglia diezelfde eiwitten juist verhoogden in normale organoïden. Dit suggereert dat defecte microglia en kwetsbare neuronen samen optreden om de connectiviteit van de hersenen te ondermijnen.
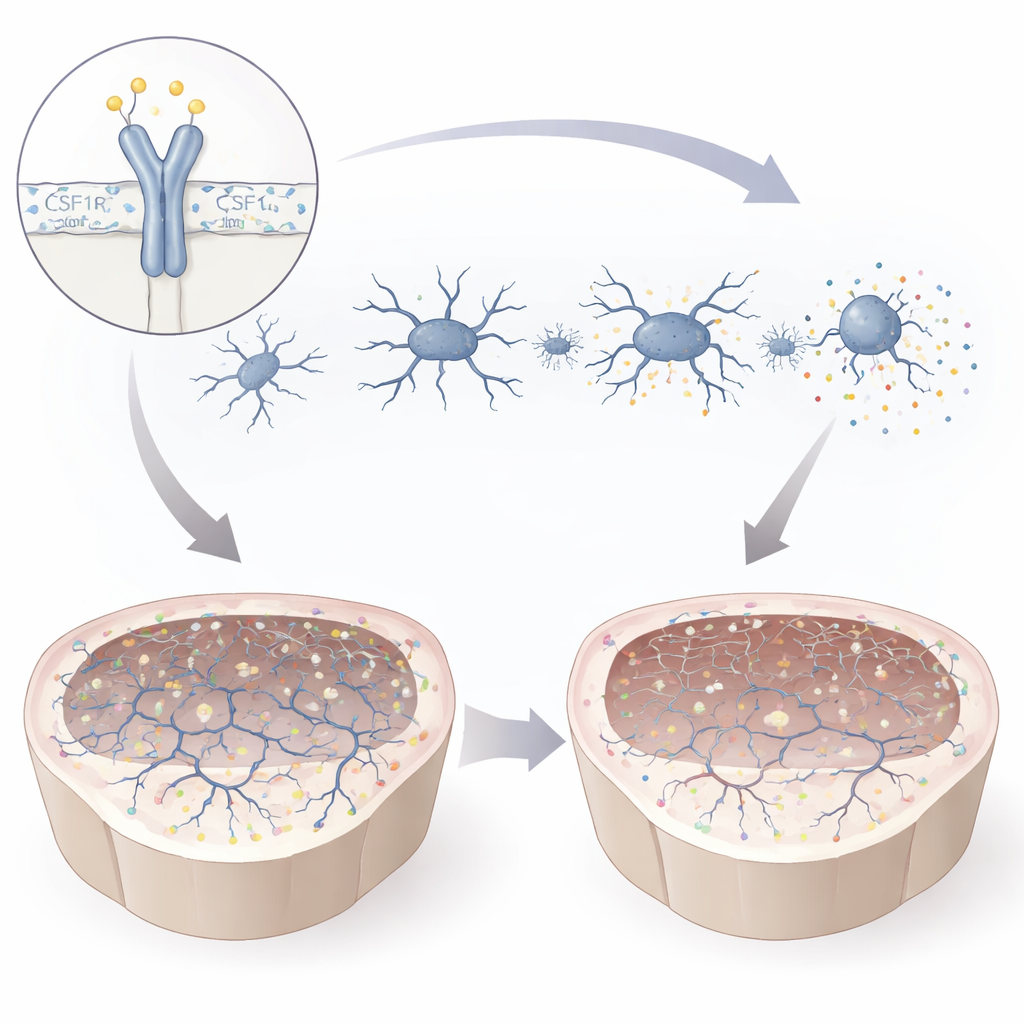
Wat dit betekent voor patiënten en toekomstige behandelingen
Door de effecten van de T567M-mutatie van gen naar cel naar mini-brein te volgen, laat de studie zien dat zelfs een subtiele verandering in CSF1R buiten zijn belangrijkste regelregio microglia kan destabiliseren, de hersenontwikkeling kan ontsporen en synapsen kan verzwakken, wat een plausibele verklaring biedt voor de geheugen- en bewegingsproblemen die bij patiënten worden gezien. Het werk benadrukt CSF1R-signaleringsroutes als een centraal bewaker van “neurale homeostase” — het evenwicht dat ervoor zorgt dat hersencellen soepel blijven communiceren. Even belangrijk bieden de uit patiënt afgeleide twee- en driedimensionale modellen een krachtig testveld voor toekomstige therapieën, van geneesmiddelen die microglia moduleren tot celvervangingstrategieën, wat hoop wekt dat gepersonaliseerde behandelingen voor CSF1R-gerelateerde aandoeningen mogelijk binnen bereik komen.
Bronvermelding: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
Trefwoorden: CSF1R-gerelateerde aandoening, microglia, cerebrale organoïden, synaptische disfunctie, neurodegeneratie