Clear Sky Science · ar
طفرة CSF1R T567M تُحدث خللاً في عمل الخلايا الدبقية الصغرى وتُضعف التشابك في أعضاء دماغية محاكاة مشتقة من خلايا iPSC لمَرَض مرتبط بـ CSF1R
عندما يختل عمل القائمين على رعاية الدماغ
بعض أمراض الدماغ النادرة تصيب البالغين في عزّ حياتهم، فتسرق الذاكرة والمزاج والحركة بينما تكشف صور المسح عن تلف غامض في المادّة البيضاء — الأسلاك التي تربط مناطق الدماغ. تَغُوص هذه الدراسة في أحد هذه الاضطرابات المرتبطة بجين يُدعى CSF1R، الذي يساهم في تنظيم خلايا المناعة في الدماغ المعروفة بالخلايا الدبقية الصغرى. من خلال زراعة نماذج دماغية صغيرة مصنوعة مختبريًا من خلايا المرضى، يبيّن الباحثون كيف يمكن لتغير وراثي واحد أن يخلّ بتوازن هؤلاء القائمين على الرعاية، ويعطل تطور الدماغ، ويضعف الاتصالات بين الخلايا العصبية التي تقوم عليها المعرفة والسلوك.
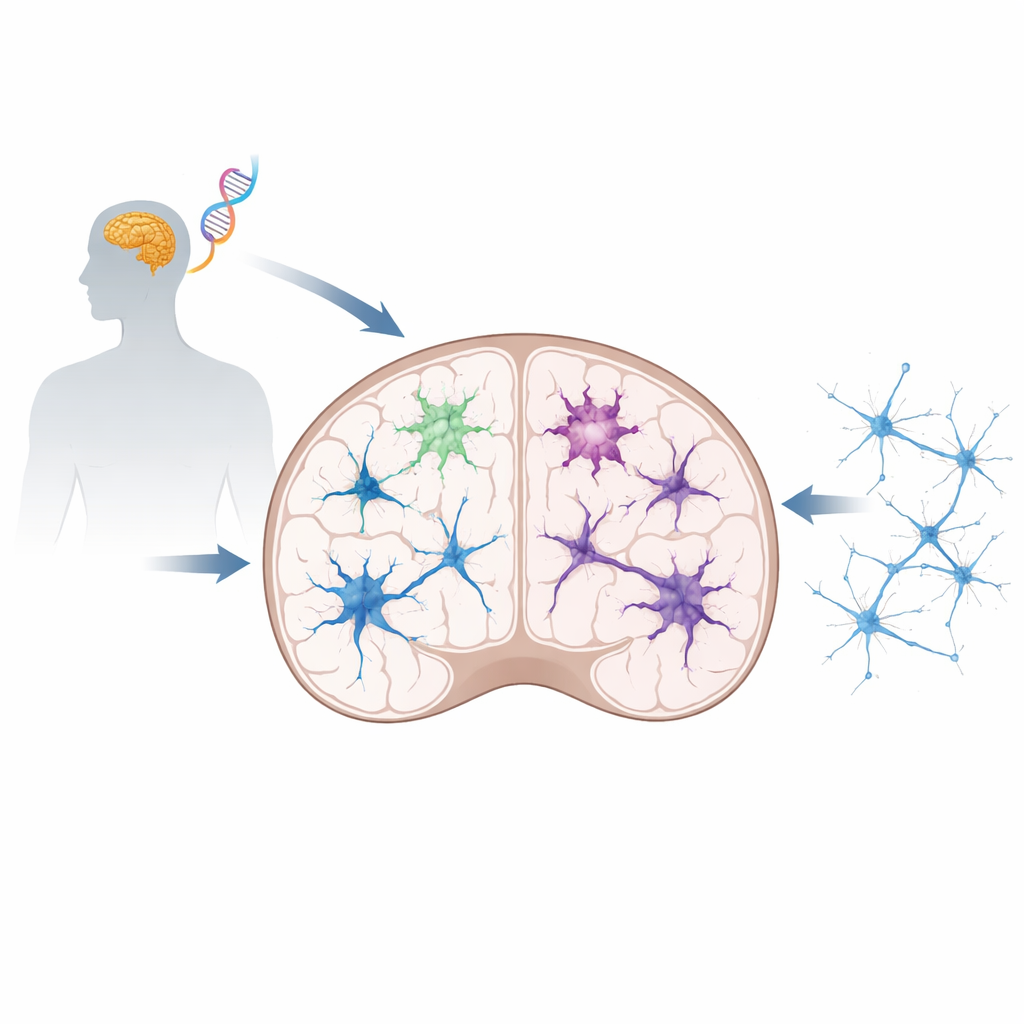
مرض دماغي نادر لكنه مُوحٍ
الاضطراب المرتبط بـ CSF1R هو حالة وراثية تقدمية تظهر عادة في مرحلة البلوغ وتسبب تدهورًا معرفيًا، ومشاكل حركية، وأعراضًا نفسية. يرتبط ارتباطًا وثيقًا بمرض كان يُعرف تاريخيًا باسم ALSP، والمُميّز بتلف المادّة البيضاء في الدماغ. وُجدت أخطاء متعددة في جين CSF1R، أغلبها يؤثر على منطقة تعمل كمفتاح تشغيل/إيقاف رئيسي للجين. يركّز العمل الجديد على طفرة اُكتُشفت مؤخرًا تُدعى T567M، تقع خارج هذه المنطقة الكلاسيكية للتحكم. وبما أن هذا الموقع لم يُربط سابقًا بالمرض، لم يُعرف إن كان وكيف يمكن أن يسبب مثل هذا التلف الدماغي الخطير.
بناء أدمغة مصغّرة من خلايا المرضى
لاستكشاف هذا السؤال، أخذ الفريق خلايا دموية من شخص يحمل طفرة T567M وأعاد برمجتها إلى خلايا جذعية مستحثة متعددة القدرات — نوع مرن من الخلايا يمكن دفعه ليتحوّل إلى أنسجة متنوعة. من هذه الخلايا، أنشأوا مجموعتين متطابقتين: إحداهما احتفظت بطفرة المريض، والأخرى «أُصلحت» بدقة باستخدام أدوات تحرير الجينات، لتعمل كمقارنة صحية. ثم نمّوا ثلاثة مكوّنات دماغية رئيسية: الخلايا الدبقية الصغرى، والخلايا العصبية، والأعضاء الدماغية ثلاثية الأبعاد، وهي نماذج صغيرة مبسطة للدماغ البشري النامي. أتاحهم هذا الإعداد مشاهدة، جنبًا إلى جنب، كيف أعادت الطفرة تشكيل خلايا الدماغ وتفاعلاتها.
خلايا دبقية صغرى مفرطة النشاط وأسلاك دماغية متوترة
أضعفت الطفرة بروتين CSF1R وغيرت نشاطه الكيميائي عند موقع حاسم، مما ترك الخلايا الدبقية الصغرى ناقصة جزئيًا من الإشارة. في المزرعة الخلوية، أصبحت الخلايا الدبقية الطافرة أصغر وأقل تشعّبًا، وهي حالة شكلية مرتبطة بالنشاط المجهد والمُنبه. أفرزت جزيئات التهابية وهاجرت بشكل سيئ نحو الإشارات التي عادة ما تجذبها إلى المناطق المصابة. في الوقت نفسه، أبدت ميلًا متزايدًا لاحتواء المادة المحيطة، بما في ذلك الميالين وجسيمات على شكل حبات تُحاكي الحطام الخلوي. كشف تحليل نشاط الجينات تحولًا بعيدًا عن البرامج التي تدعم نمو الخلايا العصبية والتشابكات، ونحو مسارات مرتبطة بتنشيط الجهاز المناعي. معًا، ترسم هذه التغيرات صورة خلايا دبقية صغرى مفرطة التفاعل ومُتضررة وظيفيًا — غير مجهزة بشكل جيد لدعم الدوائر الدماغية الصحية.
خلايا عصبية متوقفة وإشارات مُضعفة في الأدمغة المصغّرة
أربكت الطفرة أيضًا تطور الخلايا العصبية نفسها. انقسمت الخلايا السلفية المبكرة أكثر من المعتاد، لكن عددًا أقل منها نضج ليصبح خلايا عصبية مكتملة ذات تفرعات طويلة ومعقّدة. في الأعضاء الدماغية المحاكاة المأخوذة من خلايا طافرة، انخفضت مؤشرات الخلايا العصبية الناضجة، وأظهرت تسجيلات كهربائية أن الخلايا العصبية كانت أصغر، وأطلقت نبضات كهربائية أقل، وتبادلت إشارات أضعف مع جيرانها. انخفضت كل من الاتصالات المنشطة والكابحة بين الخلايا بشكل حاد، مما يشير إلى تراجع واسع في وظيفة المشابك. عندما أُضيفت الخلايا الدبقية الطافرة إلى الأعضاء الطافرة، تراجعت مستويات بروتينات مشبكية رئيسية عند نقاط التلاصق بين الخلايا بدرجة أكبر، في حين عززت الخلايا الدبقية السليمة هذه البروتينات في الأعضاء الطبيعية. وهذا يشير إلى أن الخلايا الدبقية المعيبة والخلايا العصبية الضعيفة تتعاونان في تقويض الترابط الدماغي.
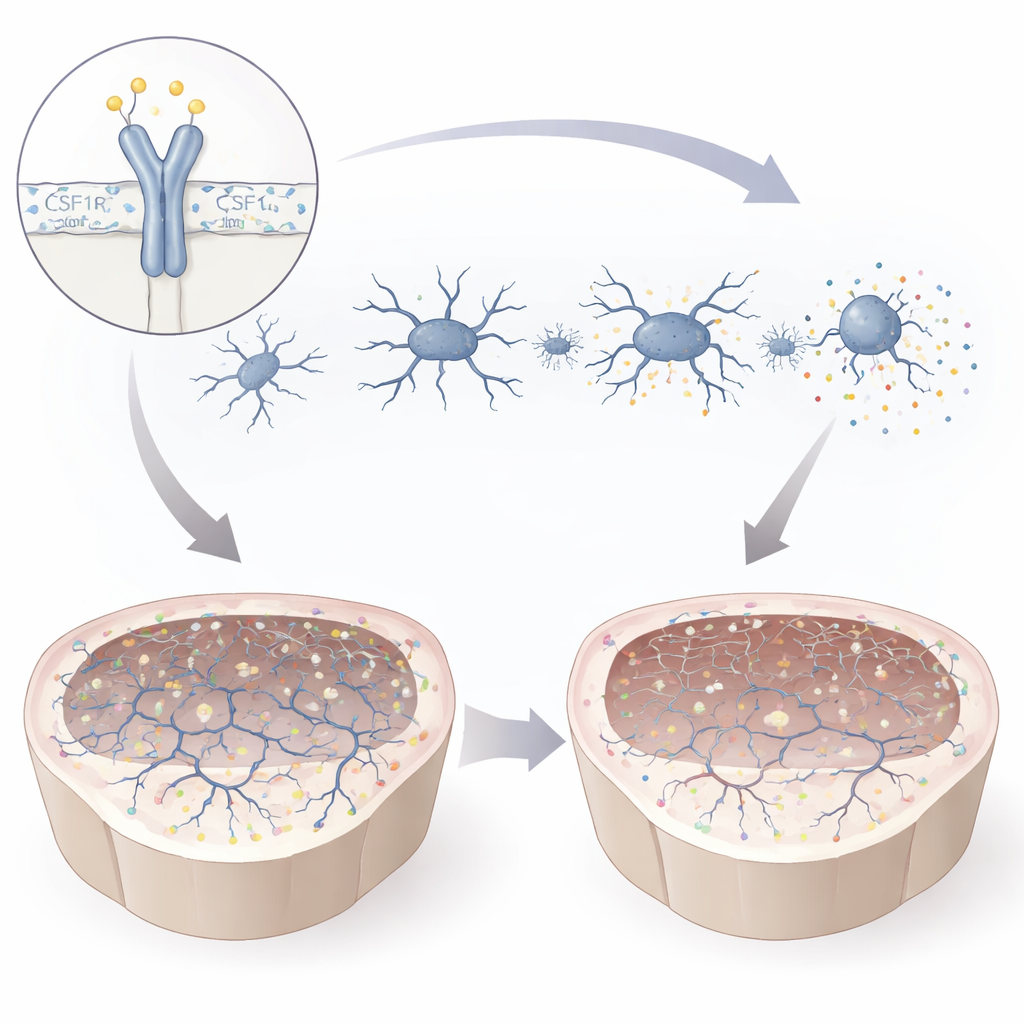
ما يعنيه هذا للمرضى والعلاجات المستقبلية
من خلال تتبع آثار طفرة T567M من الجين إلى الخلية إلى الدماغ المصغر، تُظهر الدراسة أن حتى تغييرًا طفيفًا في CSF1R خارج منطقة التحكم الرئيسية يمكن أن يزعزع الخلايا الدبقية الصغرى، ويعطل تطور الدماغ، ويضعف المشابك، مما يقدم تفسيرًا معقولًا لمشاكل الذاكرة والحركة التي يُعاني منها المرضى. يبرز العمل إشارة CSF1R كحارس مركزي لـ «التوازن العصبي» — التوازن الذي يحافظ على تواصل خلايا الدماغ بسلاسة. وبقدر أهمية ذلك، فإن النماذج المأخوذة من المرضى ثنائية وثلاثية الأبعاد توفر ميدان اختبار قويًا للعلاجات المستقبلية، من أدوية تعدّل عمل الخلايا الدبقية إلى استراتيجيات استبدال الخلايا، مما يثير الأمل في أن تصبح علاجات مخصّصة لاضطرابات مرتبطة بـ CSF1R متاحة يومًا ما.
الاستشهاد: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
الكلمات المفتاحية: اضطراب مرتبط بـ CSF1R, الخلايا الدبقية الصغرى, أعضاء دماغية محاكاة, اختلال تشابكي, تنكّس عصبي