Clear Sky Science · pl
Mutacja CSF1R T567M wywołuje dysfunkcję mikrogleju i upośledzenie synaps w organoidach mózgowych pochodzących z iPSC pacjentów z zaburzeniem związanym z CSF1R
Kiedy opiekunowie mózgu zawodzą
Niektóre rzadkie choroby mózgu uderzają w dorosłych w pełni sił, odbierając pamięć, nastrój i zdolność ruchu, podczas gdy badania obrazowe ujawniają tajemnicze uszkodzenia istoty białej — okablowania łączącego obszary mózgu. W tej pracy badamy jedno z takich zaburzeń związanych z genem CSF1R, który reguluje komórki odpornościowe mózgu, zwane mikroglejem. Hodując małe, laboratoryjne modele mózgu z komórek pacjenta, badacze pokazują, jak jedna zmiana genetyczna może wytrącić tych opiekunów z równowagi, zaburzyć rozwój mózgu i osłabić połączenia między komórkami nerwowymi, leżące u podstaw myślenia i zachowania.
Rzadka, lecz pouczająca choroba mózgu
Zaburzenie związane z CSF1R to dziedziczna, postępująca choroba, która zwykle ujawnia się w wieku dorosłym i powoduje pogorszenie funkcji poznawczych, problemy ruchowe oraz objawy psychiatryczne. Jest ściśle powiązana z chorobą historycznie nazywaną ALSP, charakteryzującą się uszkodzeniem istoty białej mózgu. Opisano wiele różnych błędów w genie CSF1R, z których większość dotyczy regionu pełniącego rolę głównego przełącznika on–off genu. Nowe badanie koncentruje się na niedawno odkrytej mutacji, zwanej T567M, która znajduje się poza tym klasycznym regionem kontrolnym. Ponieważ to miejsce wcześniej nie było powiązane z chorobą, naukowcy nie wiedzieli, czy i w jaki sposób może powodować tak poważne uszkodzenia mózgu.
Budowanie mini-mózgów z komórek pacjenta
Aby zbadać to zagadnienie, zespół pobrał komórki krwi od osoby noszącej mutację T567M i przeprogramował je do indukowanych pluripotentnych komórek macierzystych — wszechstronnego typu komórek, które można nakłonić do różnicowania w różne tkanki. Z tych komórek stworzono dwie sparowane linie: jedna zachowała mutację pacjenta, a druga została precyzyjnie „naprawiona” za pomocą narzędzi do edycji genów i służyła jako zdrowe porównanie. Następnie wyhodowano trzy kluczowe składniki mózgu: mikroglej, neurony i trójwymiarowe organoidy mózgowe — małe, uproszczone modele rozwijającego się ludzkiego mózgu. Takie przygotowanie pozwoliło obserwować obok siebie, jak mutacja przekształca komórki mózgowe i ich wzajemne interakcje.
Nadmiernie aktywny mikroglej i zestresowane okablowanie mózgowe
Mutacja osłabiła białko CSF1R i zmieniła jego chemiczną aktywację w kluczowym miejscu, pozostawiając mikroglej częściowo pozbawiony sygnału. W hodowli mikroglej z mutacją stał się mniejszy i mniej rozgałęziony — kształt kojarzony ze stanem aktywacji i stresu. Wydzielał molekuły zapalne i słabiej migrował w stronę sygnałów, które normalnie przyciągałyby go do uszkodzonych obszarów. Jednocześnie chętniej pochłaniał materiał otaczający, w tym mielinę i cząsteczki przypominające szczątki komórkowe. Profilowanie aktywności genów ujawniło przesunięcie z programów wspierających wzrost neuronów i synaps w stronę szlaków związanych z aktywacją układu odpornościowego. Razem te zmiany malują obraz mikrogleju jednocześnie nadreaktywnego i funkcjonalnie upośledzonego — słabo przygotowanego do wspierania zdrowych obwodów mózgowych.
Upośledzone neurony i osłabione sygnały w mini-mózgach
Mutacja zakłóciła także rozwój samych komórek nerwowych. Wczesne komórki prekursorowe dzieliły się częściej niż zwykle, ale mniej z nich różnicowało się w w pełni dojrzałe neurony o długich, złożonych rozgałęzieniach. W organoidach mózgowych pochodzących z komórek z mutacją zmniejszyła się liczba markerów dojrzałych neuronów, a zapisy elektryczne wykazały, że neurony były mniejsze, wyładowywały mniej impulsów elektrycznych i wymieniały słabsze sygnały z sąsiadami. Zarówno komunikacja pobudzająca, jak i hamująca między komórkami spadła gwałtownie, co wskazuje na szeroki spadek funkcji synaptycznej. Gdy do mutacyjnych organoidów dodano mutacyjny mikroglej, poziomy kluczowych białek synaptycznych na złączach między neuronami spadły jeszcze bardziej, podczas gdy zdrowy mikroglej podnosił te same białka w normalnych organoidach. Sugeruje to, że wadliwy mikroglej i wrażliwe neurony działają razem, osłabiając łączność mózgu.
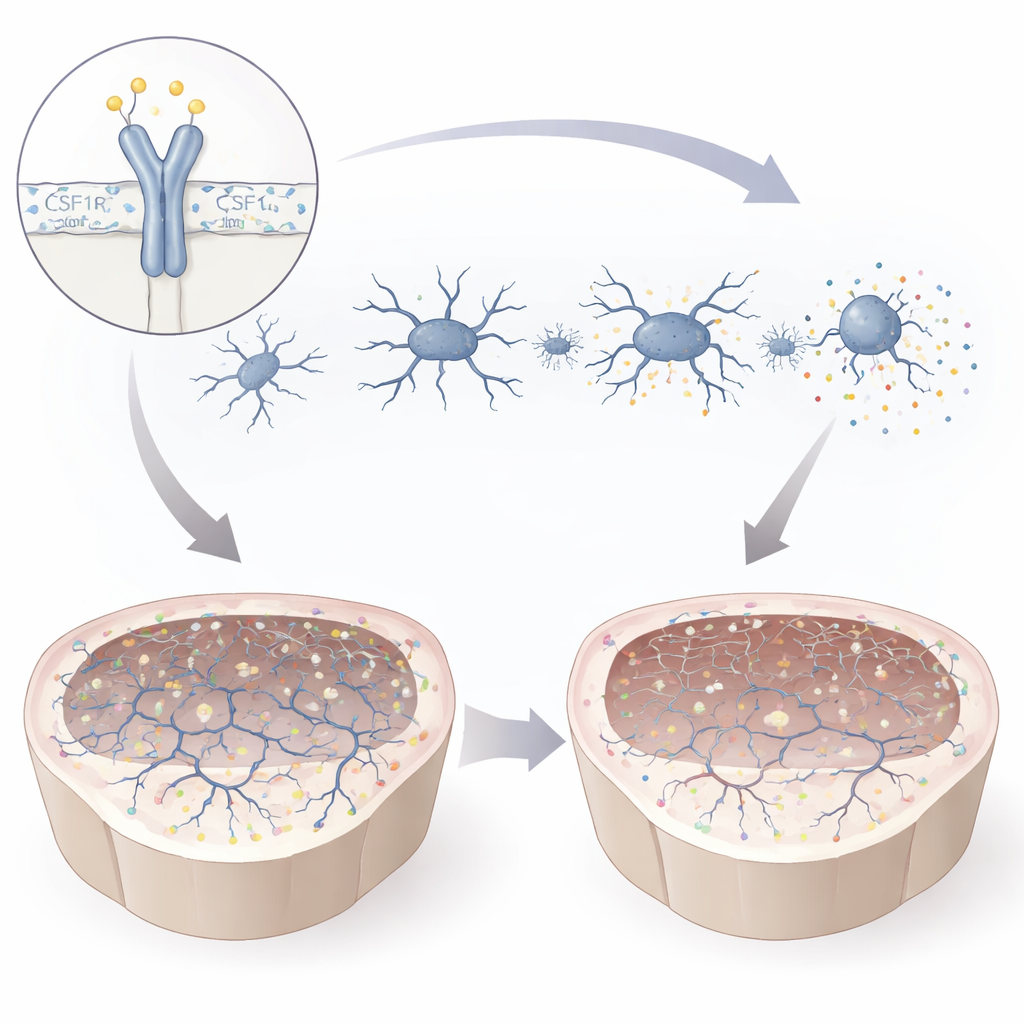
Co to oznacza dla pacjentów i przyszłych terapii
Śledząc skutki mutacji T567M od genu przez komórkę do mini-mózgu, badanie pokazuje, że nawet subtelna zmiana w CSF1R poza jego głównym regionem kontrolnym może destabilizować mikroglej, wytrącać z równowagi rozwój mózgu i osłabiać synapsy, dostarczając wiarygodnego wyjaśnienia dla problemów z pamięcią i ruchami obserwowanych u pacjentów. Praca podkreśla sygnalizację CSF1R jako centralnego strażnika „homeostazy nerwowej” — równowagi, która pozwala komórkom mózgu płynnie się komunikować. Równocześnie modele pacjentów w dwóch i trzech wymiarach stanowią potężne pole do testowania przyszłych terapii, od leków modulujących mikroglej po strategie wymiany komórek, dając nadzieję, że spersonalizowane leczenie zaburzeń związanych z CSF1R może w przyszłości stać się osiągalne.
Cytowanie: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
Słowa kluczowe: zaburzenie związane z CSF1R, mikroglej, organoidy mózgowe, dysfunkcja synaptyczna, neurodegeneracja