Clear Sky Science · it
La mutazione CSF1R T567M induce disfunzione microgliale e compromissione sinaptica in organoidi cerebrali derivati da iPSC di pazienti con disturbo correlato a CSF1R
Quando i custodi del cervello vanno fuori strada
Alcune malattie cerebrali rare colpiscono adulti nel pieno della vita, sottraendo memoria, umore e movimento, mentre le immagini cerebrali rivelano misteriosi danni alla materia bianca — i cablaggi che connettono le aree del cervello. Questo studio indaga uno di questi disturbi legati a un gene chiamato CSF1R, che regola le cellule immunitarie del cervello, note come microglia. Coltivando in laboratorio minuscoli modelli cerebrali ricavati dalle cellule dei pazienti, i ricercatori mostrano come una singola modifica genetica possa destabilizzare questi custodi, alterare lo sviluppo cerebrale e indebolire le connessioni tra i neuroni che sostengono il pensiero e il comportamento.
Una malattia cerebrale rara ma istruttiva
Il disturbo correlato a CSF1R è una condizione ereditaria e progressiva che tipicamente si manifesta in età adulta e provoca declino cognitivo, problemi di movimento e sintomi psichiatrici. È strettamente correlata a una malattia storicamente chiamata ALSP, caratterizzata da danni alla materia bianca cerebrale. Sono state identificate molte varianti del gene CSF1R, la maggior parte delle quali interessa una regione che funziona come l’interruttore principale del gene. Il nuovo lavoro si concentra su una mutazione recentemente scoperta, denominata T567M, che si trova al di fuori di questa classica regione di controllo. Poiché questo sito non era stato prima associato alla malattia, gli scienziati non sapevano se e come potesse causare danni cerebrali così gravi.
Costruire mini-cervelli dalle cellule dei pazienti
Per esplorare la questione, il team ha prelevato cellule del sangue da una persona portatrice della mutazione T567M e le ha riprogrammate in cellule pluripotenti indotte — un tipo cellulare versatile che può essere indotto a diventare molti tessuti. Da queste sono stati creati due set corrispondenti di cellule: uno ha conservato la mutazione del paziente e l’altro è stato “riparato” con precisione tramite strumenti di editing genetico, fungendo da confronto sano. Successivamente hanno cresciuto tre componenti cerebrali chiave: microglia, neuroni e organoidi cerebrali tridimensionali, piccoli modelli semplificati del cervello umano in sviluppo. Questo approccio ha permesso loro di osservare, fianco a fianco, come la mutazione rimodelli le cellule cerebrali e le loro interazioni.
Microglia iperattive e cablaggio cerebrale sotto stress
La mutazione ha indebolito la proteina CSF1R e alterato la sua attivazione chimica in un sito cruciale, lasciando le microglia parzialmente prive del segnale. In coltura, le microglia mutanti sono diventate più piccole e meno ramificate, una morfologia associata a uno stato attivato e stressato. Hanno rilasciato molecole infiammatorie e migrato con difficoltà verso segnali che normalmente le attirerebbero nelle aree danneggiate. Allo stesso tempo, sono risultate più inclini a inglobare materiale circostante, inclusa la mielina e particelle a forma di perla che imitano detriti cellulari. Il profilo di espressione genica ha rivelato uno spostamento lontano dai programmi che supportano la crescita neuronale e le sinapsi, verso vie legate all’attivazione del sistema immunitario. Nel complesso, questi cambiamenti delineano microglia sia iperreattive sia funzionalmente compromesse — mal attrezzate a sostenere circuiti cerebrali sani.
Neuroni bloccati e segnali indeboliti nei mini-cervelli
La mutazione ha anche alterato lo sviluppo degli stessi neuroni. Le cellule precursori precoci si sono divise più del solito, ma poche sono maturate in neuroni completamente sviluppati con rami lunghi e complessi. Negli organoidi cerebrali derivati da cellule mutanti, i marcatori dei neuroni maturi risultavano ridotti e le registrazioni elettriche hanno mostrato che i neuroni erano più piccoli, generavano meno impulsi elettrici e scambiavano segnali più deboli con i vicini. Sia la comunicazione eccitatoria sia quella inibitoria tra le cellule sono calate drasticamente, indicando un declino diffuso della funzione sinaptica. Quando microglia mutanti sono state aggiunte ad organoidi mutanti, i livelli di proteine sinaptiche chiave nelle giunzioni tra neuroni sono diminuiti ulteriormente, mentre microglia sane hanno aumentato le stesse proteine in organoidi normali. Ciò suggerisce che microglia difettose e neuroni vulnerabili agiscono insieme per compromettere la connettività cerebrale.
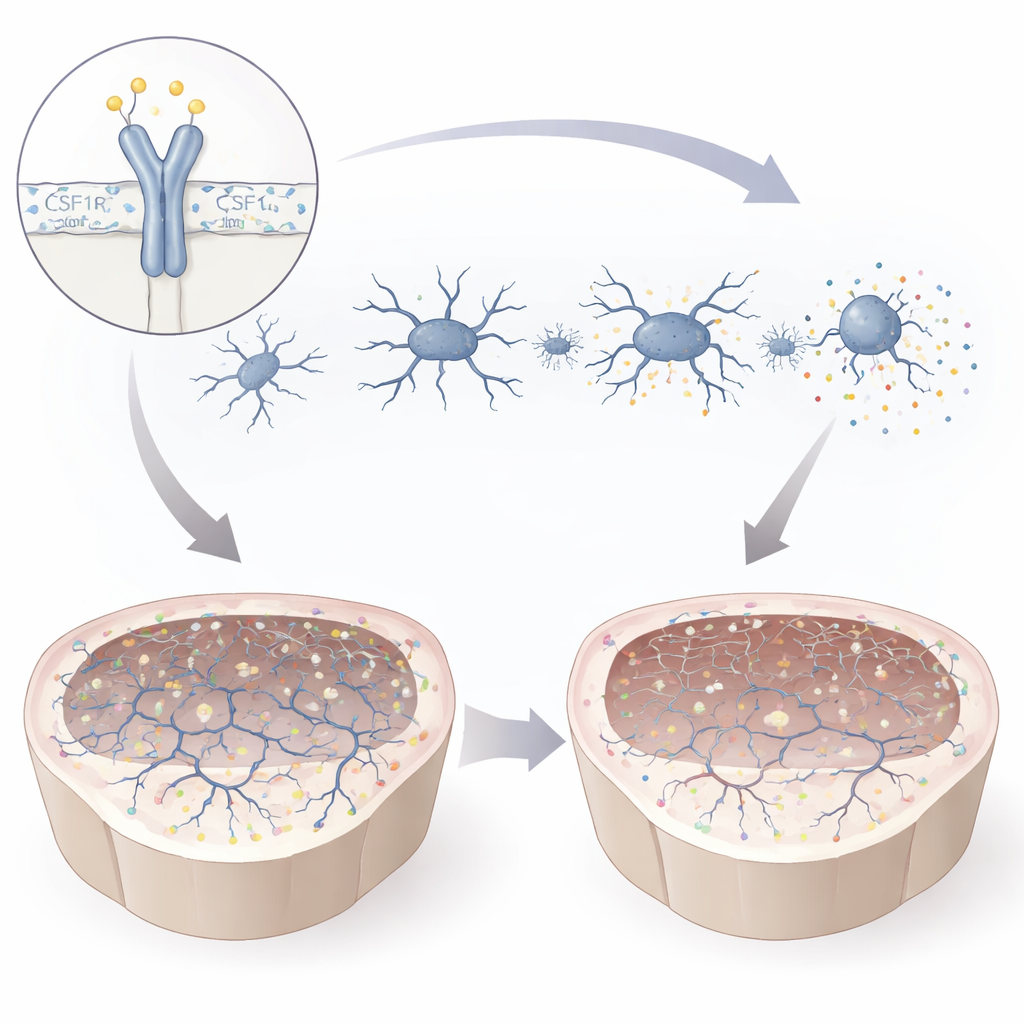
Cosa significa per i pazienti e per i trattamenti futuri
Tracciando gli effetti della mutazione T567M dal gene alla cellula fino al mini-cervello, lo studio dimostra che anche una modifica sottile in CSF1R, al di fuori della sua principale regione di controllo, può destabilizzare le microglia, mandare fuori strada lo sviluppo cerebrale e indebolire le sinapsi, offrendo una spiegazione plausibile per i problemi di memoria e di movimento osservati nei pazienti. Il lavoro evidenzia la segnalazione di CSF1R come guardiano centrale dell’“omeostasi neurale” — l’equilibrio che mantiene una comunicazione fluida tra le cellule cerebrali. Altrettanto importante, i modelli paziente-derivati bidimensionali e tridimensionali forniscono un banco di prova potente per terapie future, dai farmaci che modulano le microglia a strategie di sostituzione cellulare, accrescendo la speranza che trattamenti personalizzati per i disturbi correlati a CSF1R possano un giorno diventare realtà.
Citazione: Chi, L., Tu, H., Li, Z. et al. CSF1R T567M mutation induces microglial dysfunction and synaptic impairment in patient iPSC-derived cerebral organoids of CSF1R-related disorder. Cell Death Discov. 12, 148 (2026). https://doi.org/10.1038/s41420-026-02995-2
Parole chiave: disturbo correlato a CSF1R, microglia, organoidi cerebrali, disfunzione sinaptica, neurodegenerazione