Clear Sky Science · sv
KAT5-medierad acetylering förbättrar OTUB2:s deubikvitinering av HASPIN och främjar bröstcancerns progression
Varför denna cancerberättelse är viktig
Bröstcancer är fortfarande en av de främsta dödsorsakerna för kvinnor globalt, huvudsakligen eftersom aggressiva tumörer sprider sig till avlägsna organ. Denna studie granskar de små molekylära ”vippor” som hjälper bröstcancerceller att växa och ta sig genom kroppen. Genom att avslöja ett nytt sätt som cancerceller håller ett tillväxtdrivande protein vid liv och aktivt, pekar forskarna på nya möjligheter för mer precisa behandlingar som en dag skulle kunna bromsa eller stoppa dödlig spridning.
Ett protein som driver cancerceller framåt
I centrum för arbetet står ett protein kallat HASPIN, en typ av enzym som hjälper celler att dela sig genom att styra hur kromosomer hanteras vid celldelning. Forskarna fann att nivåerna av HASPIN är mycket högre i bröstcancervävnad än i normal bröstvävnad, och att patienter vars tumörer innehåller mer HASPIN tenderar att ha sämre överlevnad. När forskarna sänkte HASPIN i bröstcancercellinjer växte cellerna långsammare, bildade färre kolonier och hade minskad förmåga att röra sig och invadera genom laboratoriemembran. När de ökade HASPIN hände motsatsen: cellerna blev mer aggressiva. Dessa experiment visar att HASPIN beter sig som ett ”onkogen” i bröstcancer—en av de interna motorerna som driver tumörtillväxt och spridning.
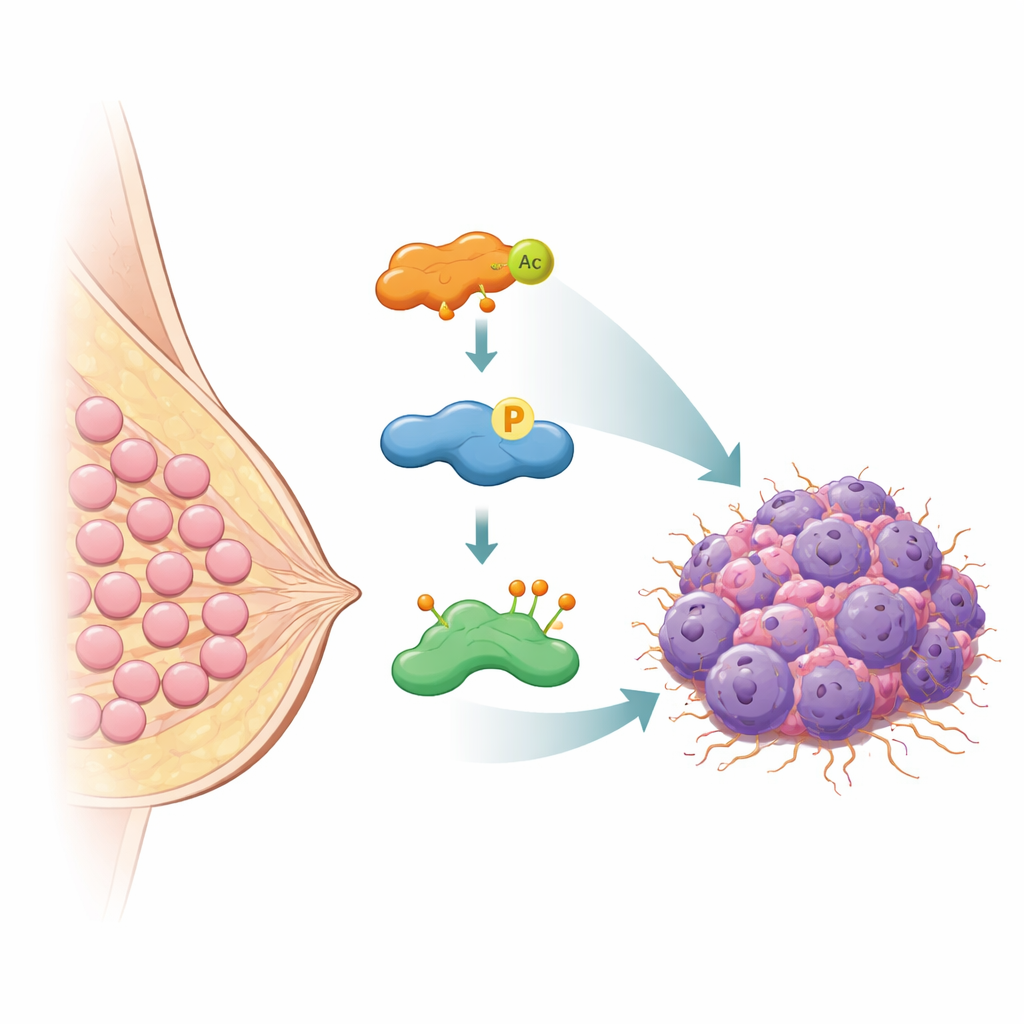
Den molekylära livvakten som räddar HASPIN från förstörelse
Celler förhindrar normalt farlig proteinansamling genom att märka onödiga proteiner för förstörelse med små märken kallade ubiquitin, vilka skickar dem till cellens avfallshanteringsmaskineri. Författarna upptäckte att ett protein kallat OTUB2 fungerar som en molekylär livvakt för HASPIN. OTUB2 tillhör en familj av enzymer som tar bort dessa ubiquitinmärken. Med flera biokemiska metoder visade teamet att OTUB2 binder direkt till HASPIN inne i bröstcancerceller. När OTUB2 avlägsnades blev HASPIN tungt märkt med en särskild form av ubiquitin som signalerar för proteinnedbrytning och dess nivåer föll. När OTUB2 ökades avlägsnades dessa märken, HASPIN skonades från förstörelse och dess nivåer steg. I musemodeller växte tumörer med mer OTUB2 snabbare och spred sig lättare till lungorna, men dessa effekter var beroende av HASPIN, vilket understryker hur nära deras öden är kopplade.
En kemisk justering som förstärker partnerskapet
Berättelsen slutar inte med OTUB2. Forskarna fann att HASPIN också bär en annan vanlig kemisk markering kallad en acetylgrupp på en specifik position. Denna acetylmark tillsätts av ett enzym som heter KAT5, känt för att modifiera proteiner som kontrollerar DNA och genaktivitet. När KAT5 lade till en acetylgrupp på HASPIN vid ett nyckelställe blev HASPIN:s grepp om OTUB2 starkare. Som ett resultat kunde OTUB2 mer effektivt avlägsna degraderingstagen från HASPIN, vilket ytterligare ökade HASPIN:s stabilitet. Att mutera denna enda plats så att acetylering förhindras försvagade interaktionen med OTUB2 och gjorde det möjligt för fler ubiquitinmärken att ackumuleras, vilket fick HASPIN att brytas ner snabbare. I praktiken vrider KAT5 på en ratt som styr hur tätt HASPIN och OTUB2 samarbetar.
Från cellodlingsskålar till patienttumörer
För att koppla dessa fynd till verklig sjukdom granskade teamet bröstcancerprover från patienter. Både HASPIN och OTUB2-proteiner var konsekvent högre i tumörvävnad än i intilliggande normalvävnad. I flera dussin fall tenderade tumörer med mer OTUB2 också att ha mer HASPIN, vilket speglar det molekylära partnerskap som sågs i laboratoriet. Viktigt är att patienter vars tumörer visade höga nivåer av något av proteinerna hade sämre överlevnad över tid. Denna kliniska koppling stöder idén att KAT5–HASPIN–OTUB2-kedjan inte är en laboratorieföreteelse utan en fungerande motor i mänskliga cancerformer som hjälper dem att växa och sprida sig.
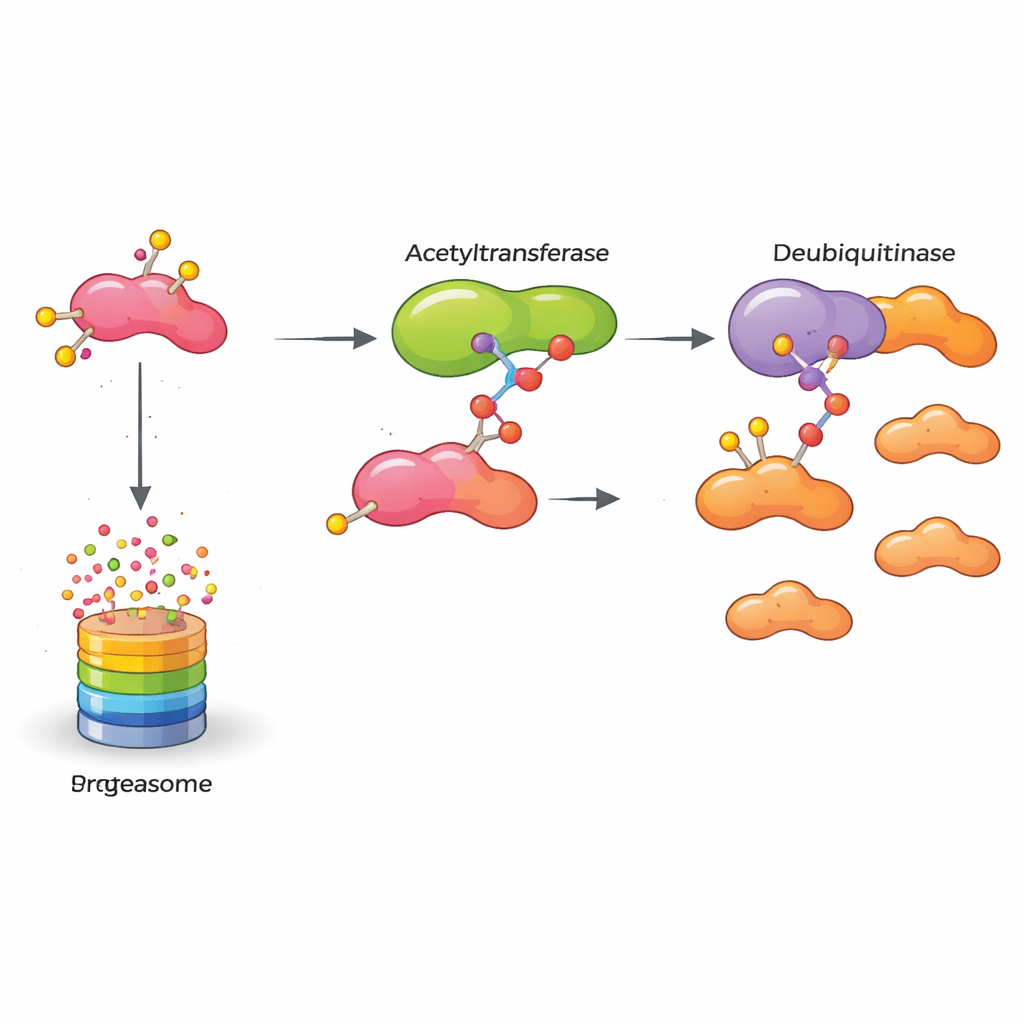
Vad detta betyder för framtida behandlingar
Sammantaget avslöjar studien en molekylär reläkedja som håller ett cancerfrämjande protein aktiverat: KAT5 modifierar HASPIN kemiskt, vilket gör att HASPIN fäster hårdare vid OTUB2, som i sin tur skyddar HASPIN från att förstöras. Detta stabiliserade HASPIN driver bröstcancerceller att föröka sig och invadera. För icke-specialister är huvudpoängen att blockera någon länk i denna kedja—KAT5:s acetylmärke, OTUB2:s skyddande handling eller HASPIN själv—kan försvaga tumörens interna maskineri. Att omvandla dessa insikter till läkemedel kommer att ta tid, men arbetet öppnar nya vägar för terapier utformade för att selektivt avväpna aggressiva bröstcancerformer genom att låta deras egna kvalitetskontrollsystem slutligen ta hand om det molekylära skräpet.
Citering: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
Nyckelord: bröstcancer, HASPIN, OTUB2, proteinnedbrytning, riktad terapi