Clear Sky Science · nl
KAT5-gemedieerde acetylatie bevordert de deubiquitinering van HASPIN door OTUB2 en stimuleert de progressie van borstkanker
Waarom dit kankerverhaal ertoe doet
Borstkanker blijft wereldwijd een van de belangrijkste doodsoorzaken bij vrouwen, grotendeels omdat agressieve tumoren naar verre organen uitzaaien. Deze studie gaat in op de kleine moleculaire "schakelaars" die borstkankercellen helpen groeien en door het lichaam reizen. Door een nieuwe manier te onthullen waarop kankercellen een groei-stimulerend eiwit in leven en actief houden, wijzen de onderzoekers op nieuwe mogelijkheden voor preciezere behandelingen die op termijn de verspreiding van dodelijke ziekte kunnen vertragen of stoppen.
Een eiwit dat kankercellen vooruitduwt
Centrisch in dit werk staat een eiwit genaamd HASPIN, een type enzym dat cellen helpt delen door te sturen hoe chromosomen tijdens celdeling worden behandeld. Het team ontdekte dat HASPIN-niveaus veel hoger zijn in borsttumorweefsel dan in normaal borstweefsel, en dat patiënten van wie de tumoren meer HASPIN bevatten doorgaans een slechtere algemene overleving hebben. Toen de onderzoekers HASPIN in borstkankercellijnen terugschroefden, groeiden de cellen langzamer, vormden ze minder kolonies en waren ze minder in staat te migreren en te invaseren door laboratoriummembranen. Toen ze HASPIN verhoogden, gebeurde het omgekeerde: de cellen werden agressiever. Deze experimenten tonen aan dat HASPIN zich gedraagt als een „oncogen" in borstkanker — een van de interne motoren die tumorgroei en uitzaaiing aandrijven.
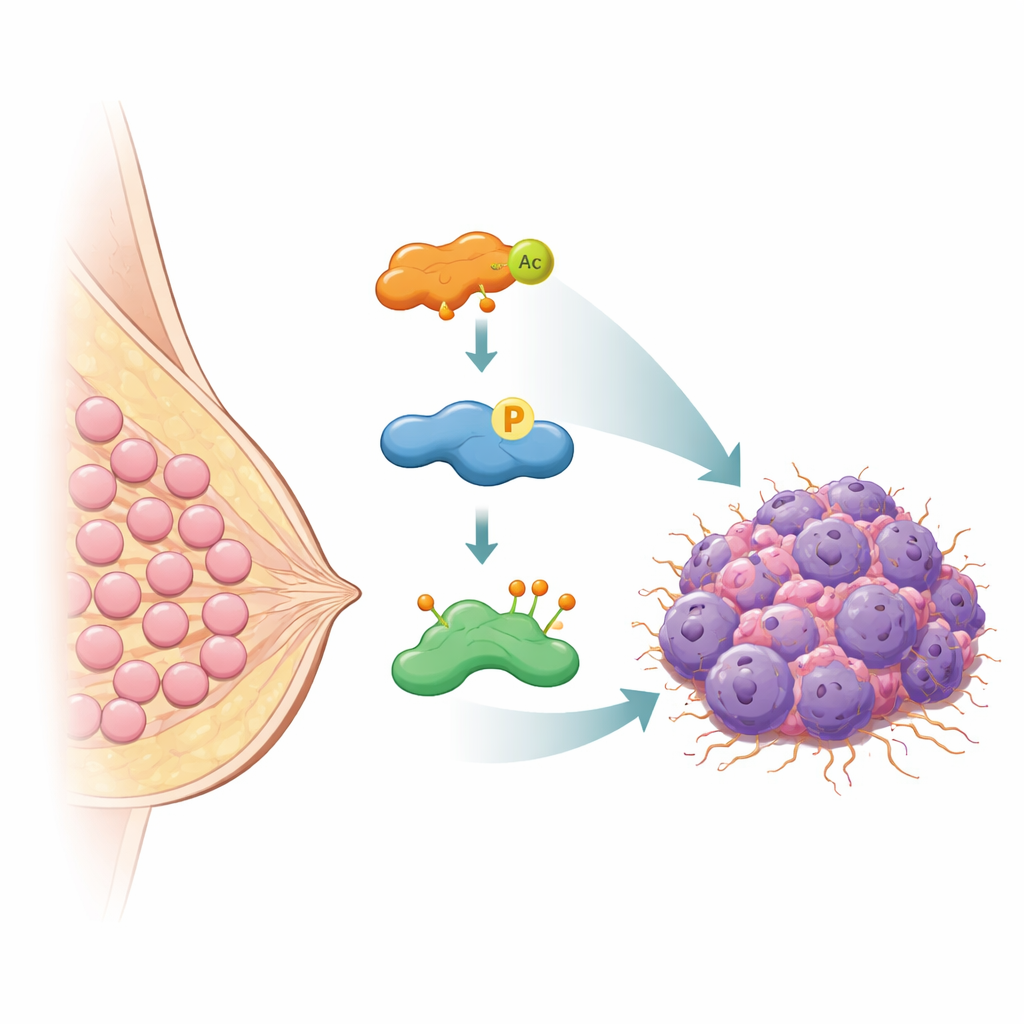
De moleculaire bodyguard die HASPIN van vernietiging redt
Cellen voorkomen normaal gesproken gevaarlijke eiwitophoping door onnodige eiwitten te markeren voor afbraak met kleine labels genaamd ubiquitine, die ze naar de afvalverwerkingsmachinerie van de cel sturen. De auteurs ontdekten dat een eiwit genaamd OTUB2 fungeert als een moleculaire bodyguard voor HASPIN. OTUB2 behoort tot een familie enzymen die deze ubiquitinelabels verwijderen. Met meerdere biochemische methoden toonde het team aan dat OTUB2 direct aan HASPIN bindt binnen borstkankercellen. Wanneer OTUB2 werd verwijderd, werd HASPIN zwaar gemarkeerd met een specifieke vorm van ubiquitine die signaleert voor eiwitafbraak en daalden de niveaus. Wanneer OTUB2 werd verhoogd, werden deze labels verwijderd, bleef HASPIN gespaard van vernietiging en stegen de niveaus. In muismodellen groeiden tumoren met meer OTUB2 sneller en verspreidden ze zich gemakkelijker naar de longen, maar deze effecten waren afhankelijk van HASPIN, wat onderstreept hoe nauw hun lot met elkaar verbonden is.
Een chemische aanpassing die de samenwerking versterkt
Het verhaal eindigt niet bij OTUB2. De onderzoekers ontdekten dat HASPIN ook een andere veelvoorkomende chemische markering draagt, een acetylgroep op een specifieke positie. Deze acetylmarkering wordt toegevoegd door een enzym genaamd KAT5, dat bekendstaat om het modificeren van eiwitten die DNA en genactiviteit reguleren. Wanneer KAT5 een acetylgroep aan HASPIN toevoegt op één sleutelplek, werd HASPINs hechting aan OTUB2 sterker. Daardoor kon OTUB2 effectiever de afbraaketiketten van HASPIN verwijderen en de stabiliteit van HASPIN verder verhogen. Het muteren van deze enkele plaats om acetylatie te voorkomen verzwakte de interactie met OTUB2 en liet meer ubiquitinelabels accumuleren, waardoor HASPIN sneller afgebroken werd. In wezen draait KAT5 aan een knop die regelt hoe stevig HASPIN en OTUB2 samenwerken.
Van celkweekschotels naar patiëntentumoren
Om deze bevindingen aan ziekte in de echte wereld te koppelen, onderzocht het team borsttumormonsters van patiënten. Zowel HASPIN als OTUB2-eiwitten waren consequent hoger in tumorweefsel dan in nabijgelegen normaal weefsel. Over tientallen gevallen hadden tumoren met meer OTUB2 ook vaak meer HASPIN, en spiegelden zo de moleculaire samenwerking die in het laboratorium werd gezien. Belangrijk is dat patiënten van wie de tumoren hoge niveaus van één of beide eiwitten toonden, een slechtere overlevingstijd hadden. Deze klinische link ondersteunt het idee dat de KAT5–HASPIN–OTUB2-keten geen laboratoriumcuriositeit is maar een werkende motor in menselijke kankers die hen helpt groeien en uitzaaien.
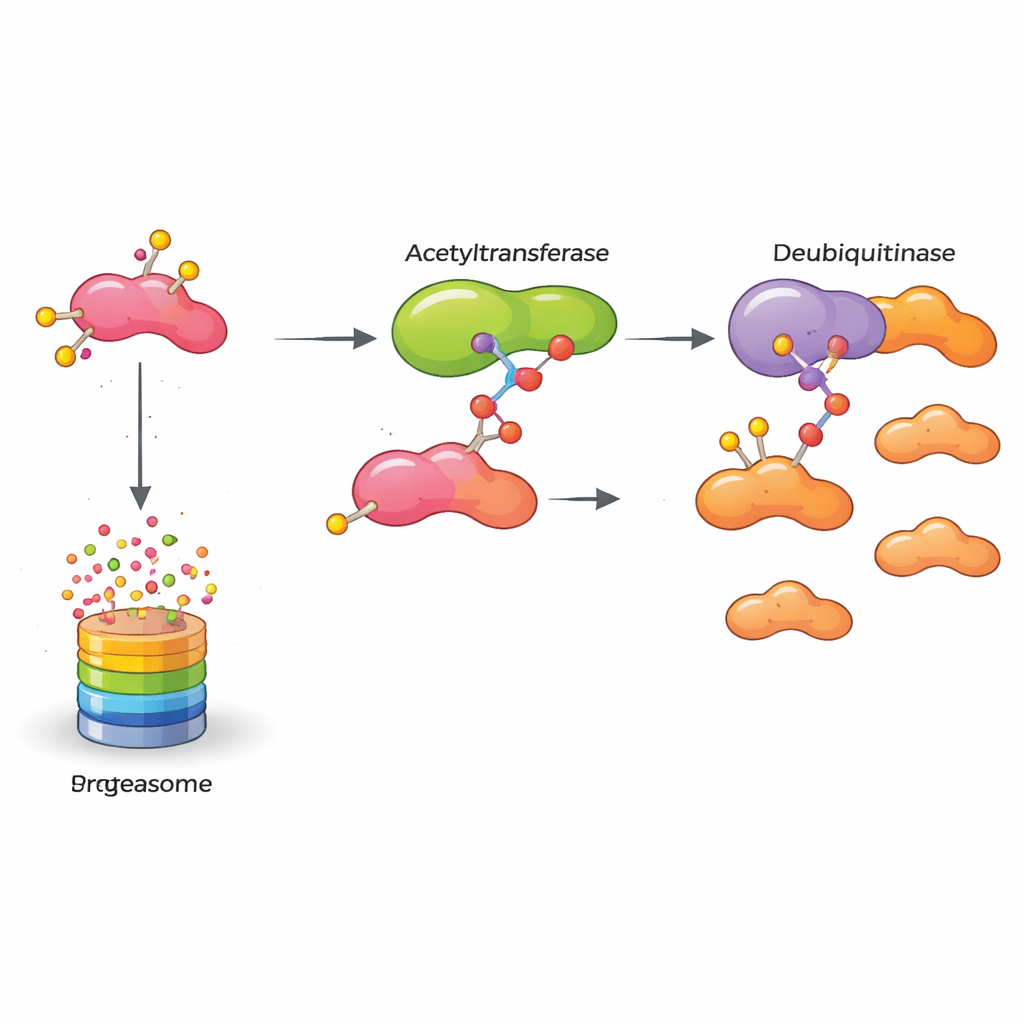
Wat dit betekent voor toekomstige behandelingen
Samengevat onthult de studie een moleculair relais dat een kankerversterkend eiwit ingeschakeld houdt: KAT5 modificeert HASPIN chemisch, waardoor HASPIN steviger aan OTUB2 gaat vastzitten, en OTUB2 op zijn beurt HASPIN beschermt tegen vernietiging. Dit gestabiliseerde HASPIN drijft borstkankercellen tot vermenigvuldiging en invasie. Voor niet-specialisten is de belangrijkste conclusie dat het blokkeren van eender welk schakel in deze keten — KAT5’s acetylmarkering, OTUB2’s beschermende werking, of HASPIN zelf — de interne machinerie van de tumor zou kunnen verzwakken. Hoewel het omzetten van deze inzichten in geneesmiddelen tijd zal vergen, opent het werk nieuwe wegen naar therapieën die ontworpen zijn om agressieve borstkankers selectief uit te schakelen door hun eigen kwaliteitscontrolesystemen eindelijk het moleculaire afval te laten opruimen.
Bronvermelding: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
Trefwoorden: borstkanker, HASPIN, OTUB2, proteïne-afbraak, gerichte therapie