Clear Sky Science · he
אצטילציית KAT5 משפרת את דה‑אוביקוויטינציה של HASPIN על‑ידי OTUB2 ומקדמת התקדמות של סרטן השד
מדוע הסיפור הזה על סרטן חשוב
סרטן השד נותר סיבה מובילה לתמותה בקרב נשים ברחבי העולם, בעיקר משום שתאים סרטניים אגרסיביים נוטים להתפשט לאיברים מרוחקים. מחקר זה בוחן את ה"מפסקיים" המולקולאריים הקטנים שמסייעים לתאי סרטן השד לגדול ולהיסע בגוף. על ידי גילוי מנגנון חדש שבו תאים סרטניים שומרים על חלבון ממריץ גדילה חי ופעיל, החוקרים מצביעים על הזדמנויות חדשות לטיפולים מדויקים יותר שעשויים יום אחד להאט או לעצור את התפשטות המחלה המסכנת חיים.
חלבון שמניע את התקדמות התאים הסרטניים
במרכזה של העבודה נמצא חלבון בשם HASPIN, סוג של אנזים המסייע לתאי להתחלק על‑ידי הנחייה בטיפול בכרומוזומים במהלך החלוקה. הצוות מצא שרמות HASPIN גבוהות הרבה יותר ברקמות סרטן השד בהשוואה לרקמה שדית נורמלית, ושחולים שלגידוליהם יש רמות גבוהות של HASPIN נוטים לתמותה כוללת גרועה יותר. כאשר החוקרים הורידו את ביטוי HASPIN בקווי תאים של סרטן השד, התאים גדלו לאט יותר, יצרו פחות מושבות והיו פחות מסוגלים לנוע ולחדור דרך ממברנות במבחנה. כאשר הגבירו את HASPIN, נצפו ההשפעות ההפוכות: התאים הפכו לאגרסיביים יותר. ניסויים אלה מראים ש‑HASPIN מתנהג כ"אונקגֵן" בסרטן השד—אחד ממנועי הפנימי שמזינים את גדילת הגידול והתפשטותו.
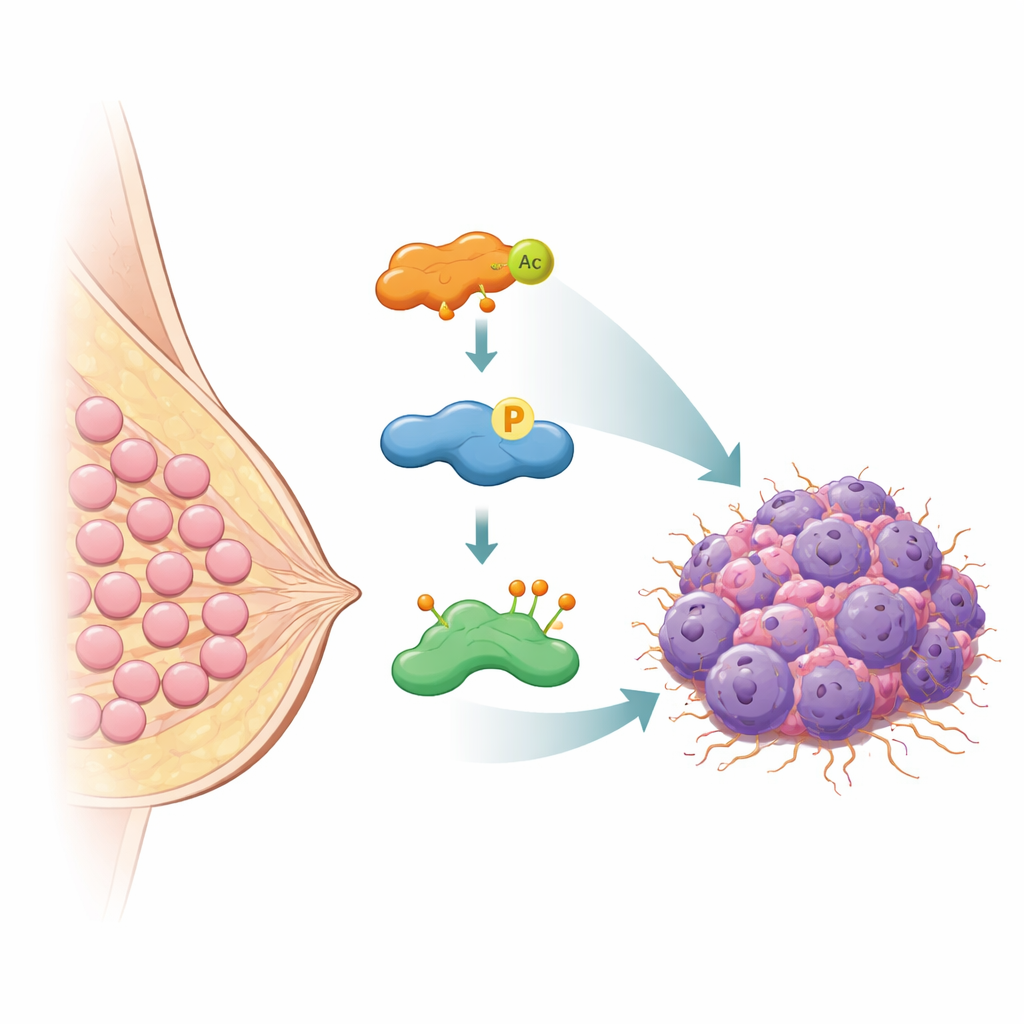
המאבטח המולקולרי ששומר על HASPIN מפירוק
תאים בדרך כלל מונעים הצטברות מסוכנת של חלבונים על‑ידי סימון חלבונים מיותרים להשמדה בתגיות קטנות הנקראות יוביקוויטין, ששולחות אותם למכונת הסילוק של התא. המחברים גילו שחלבון בשם OTUB2 פועל כמאבטח מולקולרי עבור HASPIN. OTUB2 שייך למשפחה של אנזימים שמסירים תגיות יוביקוויטין אלה. באמצעות שיטות ביוכימיות שונות הראו החוקרים ש‑OTUB2 נקשר ישירות ל‑HASPIN בתוך תאי סרטן השד. כאשר הוסר OTUB2, HASPIN נצבר עם סוג מסוים של יוביקוויטין שמסמן פירוק, ורמותיו ירדו. כאשר הגבירו את OTUB2, תגיות אלה הוסרו, HASPIN ניצל מהשמדה ורמותיו עלו. במודלים בחולדות, גידולים עם רמות גבוהות יותר של OTUB2 גדלו מהר יותר והתפשטו ביתר קלות אל הריאות, אך אפקטים אלה היו תלויים ב‑HASPIN, מה שמדגיש עד כמה גורלותיהם מקושרים.
תיקון כימי שמחזק את השותפות
הסיפור אינו מסתיים ב‑OTUB2. החוקרים מצאו שגם ל‑HASPIN יש סימן כימי נפוץ נוסף הנקרא קבוצת אצטיל במיקום ספציפי. סימון זה נוסף על‑ידי אנזים בשם KAT5, הידוע במודיפיקציה של חלבונים השולטים על DNA ופעילות גנים. כאשר KAT5 הוסיף קבוצת אצטיל ל‑HASPIN בנקודה מרכזית אחת, הקשר של HASPIN ל‑OTUB2 התחזק. כתוצאה מכך, OTUB2 יכול היה להסיר ביתר יעילות את תגי הפירוק מ‑HASPIN, מה שהגביר עוד יותר את יציבותו של HASPIN. מוטציה באתר יחיד זה שמנעה אצטילציה החלישה את האינטראקציה עם OTUB2 ואפשרה הצטברות של תגי יוביקוויטין, מה שגרם ל־HASPIN להתפרק מהר יותר. במילים אחרות, KAT5 מכוונן את עוצמת שיתוף הפעולה בין HASPIN ל‑OTUB2.
מצלחות תרבית תאים עד לדגימות מטופלים
כדי לקשר ממצאים אלה למחלה במציאות, הצוות בחן דגימות סרטן שד של מטופלים. גם HASPIN וגם OTUB2 היו גבוהים בעקביות ברקמת הגידול בהשוואה לרקמה הסמוכה הנורמלית. בעשרות מקרים, גידולים עם רמות גבוהות יותר של OTUB2 נטו גם הם להכיל רמות גבוהות של HASPIN, מה שמשקף את השותפות המולקולרית שנצפתה במעבדה. חשוב מכך, מטופלים שלגידוליהם היו רמות גבוהות של אחד מהחלבונים הללו הראו הישרדות גרועה יותר לאורך זמן. הקשר הקליני הזה תומך ברעיון ששרשרת KAT5–HASPIN–OTUB2 אינה מוקדמת ניסויית בלבד אלא מנוע עובד בתוך סרטן אנושי המסייע לו לגדול ולהתפשט.
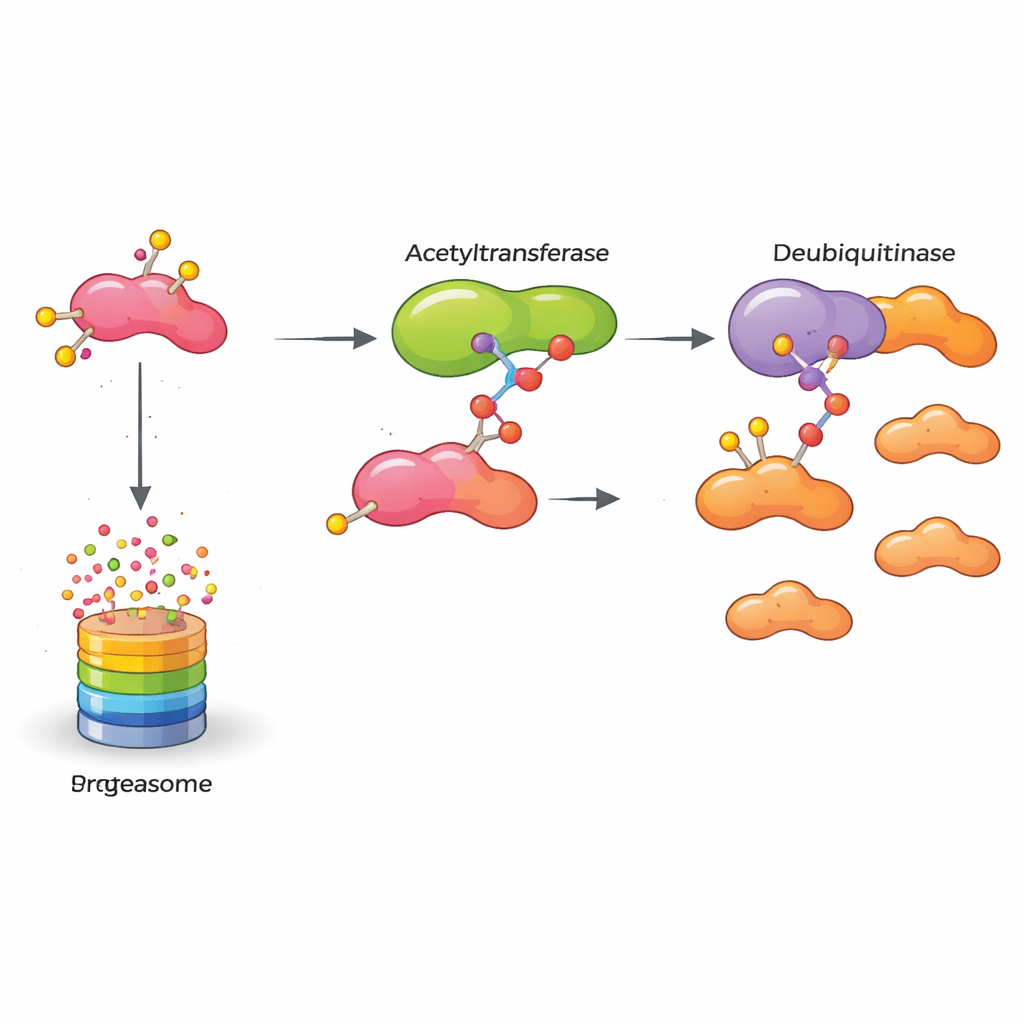
מה משמעות הדבר עבור טיפולים עתידיים
סיכום הממצאים חושף מרתון מולקולרי שמשאיר חלבון המקדם סרטן במצב פעיל: KAT5 משנה כימית את HASPIN, שזו מתהדקת יותר ל‑OTUB2, וזה בתורו מגן על HASPIN מפירוק. HASPIN המיצב מקדם שכפול והתפשטות של תאי סרטן השד. עבור קהל לא מקצועי, המסקנה המרכזית היא ששיבוש כל קישור בשרשרת הזו—אותו סימון אצטיל של KAT5, פעולה המגוננת של OTUB2 או HASPIN עצמו—יכול להחליש את המכונה הפנימית של הגידול. פיתוח תרופות המבוסס על תובנות אלה ידרוש זמן, אך העבודה פותחת דרכים חדשות לטיפולים שמטרתם לנטרל באופן סלקטיבי סרטןי שד אגרסיביים על‑ידי מתן לְּמערכות בקרת האיכות של התא לבצע סוף‑סוף את עבודת הסילוק המולקולרית.
ציטוט: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
מילות מפתח: סרטן השד, HASPIN, OTUB2, degradation חלבונים, טיפול ממוקד