Clear Sky Science · ar
تعديل الأسيتيل بواسطة KAT5 يعزز نزع اليوبكويتين عن HASPIN بواسطة OTUB2 ويُسرِّع تقدم سرطان الثدي
لماذا تهم هذه القصة السرطانية
لا يزال سرطان الثدي سببًا رئيسيًا لوفيات النساء حول العالم، ويرجع جزء كبير من ذلك إلى أن الأورام العدوانية تنتشر إلى أعضاء بعيدة. تتعمق هذه الدراسة في "المفاتيح" الجزيئية الصغيرة التي تساعد خلايا سرطان الثدي على النمو والتنقل داخل الجسم. من خلال كشف طريقة جديدة تحافظ بها الخلايا السرطانية على بقاء بروتين يدفع النمو نشطًا، يشير الباحثون إلى فرص جديدة لعلاجات أكثر دقة قد تبطئ أو توقف في يوم من الأيام انتشار المرض المميت.
بروتين يدفع الخلايا السرطانية إلى الأمام
في مركز هذا العمل يوجد بروتين يدعى HASPIN، وهو نوع من الإنزيمات التي تساعد الخلايا على الانقسام عبر توجيه كيفية التعامل مع الكروموسومات أثناء الانقسام الخلوي. وجد الفريق أن مستويات HASPIN أعلى بكثير في أنسجة سرطان الثدي مقارنة بالأنسجة الثديية الطبيعية، وأن المرضى الذين تحتوي أورامهم على مزيد من HASPIN يميلون إلى قلة البقاء الكلي. عندما قلل الباحثون من مستوى HASPIN في سلالات خلايا سرطان الثدي، نمت الخلايا ببطء أكبر، شكلت مستعمرات أقل، وكانت أقل قدرة على الحركة والغزو عبر أغشية مخبرية. وعندما زادوا HASPIN، حدث العكس: أصبحت الخلايا أكثر عدوانية. تُظهر هذه التجارب أن HASPIN يتصرف كـ"جين مُسبب للسرطان" في سرطان الثدي—أحد المحركات الداخلية التي تغذي نمو الورم وانتشاره.
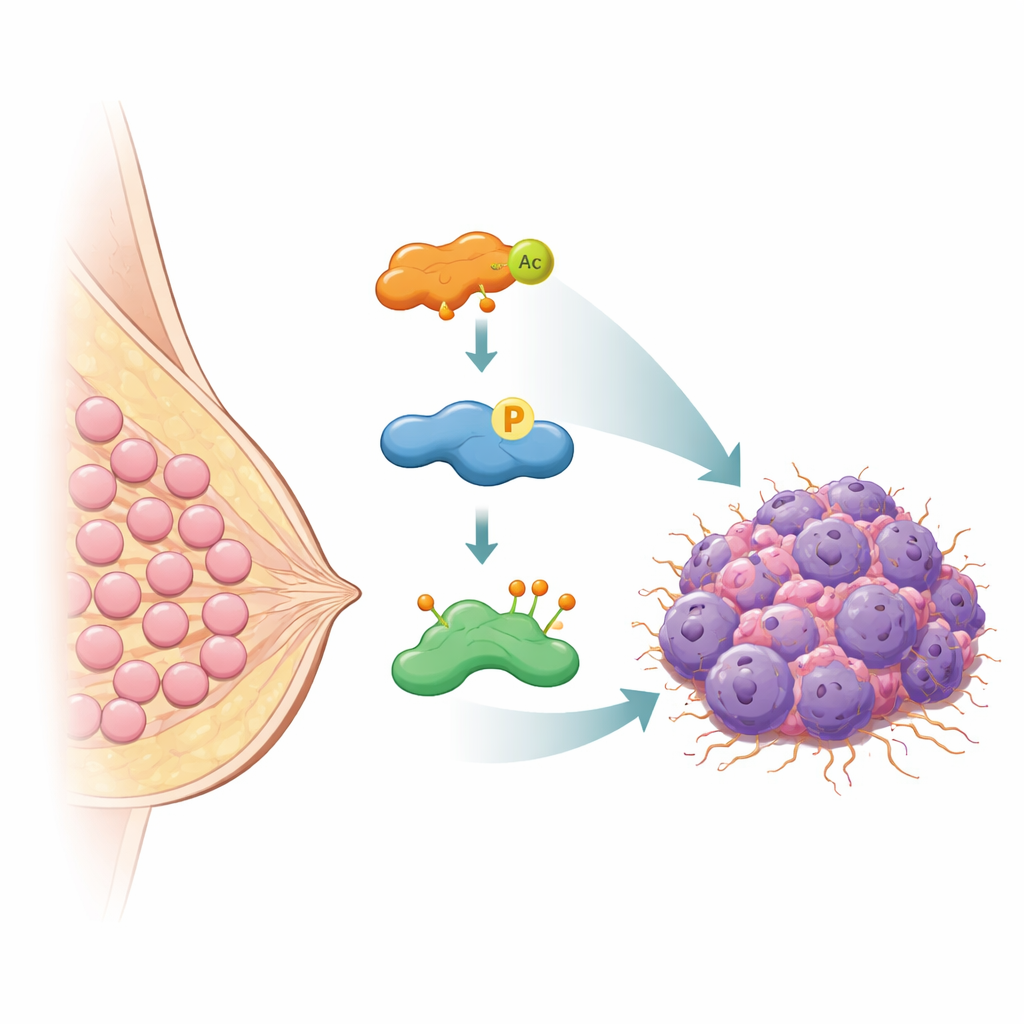
الحرَّاس الجزيئي الذي ينقذ HASPIN من التحلل
تمنع الخلايا عادة تراكم البروتينات الضارة عن طريق وسم البروتينات غير المطلوبة بعلامات صغيرة تسمى اليوبكويتين، التي توجهها إلى آليات التخلص داخل الخلية. اكتشف المؤلفون أن بروتينًا يدعى OTUB2 يعمل كحارس جزيئي لـ HASPIN. ينتمي OTUB2 إلى عائلة من الإنزيمات التي تزيل هذه علامات اليوبكويتين. باستخدام طرق بيوكيميائية متعددة، أظهر الفريق أن OTUB2 يرتبط مباشرة بـ HASPIN داخل خلايا سرطان الثدي. عندما أزيل OTUB2، أصبح HASPIN مُعلّمًا بكثرة بشكل خاص بنوعية من اليوبكويتين التي تشير إلى التحلل وانخفضت مستوياته. وعندما زاد OTUB2، أُزيِلت هذه العلامات، نجَا HASPIN من التحلل، وارتفعت مستوياته. في نماذج الفئران، نمت الأورام التي تحتوي على مزيد من OTUB2 بسرعة أكبر وانتشرت إلى الرئتين بسهولة أكبر، لكن هذه التأثيرات اعتمدت على HASPIN، مما يؤكد مدى ارتباط مصيرهما.
تعديل كيميائي يشد الشراكة
لا تنتهي القصة عند OTUB2. وجد الباحثون أن HASPIN يحمل أيضًا علامة كيميائية شائعة أخرى تُسمى مجموعة أسيتيل في موقع محدد. تُضاف هذه العلامة الأسيتيلية بواسطة إنزيم يُدعى KAT5، المعروف بتعديل البروتينات التي تتحكم في الحمض النووي ونشاط الجينات. عندما أضاف KAT5 مجموعة أسيتيل إلى HASPIN في موقع رئيسي واحد، أصبح ارتباط HASPIN بـ OTUB2 أقوى. ونتيجة لذلك، تمكن OTUB2 من إزالة علامات التحلل من HASPIN بشكل أكثر فعالية، مما زاد من استقرار HASPIN بشكل أكبر. أدى تحوير هذا الموقع المفرد لمنع الأسيتلة إلى إضعاف التفاعل مع OTUB2 وسمح بتراكم مزيد من علامات اليوبكويتين، مما تسبب في تحلل HASPIN بشكل أسرع. باختصار، يعمل KAT5 كمقبض يتحكم في مدى تشابك عمل HASPIN وOTUB2.
من أطباق الزراعة الخلوية إلى أورام المرضى
لربط هذه النتائج بالمرض في العالم الحقيقي، فحص الفريق نماذج من سرطانات الثدي لدى المرضى. كان كل من بروتيني HASPIN وOTUB2 أعلى باستمرار في نسيج الورم مقارنة بالنسيج الطبيعي المجاور. عبر عشرات الحالات، كانت الأورام التي تحتوي على مزيد من OTUB2 تميل أيضًا إلى احتواء مزيد من HASPIN، مما يعكس الشراكة الجزيئية المرصودة في المختبر. والأهم من ذلك، أن المرضى الذين أظهرت أورامهم مستويات مرتفعة لأي من البروتينين كان لديهم بقاء أسوأ مع مرور الوقت. يدعم هذا الارتباط السريري فكرة أن سلسلة KAT5–HASPIN–OTUB2 ليست مجرد ملاحظة مخبرية بل محرك فعّال داخل السرطانات البشرية يساعدها على النمو والانتشار.
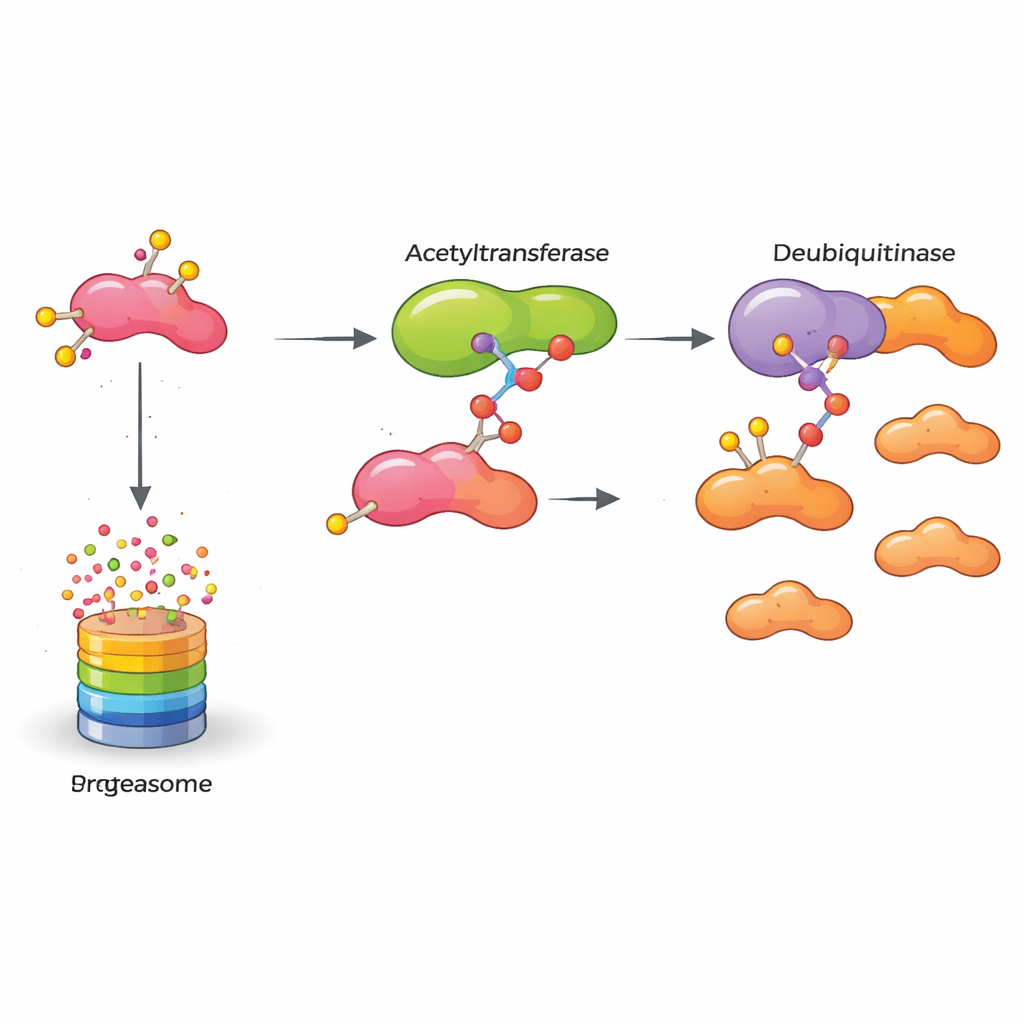
ما يعنيه هذا للعلاجات المستقبلية
عند جمع النتائج معًا، تكشف الدراسة عن تتابع جزيئي يحافظ على بقاء بروتين مشجّع للسرطان مُشغلاً: يُعدّل KAT5 كيميائيًا HASPIN، فيلتصق الأخير بشكل أقوى بـ OTUB2، الذي بدوره يحمي HASPIN من التحلل. يقود HASPIN المُستقر هذا خلايا سرطان الثدي إلى التكاثر والغزو. للقراء غير المتخصصين، الخلاصة الأساسية هي أن إيقاف أي حلقة في هذه السلسلة—علامة الأسيتيل التي يضعها KAT5، فعلية الحماية لـ OTUB2، أو HASPIN نفسه—يمكن أن يضعف الآلية الداخلية للورم. وعلى الرغم من أن تحويل هذه الرؤى إلى أدوية سيستغرق وقتًا، فإن العمل يفتح مسارات جديدة لعلاجات مصممة لتعطيل السرطانات الثديية العدوانية بشكل انتقائي بواسطة السماح لأنظمة الرقابة الجودة الخاصة بها بالتخلص من النفايات الجزيئية.
الاستشهاد: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
الكلمات المفتاحية: سرطان الثدي, HASPIN, OTUB2, تحلل البروتين, العلاج المستهدف