Clear Sky Science · fr
L’acétylation médiée par KAT5 améliore la désubiquitination de HASPIN par OTUB2 et favorise la progression du cancer du sein
Pourquoi cette histoire de cancer importe
Le cancer du sein reste une cause majeure de mortalité chez les femmes dans le monde, en grande partie parce que les tumeurs agressives se propagent vers des organes distants. Cette étude explore les petits « interrupteurs » moléculaires qui aident les cellules du cancer du sein à croître et à migrer dans l’organisme. En mettant au jour un nouveau mécanisme par lequel les cellules cancéreuses maintiennent en vie et actives des protéines qui stimulent la croissance, les chercheurs ouvrent des opportunités pour des traitements plus précis susceptibles, un jour, de ralentir ou d’empêcher la dissémination mortelle de la maladie.
Une protéine qui pousse les cellules cancéreuses en avant
Au cœur de ce travail se trouve une protéine appelée HASPIN, un type d’enzyme qui aide les cellules à se diviser en guidant la façon dont les chromosomes sont manipulés pendant la division cellulaire. L’équipe a constaté que les niveaux de HASPIN sont bien plus élevés dans les tissus du cancer du sein que dans le tissu mammaire normal, et que les patientes dont les tumeurs contiennent davantage de HASPIN ont tendance à avoir une survie globale plus mauvaise. Lorsque les chercheurs ont réduit l’expression de HASPIN dans des lignées cellulaires du cancer du sein, les cellules ont proliferé plus lentement, formé moins de colonies et montré une capacité réduite de migration et d’invasion à travers des membranes en laboratoire. À l’inverse, lorsqu’ils ont augmenté HASPIN, les cellules sont devenues plus agressives. Ces expériences montrent que HASPIN se comporte comme un « oncogène » dans le cancer du sein — l’un des moteurs internes qui alimentent la croissance et la dissémination tumorales.
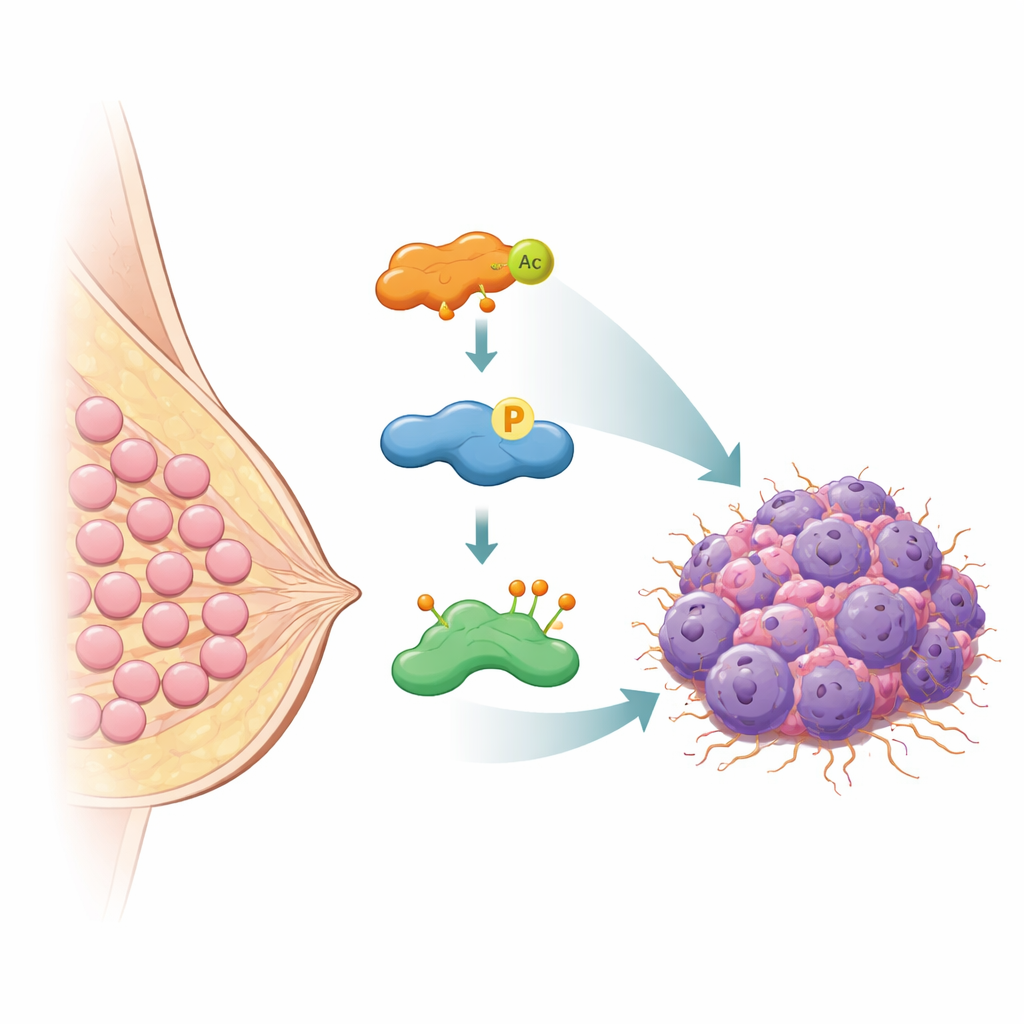
Le garde du corps moléculaire qui sauve HASPIN de la destruction
Les cellules empêchent normalement l’accumulation dangereuse de protéines en étiquetant les protéines inutiles pour destruction avec de petites balises appelées ubiquitines, qui les dirigent vers la machinerie d’élimination cellulaire. Les auteurs ont découvert qu’une protéine nommée OTUB2 agit comme un garde du corps moléculaire pour HASPIN. OTUB2 appartient à une famille d’enzymes qui retirent ces marques ubiquitine. À l’aide de multiples méthodes biochimiques, l’équipe a montré que OTUB2 se lie directement à HASPIN à l’intérieur des cellules du cancer du sein. Lorsque OTUB2 était supprimé, HASPIN était fortement marqué par une forme particulière d’ubiquitine signalant la dégradation et ses niveaux chutaient. Lorsque OTUB2 était augmenté, ces marques étaient éliminées, HASPIN était épargné de la destruction et ses niveaux augmentaient. Chez la souris, les tumeurs contenant davantage d’OTUB2 croissaient plus vite et se dispersaient plus facilement vers les poumons, mais ces effets dépendaient de HASPIN, soulignant à quel point leurs destins sont liés.
Une modification chimique qui resserre le partenariat
L’histoire ne s’arrête pas à OTUB2. Les chercheurs ont trouvé que HASPIN porte aussi une autre marque chimique courante, un groupe acétyle, en un site spécifique. Cette marque d’acétylation est ajoutée par une enzyme nommée KAT5, connue pour modifier des protéines qui contrôlent l’ADN et l’activité des gènes. Lorsque KAT5 ajoutait un groupe acétyle à HASPIN à un site clé, l’affinité de HASPIN pour OTUB2 augmentait. En conséquence, OTUB2 pouvait retirer plus efficacement les balises de dégradation de HASPIN, renforçant ainsi la stabilité de HASPIN. La mutation de ce seul site pour empêcher l’acétylation affaiblissait l’interaction avec OTUB2 et permettait l’accumulation de davantage d’ubiquitines, entraînant une dégradation plus rapide de HASPIN. En substance, KAT5 agit comme un cadran qui contrôle la fermeté de la coopération entre HASPIN et OTUB2.
Des cultures cellulaires aux tumeurs de patientes
Pour relier ces résultats à la maladie humaine, l’équipe a examiné des échantillons de cancer du sein issus de patientes. Les protéines HASPIN et OTUB2 étaient systématiquement plus élevées dans les tissus tumoraux que dans le tissu normal adjacent. Sur des dizaines de cas, les tumeurs présentant davantage d’OTUB2 avaient aussi tendance à contenir plus de HASPIN, reflétant le partenariat moléculaire observé en laboratoire. De manière importante, les patientes dont les tumeurs montraient des niveaux élevés de l’une ou l’autre protéine présentaient une survie plus mauvaise au fil du temps. Ce lien clinique soutient l’idée que la chaîne KAT5–HASPIN–OTUB2 n’est pas une curiosité de laboratoire mais un moteur opérationnel au sein des cancers humains qui favorise leur croissance et leur propagation.
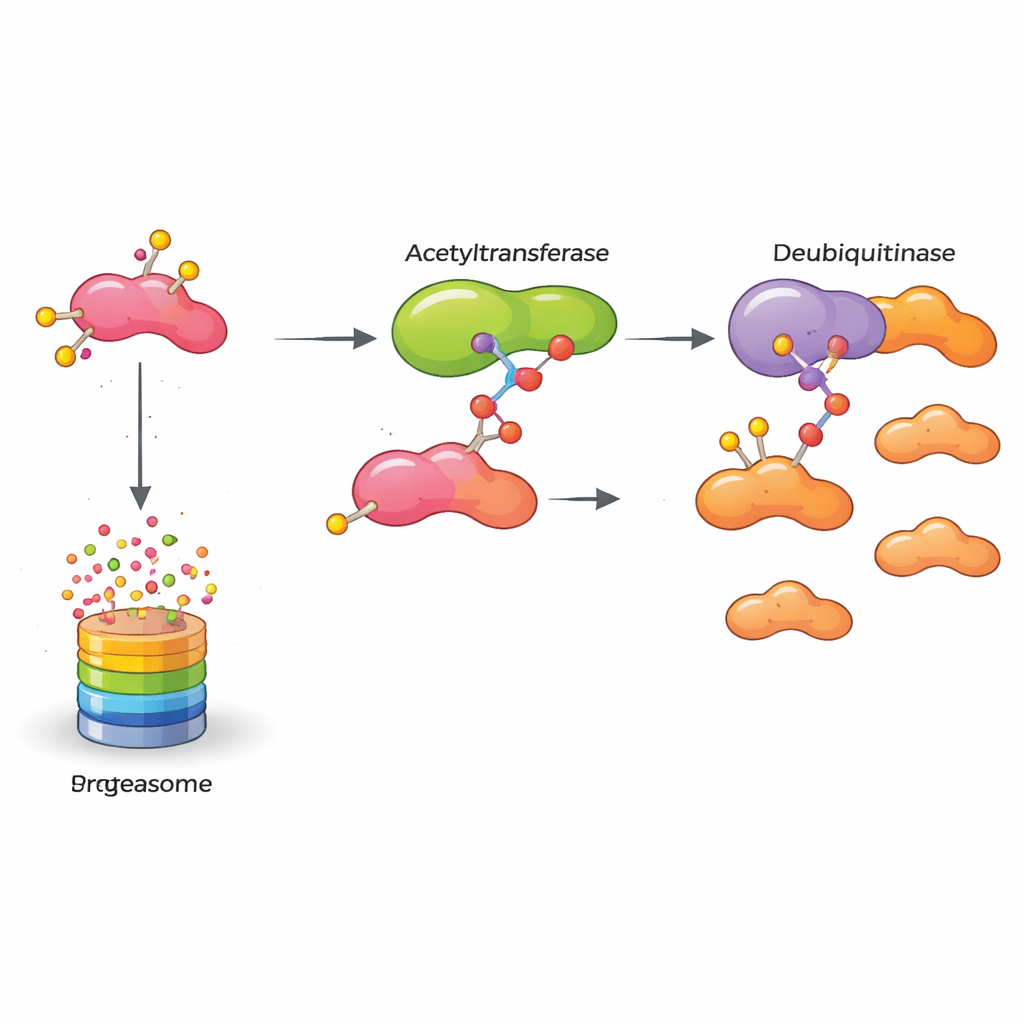
Ce que cela signifie pour les traitements futurs
En synthèse, l’étude révèle une chaîne moléculaire qui maintient une protéine promotrice de cancer activée : KAT5 modifie chimiquement HASPIN, ce dernier se lie plus fortement à OTUB2, qui à son tour protège HASPIN de la destruction. Ce HASPIN stabilisé pousse les cellules du cancer du sein à se multiplier et à envahir. Pour un public non spécialiste, le point clé est que bloquer n’importe quel maillon de cette chaîne — la marque d’acétylation de KAT5, l’action protectrice d’OTUB2 ou HASPIN lui‑même — pourrait affaiblir la machinerie interne de la tumeur. Transformer ces découvertes en médicaments prendra du temps, mais ce travail ouvre de nouvelles pistes pour des thérapies visant à neutraliser sélectivement les cancers du sein agressifs en permettant aux systèmes de contrôle qualité cellulaires d’éliminer finalement ces éléments moléculaires nuisibles.
Citation: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
Mots-clés: cancer du sein, HASPIN, OTUB2, dégradation des protéines, thérapie ciblée