Clear Sky Science · it
L’acetilazione mediata da KAT5 potenzia la deubiquitinazione di HASPIN da parte di OTUB2 e favorisce la progressione del cancro al seno
Perché questa storia sul cancro è importante
Il cancro al seno resta una delle principali cause di morte tra le donne a livello mondiale, in gran parte perché i tumori aggressivi si diffondono a organi distanti. Questo studio indaga i minuscoli “interruttori” molecolari che aiutano le cellule del seno tumorali a crescere e a migrare nell’organismo. Svelando un nuovo meccanismo con cui le cellule cancerose mantengono in vita e attivo un proteina che promuove la crescita, i ricercatori indicano nuove opportunità per terapie più precise che un giorno potrebbero rallentare o arrestare la diffusione letale della malattia.
Una proteina che spinge le cellule tumorali avanti
Al centro di questo lavoro c’è una proteina chiamata HASPIN, un tipo di enzima che aiuta le cellule a dividersi guidando il comportamento dei cromosomi durante la divisione cellulare. Il gruppo ha scoperto che i livelli di HASPIN sono molto più alti nel tessuto di cancro al seno rispetto al tessuto mammario normale, e che i pazienti i cui tumori contengono più HASPIN tendono ad avere una sopravvivenza complessiva peggiore. Quando i ricercatori hanno ridotto l’espressione di HASPIN in linee cellulari di cancro al seno, le cellule crescevano più lentamente, formavano meno colonie e avevano minore capacità di muoversi e invadere membrane in laboratorio. Quando hanno aumentato HASPIN, è successo l’opposto: le cellule sono diventate più aggressive. Questi esperimenti mostrano che HASPIN si comporta come un “oncogene” nel cancro al seno — uno dei motori interni che alimentano la crescita e la diffusione del tumore.
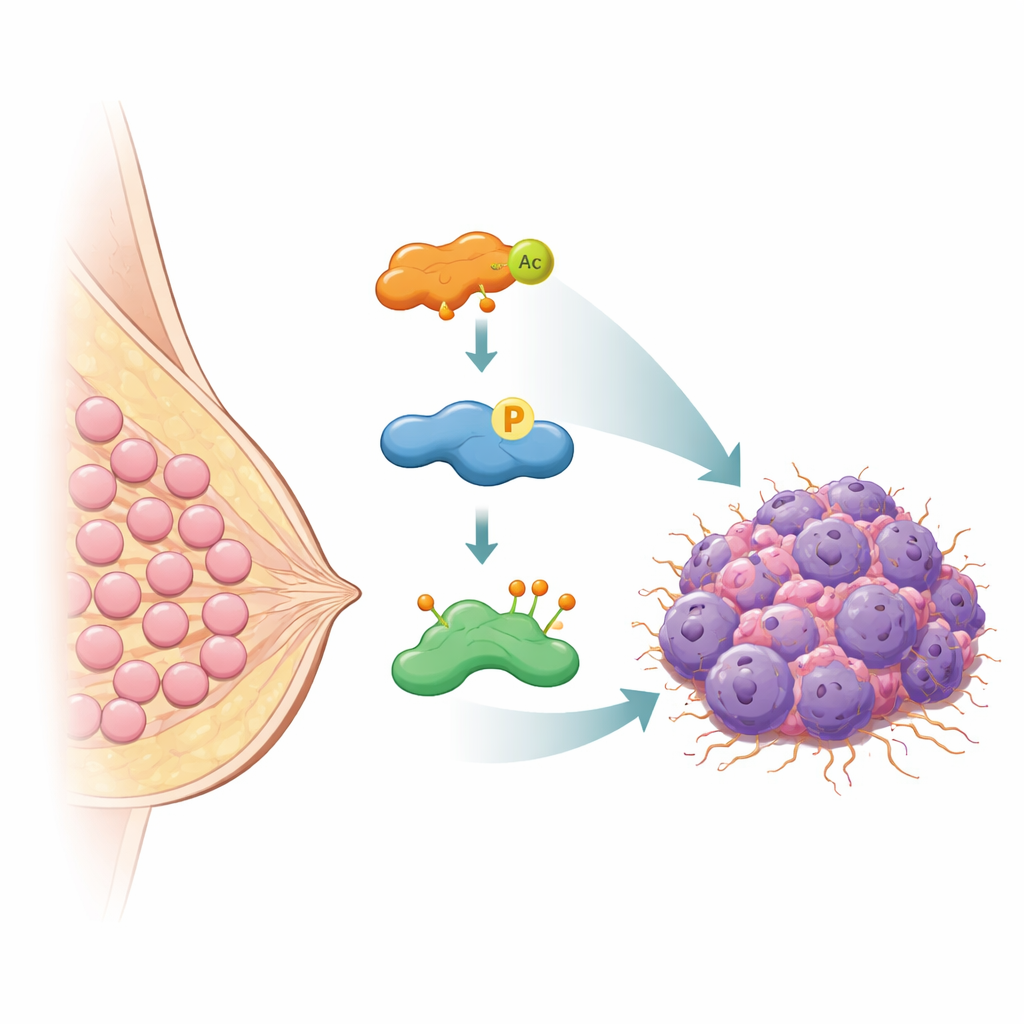
Il guardiano molecolare che salva HASPIN dalla distruzione
Le cellule normalmente prevengono l’accumulo pericoloso di proteine marcando quelle non necessarie per la distruzione con piccoli segnali chiamati ubiquitina, che le indirizzano ai meccanismi di smaltimento cellulare. Gli autori hanno scoperto che una proteina chiamata OTUB2 agisce come un guardiano molecolare per HASPIN. OTUB2 appartiene a una famiglia di enzimi che rimuovono queste etichette ubiquitina. Usando molteplici approcci biochimici, il gruppo ha dimostrato che OTUB2 si lega direttamente a HASPIN all’interno delle cellule di cancro al seno. Quando OTUB2 veniva rimosso, HASPIN veniva pesantemente marcato con una forma particolare di ubiquitina che segnala la degradazione e i suoi livelli diminuivano. Quando OTUB2 era aumentato, queste marchi venivano rimossi, HASPIN veniva risparmiato dalla distruzione e i suoi livelli salivano. Nei modelli murini, i tumori con più OTUB2 crescevano più velocemente e metastatizzavano più facilmente nei polmoni, ma questi effetti dipendevano da HASPIN, sottolineando quanto siano strettamente legati i loro destini.
Una modifica chimica che rafforza la partnership
La storia non finisce con OTUB2. I ricercatori hanno scoperto che HASPIN porta anche un’altra comune modifica chimica chiamata gruppo acetile in una posizione specifica. Questo marchio acetile è aggiunto da un enzima denominato KAT5, noto per modificare proteine che controllano il DNA e l’attività genica. Quando KAT5 aggiunge un gruppo acetile a HASPIN in un sito chiave, l’affinità di HASPIN per OTUB2 aumenta. Di conseguenza, OTUB2 riesce a rimuovere più efficacemente i segnali di degradazione da HASPIN, potenziandone ulteriormente la stabilità. Mutare questo singolo sito per impedire l’acetilazione indeboliva l’interazione con OTUB2 e permetteva l’accumulo di più marcature ubiquitina, facendo degradare HASPIN più rapidamente. In sostanza, KAT5 agisce come una manopola che regola quanto stretta sia la cooperazione tra HASPIN e OTUB2.
Dalle piastre di coltura ai tumori dei pazienti
Per collegare questi risultati alla malattia reale, il gruppo ha esaminato campioni di cancro al seno prelevati da pazienti. Sia le proteine HASPIN sia OTUB2 risultavano costantemente più elevate nel tessuto tumorale rispetto al tessuto normale circostante. In decine di casi, i tumori con livelli più alti di OTUB2 tendevano anche ad avere più HASPIN, rispecchiando la partnership molecolare osservata in laboratorio. È importante che i pazienti i cui tumori mostravano alti livelli di una o dell’altra proteina avessero una sopravvivenza peggiore nel tempo. Questo legame clinico supporta l’idea che la catena KAT5–HASPIN–OTUB2 non sia una curiosità di laboratorio ma un motore operativo all’interno dei tumori umani che li aiuta a crescere e a diffondersi.
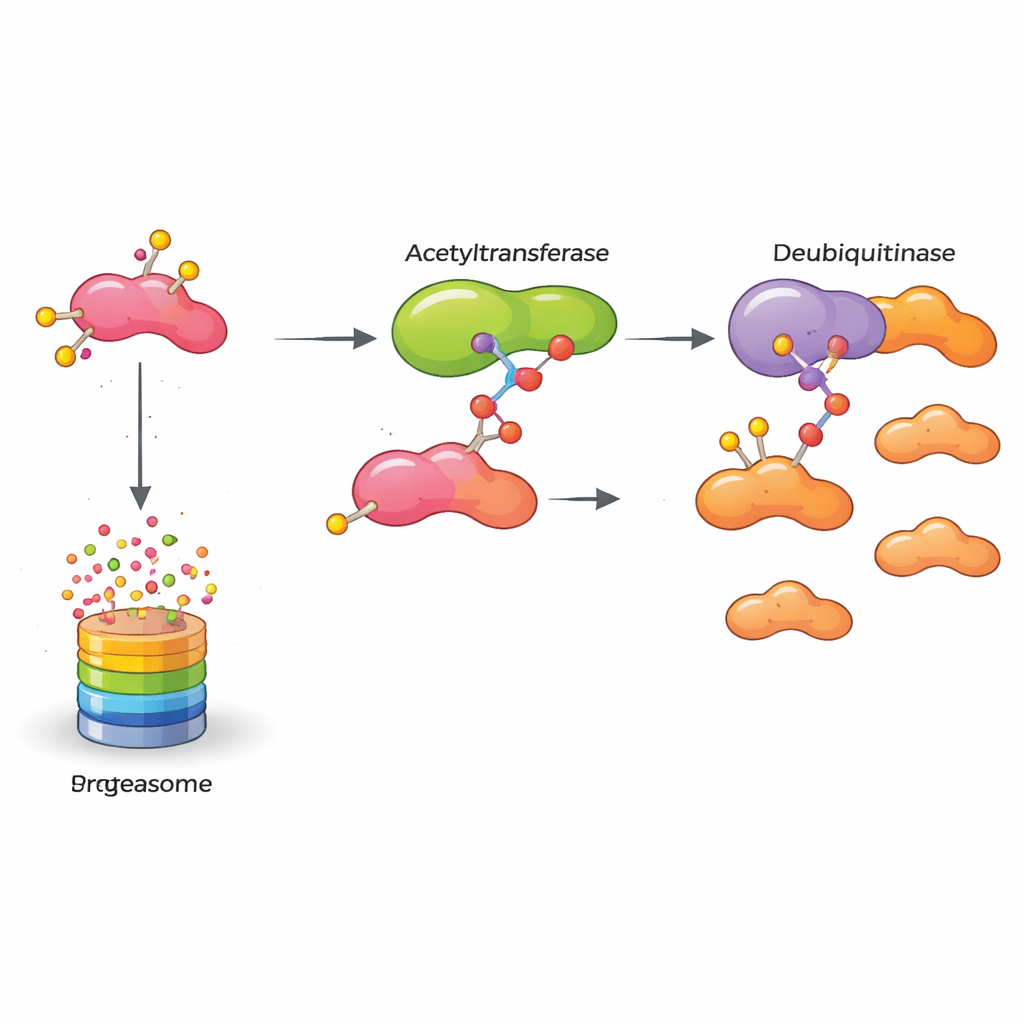
Cosa significa per i trattamenti futuri
Messo insieme, lo studio rivela un relè molecolare che mantiene accesa una proteina promotrice del cancro: KAT5 modifica chimicamente HASPIN, che quindi si lega più saldamente a OTUB2, che a sua volta protegge HASPIN dalla distruzione. Questo HASPIN stabilizzato spinge le cellule del cancro al seno a moltiplicarsi e a invadere. Per i non specialisti, il punto chiave è che bloccare qualsiasi anello di questa catena — il marchio di acetilazione di KAT5, l’azione protettiva di OTUB2 o lo stesso HASPIN — potrebbe indebolire la macchina interna del tumore. Trasformare queste intuizioni in farmaci richiederà tempo, ma il lavoro apre nuove strade per terapie progettate per disarmare selettivamente i tumori mammari aggressivi lasciando che i loro sistemi di controllo della qualità eliminino finalmente i “rifiuti” molecolari.
Citazione: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
Parole chiave: cancro al seno, HASPIN, OTUB2, degradazione proteica, terapia mirata