Clear Sky Science · es
La acetilación mediada por KAT5 potencia la desubiquitinación de HASPIN por OTUB2 y promueve la progresión del cáncer de mama
Por qué importa esta historia sobre el cáncer
El cáncer de mama sigue siendo una de las principales causas de muerte entre las mujeres en todo el mundo, en gran parte porque los tumores agresivos se diseminan a órganos distantes. Este estudio profundiza en los pequeños “interruptores” moleculares que ayudan a las células de cáncer de mama a crecer y desplazarse por el cuerpo. Al descubrir una nueva manera en que las células cancerosas mantienen vivo y activo a un oncoproteína que impulsa el crecimiento, los investigadores señalan nuevas oportunidades para tratamientos más precisos que puedan, algún día, frenar o detener la propagación mortal de la enfermedad.
Una proteína que empuja a las células cancerosas hacia adelante
En el centro de este trabajo está una proteína llamada HASPIN, un tipo de enzima que ayuda a las células a dividirse orientando el manejo de los cromosomas durante la división celular. El equipo halló que los niveles de HASPIN son mucho más altos en tejido de cáncer de mama que en tejido mamario normal, y que las pacientes cuyos tumores contienen más HASPIN tienden a tener una supervivencia global peor. Cuando los investigadores redujeron HASPIN en líneas celulares de cáncer de mama, las células crecieron más despacio, formaron menos colonias y tuvieron menor capacidad de migrar e invadir a través de membranas en el laboratorio. Al aumentar HASPIN ocurrió lo contrario: las células se volvieron más agresivas. Estos experimentos muestran que HASPIN se comporta como un “oncogén” en el cáncer de mama —uno de los motores internos que alimentan el crecimiento y la diseminación tumoral.
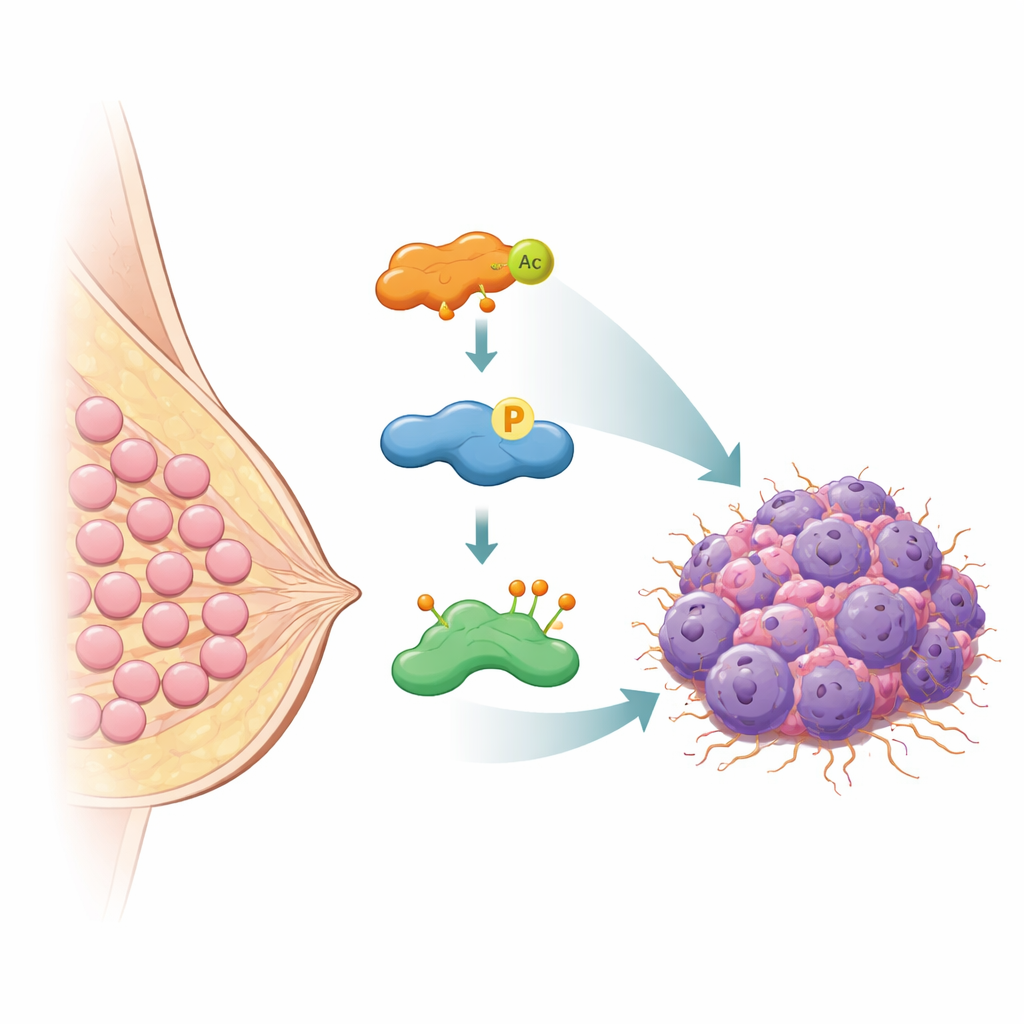
El guardaespaldas molecular que salva a HASPIN de la destrucción
Las células normalmente evitan la acumulación peligrosa de proteínas marcando las proteínas innecesarias para su destrucción con pequeñas etiquetas llamadas ubiquitinas, que las envían a la maquinaria de eliminación de la célula. Los autores descubrieron que una proteína llamada OTUB2 actúa como un guardaespaldas molecular para HASPIN. OTUB2 pertenece a una familia de enzimas que eliminan estas etiquetas de ubiquitina. Utilizando múltiples métodos bioquímicos, el equipo demostró que OTUB2 se une directamente a HASPIN dentro de las células de cáncer de mama. Cuando se eliminó OTUB2, HASPIN quedó fuertemente marcado con una forma particular de ubiquitina que señala la degradación proteica y sus niveles disminuyeron. Al aumentar OTUB2, estas etiquetas se retiraron, HASPIN quedó a salvo de la destrucción y sus niveles aumentaron. En modelos de ratón, los tumores con más OTUB2 crecían más rápido y se diseminaban con mayor facilidad a los pulmones, pero estos efectos dependían de HASPIN, subrayando lo estrechamente vinculados que están sus destinos.
Un ajuste químico que estrecha la asociación
La historia no termina con OTUB2. Los investigadores hallaron que HASPIN también porta otra marca química común llamada grupo acetilo en una posición específica. Esta marca acetil se añade por una enzima llamada KAT5, conocida por modificar proteínas que controlan el ADN y la actividad génica. Cuando KAT5 añadió un grupo acetilo a HASPIN en un sitio clave, la afinidad de HASPIN por OTUB2 se volvió más fuerte. Como resultado, OTUB2 pudo eliminar con mayor eficacia las etiquetas de degradación de HASPIN, aumentando aún más la estabilidad de HASPIN. Mutar este único sitio para impedir la acetilación debilitó la interacción con OTUB2 y permitió que se acumularan más etiquetas de ubiquitina, provocando que HASPIN se degradara más rápido. En esencia, KAT5 actúa como un mando que controla cuán estrechamente cooperan HASPIN y OTUB2.
De las placas de cultivo celular a los tumores de pacientes
Para conectar estos hallazgos con la enfermedad real, el equipo examinó muestras de cáncer de mama de pacientes. Tanto las proteínas HASPIN como OTUB2 fueron consistentemente más altas en tejido tumoral que en tejido normal cercano. En docenas de casos, los tumores que presentaban más OTUB2 también tendían a tener más HASPIN, reflejando la asociación molecular observada en el laboratorio. Importante, las pacientes cuyos tumores mostraban niveles altos de cualquiera de las dos proteínas presentaron una supervivencia peor con el tiempo. Este vínculo clínico respalda la idea de que la cadena KAT5–HASPIN–OTUB2 no es una curiosidad de laboratorio sino un motor funcional dentro de los cánceres humanos que les ayuda a crecer y diseminarse.
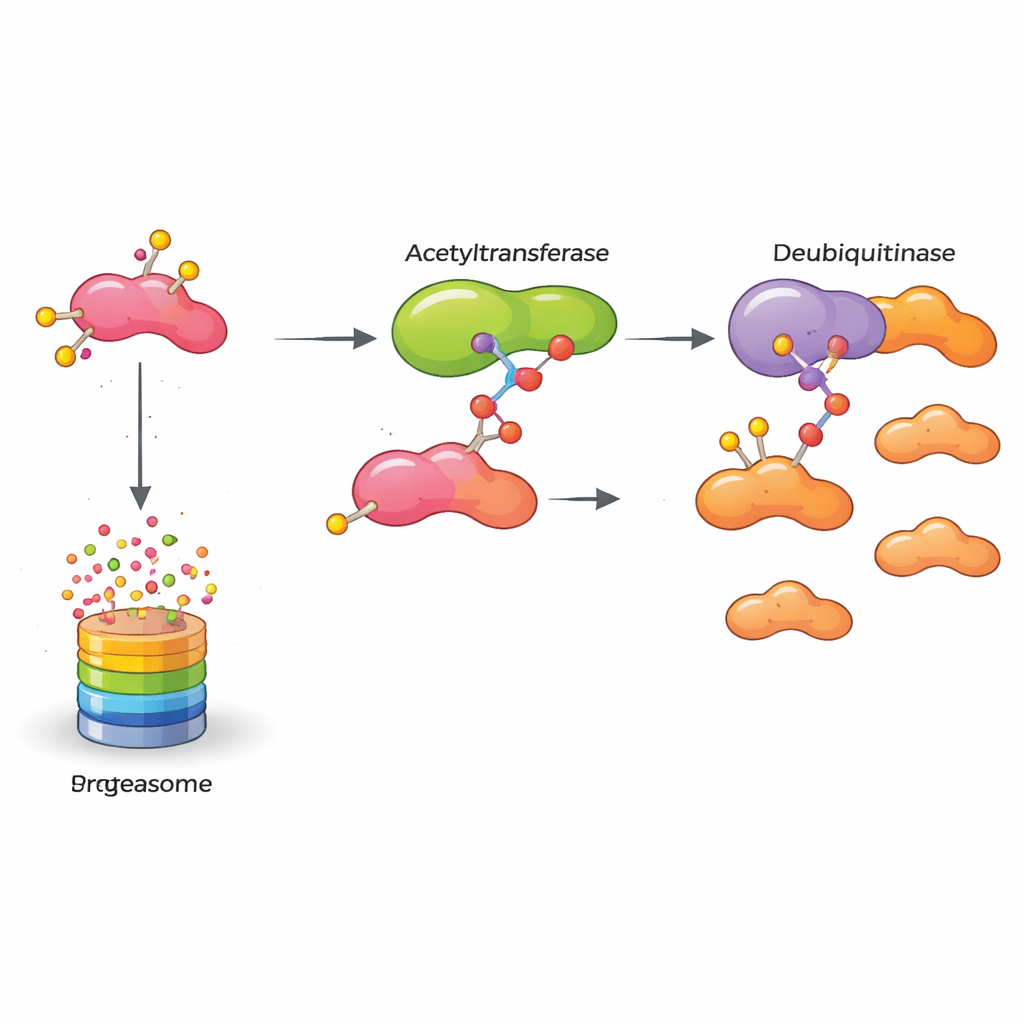
Qué significa esto para tratamientos futuros
En conjunto, el estudio revela un relevo molecular que mantiene encendida a una proteína promotora de cáncer: KAT5 modifica químicamente a HASPIN, que a su vez se une con más fuerza a OTUB2, y OTUB2 protege a HASPIN de ser destruida. Este HASPIN estabilizado impulsa a las células de cáncer de mama a multiplicarse e invadir. Para el público general, la conclusión clave es que bloquear cualquiera de los eslabones de esta cadena —la marca acetil de KAT5, la acción protectora de OTUB2 o el propio HASPIN— podría debilitar la maquinaria interna del tumor. Aunque convertir estos hallazgos en fármacos llevará tiempo, el trabajo abre nuevas vías para terapias diseñadas para desarmar selectivamente a los cánceres de mama agresivos permitiendo que sus propios sistemas de control de calidad eliminen finalmente los residuos moleculares.
Cita: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
Palabras clave: cáncer de mama, HASPIN, OTUB2, degradación de proteínas, terapia dirigida