Clear Sky Science · de
KAT5-vermittelte Acetylierung verstärkt die Deubiquitinierung von HASPIN durch OTUB2 und fördert das Fortschreiten von Brustkrebs
Warum diese Krebsstudie wichtig ist
Brustkrebs bleibt weltweit eine der Haupttodesursachen bei Frauen, vor allem weil aggressive Tumoren in entfernte Organe metastasieren. Diese Studie untersucht die winzigen molekularen „Schalter“, die Brustkrebszellen beim Wachstum und bei der Ausbreitung im Körper unterstützen. Indem die Forschenden eine neue Methode identifizieren, mit der Krebszellen ein wachstumsförderndes Protein am Leben und aktiv halten, eröffnen sie neue Ansatzpunkte für präzisere Behandlungen, die eines Tages das Fortschreiten tödlicher Erkrankungen verlangsamen oder stoppen könnten.
Ein Protein, das Krebszellen antreibt
Im Zentrum dieser Arbeit steht ein Protein namens HASPIN, ein Enzym, das die Zellteilung unterstützt, indem es die Handhabung der Chromosomen während der Mitose steuert. Das Team stellte fest, dass die HASPIN-Spiegel im Brustkrebsgewebe deutlich höher sind als im normalen Brustgewebe, und dass Patientinnen mit tumorspezifisch erhöhtem HASPIN eine schlechtere Gesamtüberlebensrate aufweisen. Reduzierten die Forschenden HASPIN in Brustkrebszelllinien, wuchsen die Zellen langsamer, bildeten weniger Kolonien und zeigten verringerte Wanderungs‑ und Invasionsfähigkeit in Labor-Assays. Bei erhöhter HASPIN-Expression trat das Gegenteil auf: Die Zellen wurden aggressiver. Diese Experimente zeigen, dass HASPIN im Brustkrebs wie ein Onkogen wirkt — ein interner Motor, der Tumorwachstum und -ausbreitung antreibt.
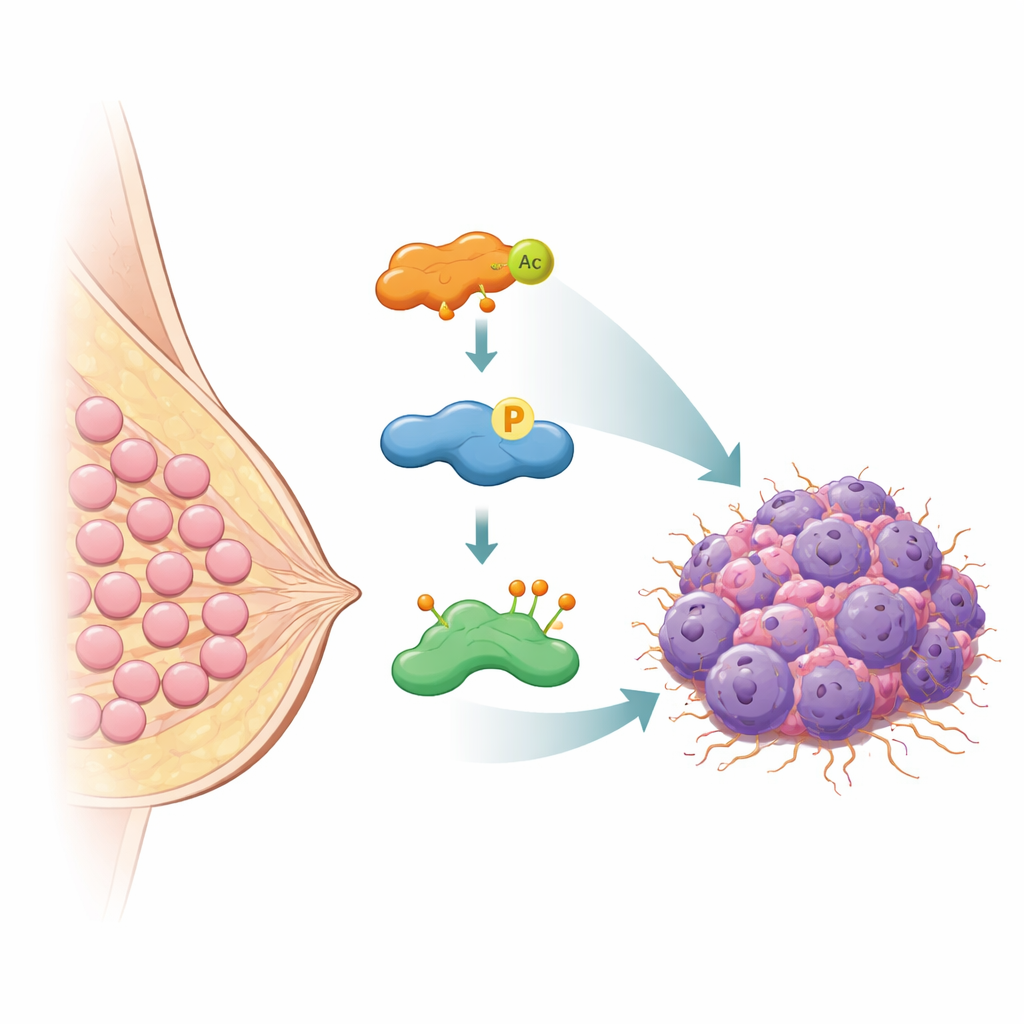
Der molekulare Bodyguard, der HASPIN vor dem Abbau schützt
Zellen verhindern normalerweise eine gefährliche Proteinansammlung, indem sie nicht mehr benötigte Proteine mit kleinen Markern namens Ubiquitin versehen, die sie zur zellulären Abbau-Maschinerie schicken. Die Autorinnen und Autoren entdeckten, dass ein Protein namens OTUB2 als molekularer Bodyguard für HASPIN fungiert. OTUB2 gehört zu einer Enzymfamilie, die diese Ubiquitin-Marker entfernt. Mit verschiedenen biochemischen Methoden zeigte das Team, dass OTUB2 direkt an HASPIN in Brustkrebszellen bindet. Wird OTUB2 entfernt, wird HASPIN stark mit einer Ubiquitin-Form markiert, die den Proteinabbau signalisiert, und seine Menge sinkt. Wird OTUB2 erhöht, werden diese Marker entfernt, HASPIN wird vor dem Abbau bewahrt und seine Spiegel steigen. In Mausmodellen wuchsen Tumoren mit mehr OTUB2 schneller und metastasierten eher in die Lunge — diese Effekte hingen jedoch von HASPIN ab und verdeutlichen, wie eng ihr Schicksal verknüpft ist.
Eine chemische Modifikation, die die Partnerschaft verstärkt
Die Geschichte endet nicht bei OTUB2. Die Forschenden fanden heraus, dass HASPIN auch eine weitere häufige chemische Markierung trägt — eine Acetylgruppe — an einer bestimmten Stelle. Diese Acetylierung wird von einem Enzym namens KAT5 hinzugefügt, das dafür bekannt ist, Proteine zu modifizieren, die DNA und Genaktivität regulieren. Wenn KAT5 eine Acetylgruppe an einer Schlüsselstelle von HASPIN anbringt, wird die Bindung von HASPIN an OTUB2 stärker. Dadurch kann OTUB2 die Abbausignale von HASPIN effektiver entfernen und erhöht so dessen Stabilität weiter. Die Mutation genau dieser Stelle, die Acetylierung verhindert, schwächte die Interaktion mit OTUB2 und ließ mehr Ubiquitin-Marker akkumulieren, sodass HASPIN schneller abgebaut wurde. Im Kern stellt KAT5 einen Regler dar, der bestimmt, wie eng HASPIN und OTUB2 zusammenarbeiten.
Von Zellkulturschalen zu Patientinnen-Tumoren
Um diese Befunde auf die klinische Realität zu übertragen, untersuchte das Team Brustkrebsproben von Patientinnen. Sowohl HASPIN als auch OTUB2 waren im Tumorgewebe konsistent höher als im angrenzenden normalen Gewebe. In Dutzenden von Fällen zeigten Tumoren mit erhöhtem OTUB2 tendenziell ebenfalls höhere HASPIN-Werte, was die im Labor beobachtete molekulare Partnerschaft widerspiegelt. Wichtig ist, dass Patientinnen, deren Tumoren hohe Spiegel eines der beiden Proteine aufwiesen, über die Zeit ein schlechteres Überleben hatten. Dieser klinische Zusammenhang stützt die Idee, dass die KAT5–HASPIN–OTUB2-Achse keine Laborkuriosität ist, sondern ein im menschlichen Krebs wirkender Mechanismus, der Tumorwachstum und -ausbreitung fördert.
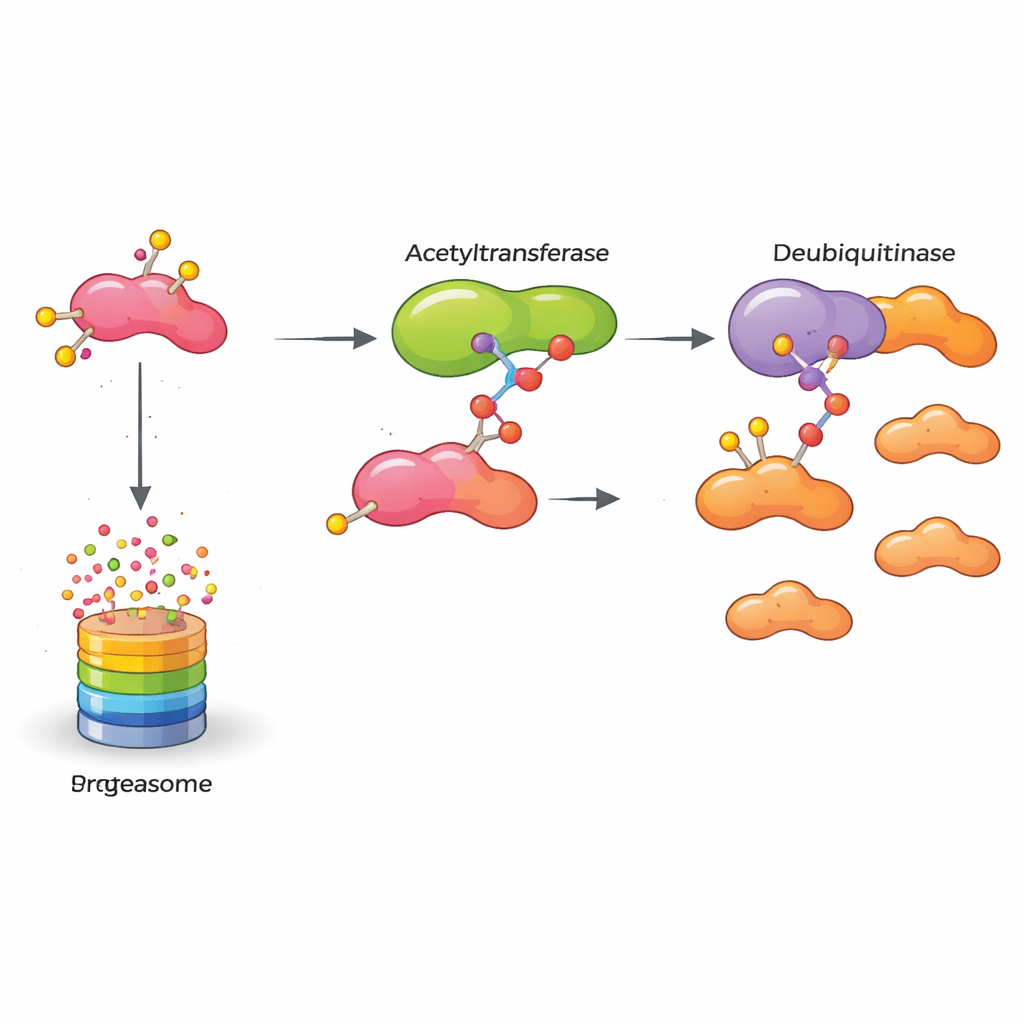
Was das für künftige Behandlungen bedeutet
Insgesamt beschreibt die Studie eine molekulare Kette, die ein krebsförderndes Protein aktiv hält: KAT5 modifiziert HASPIN chemisch, wodurch HASPIN stärker an OTUB2 bindet, das HASPIN wiederum vor dem Abbau schützt. Dieses stabilisierte HASPIN treibt die Vermehrung und Invasion von Brustkrebszellen voran. Für Nicht‑Fachleute lautet die zentrale Botschaft, dass das Blockieren eines Gliedes dieser Kette — die Acetylierung durch KAT5, die Schutzwirkung von OTUB2 oder HASPIN selbst — die interne Maschinerie des Tumors schwächen könnte. Die Umsetzung dieser Erkenntnisse in Medikamente wird Zeit benötigen, doch die Arbeit eröffnet neue Wege für Therapien, die aggressive Brustkrebse gezielt entwaffnen, indem sie deren eigene Qualitätskontrolle das molekulare „Müllproblem“ beseitigen lassen.
Zitation: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
Schlüsselwörter: Brustkrebs, HASPIN, OTUB2, Proteinabbau, zielgerichtete Therapie