Clear Sky Science · pt
A acetilação mediada por KAT5 aumenta a desubiquitinação de HASPIN por OTUB2 e promove a progressão do câncer de mama
Por que esta história sobre câncer importa
O câncer de mama continua sendo uma das principais causas de morte entre mulheres no mundo, em grande parte porque tumores agressivos se espalham para órgãos distantes. Este estudo investiga os pequenos “interruptores” moleculares que ajudam as células do câncer de mama a crescer e a se deslocar pelo corpo. Ao revelar uma nova forma pela qual as células cancerígenas mantêm uma proteína promotora de crescimento viva e ativa, os pesquisadores apontam para oportunidades promissoras de tratamentos mais precisos que, no futuro, poderiam desacelerar ou interromper a metástase fatal.
Uma proteína que impulsiona as células cancerígenas
No centro deste trabalho está uma proteína chamada HASPIN, um tipo de enzima que ajuda as células a se dividirem orientando como os cromossomos são manejados durante a divisão celular. A equipe descobriu que os níveis de HASPIN são muito mais altos em tecido de câncer de mama do que em tecido mamário normal, e que pacientes cujos tumores apresentam mais HASPIN tendem a ter pior sobrevida global. Quando os pesquisadores reduziram a expressão de HASPIN em linhas celulares de câncer de mama, as células cresceram mais devagar, formaram menos colônias e tiveram menor capacidade de migrar e invadir através de membranas em experimentos de laboratório. Quando aumentaram HASPIN, o oposto ocorreu: as células ficaram mais agressivas. Esses experimentos mostram que HASPIN se comporta como um “oncogene” no câncer de mama — um dos motores internos que alimenta o crescimento e a disseminação tumoral.
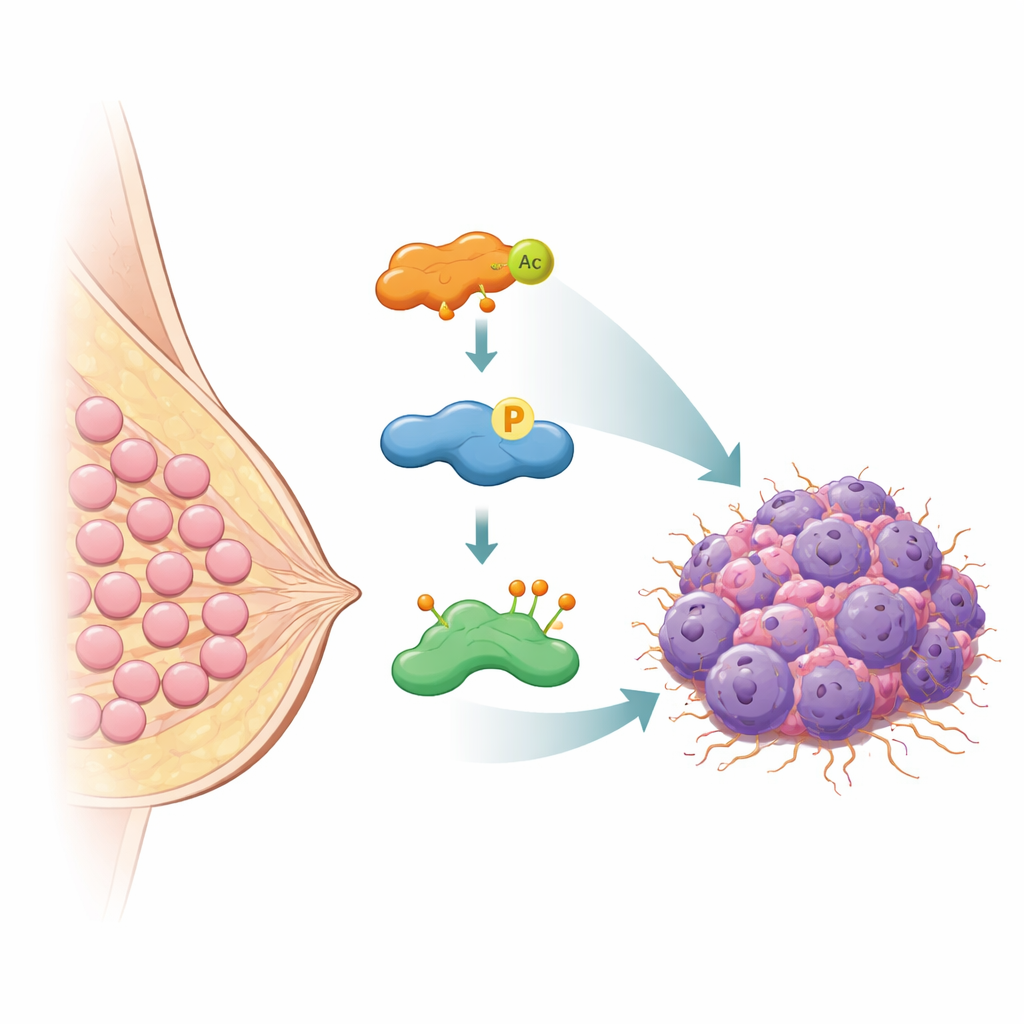
O guarda-costas molecular que salva HASPIN da destruição
As células normalmente evitam o acúmulo perigoso de proteínas marcando proteínas desnecessárias para destruição com pequenas etiquetas chamadas ubiquitinas, que as encaminham para a maquinaria de eliminação celular. Os autores descobriram que uma proteína chamada OTUB2 atua como um guarda-costas molecular para HASPIN. OTUB2 pertence a uma família de enzimas que removem essas marcas de ubiquitina. Usando múltiplos métodos bioquímicos, a equipe mostrou que OTUB2 se liga diretamente a HASPIN dentro de células de câncer de mama. Quando OTUB2 foi removida, HASPIN ficou fortemente marcada por uma forma particular de ubiquitina que sinaliza degradação proteica e seus níveis caíram. Quando OTUB2 foi aumentada, essas marcas foram removidas, HASPIN foi poupada da destruição e seus níveis aumentaram. Em modelos de camundongo, tumores com mais OTUB2 cresceram mais rápido e se espalharam mais facilmente para os pulmões, mas esses efeitos dependiam de HASPIN, ressaltando o quão estreitamente seus destinos estão ligados.
Uma modificação química que reforça a parceria
A história não termina com OTUB2. Os pesquisadores descobriram que HASPIN também carrega outra marca química comum chamada grupo acetil em uma posição específica. Essa marca acetil é adicionada por uma enzima chamada KAT5, conhecida por modificar proteínas que controlam o DNA e a atividade gênica. Quando KAT5 adicionou um grupo acetil a HASPIN em um ponto-chave, a afinidade de HASPIN por OTUB2 ficou mais forte. Como resultado, OTUB2 pôde remover de forma mais eficaz as etiquetas de degradação de HASPIN, aumentando ainda mais a estabilidade de HASPIN. Mutar esse único sítio para impedir a acetilação enfraqueceu a interação com OTUB2 e permitiu que mais marcas de ubiquitina se acumulassem, causando uma degradação mais rápida de HASPIN. Em essência, KAT5 ajusta um botão que controla o quão firmemente HASPIN e OTUB2 cooperam.
De placas de cultura a tumores de pacientes
Para conectar essas descobertas à doença no mundo real, a equipe examinou amostras de câncer de mama de pacientes. Tanto as proteínas HASPIN quanto OTUB2 estavam consistentemente mais altas no tecido tumoral do que no tecido normal adjacente. Em dezenas de casos, tumores com mais OTUB2 também tenderam a ter mais HASPIN, espelhando a parceria molecular observada no laboratório. Importante, pacientes cujos tumores mostraram altos níveis de qualquer uma das proteínas apresentaram pior sobrevida ao longo do tempo. Esse vínculo clínico apoia a ideia de que a cadeia KAT5–HASPIN–OTUB2 não é uma curiosidade de laboratório, mas um mecanismo ativo em cânceres humanos que os ajuda a crescer e se disseminar.
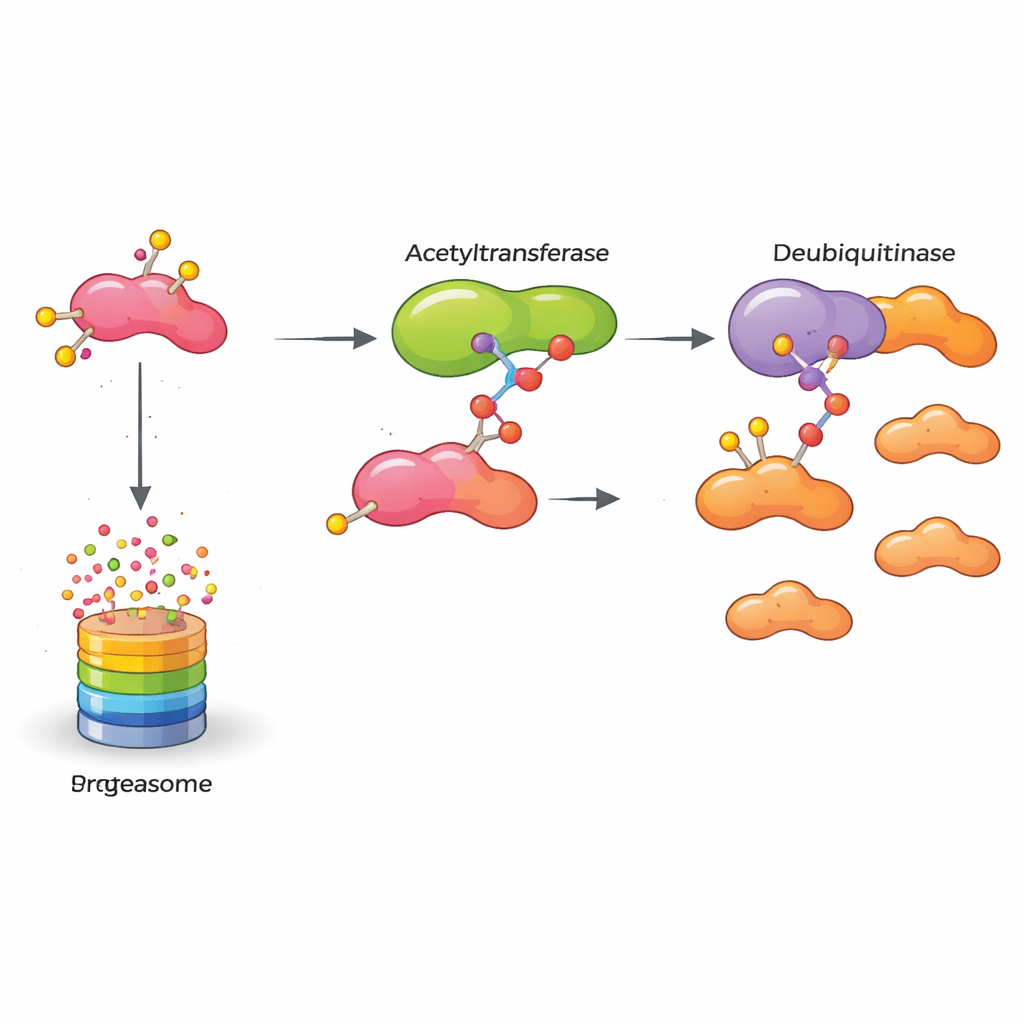
O que isso significa para tratamentos futuros
Em conjunto, o estudo revela um circuito molecular que mantém uma proteína promotora de câncer ativada: KAT5 modifica quimicamente HASPIN, que então se liga mais firmemente à OTUB2, que por sua vez protege HASPIN da destruição. Essa HASPIN estabilizada impulsiona as células de câncer de mama a se multiplicarem e invadirem. Para não especialistas, a conclusão principal é que bloquear qualquer elo dessa cadeia — a marca acetil de KAT5, a ação protetora de OTUB2 ou a própria HASPIN — poderia enfraquecer a maquinaria interna do tumor. Embora transformar essas descobertas em medicamentos leve tempo, o trabalho abre novos caminhos para terapias projetadas para desarmar seletivamente cânceres de mama agressivos, permitindo que seus próprios sistemas de controle de qualidade finalmente eliminem o material molecular indesejado.
Citação: Guo, J., Kang, K., Wang, S. et al. KAT5-mediated acetylation enhances the deubiquitination of HASPIN by OTUB2 and promotes breast cancer progression. Cell Death Dis 17, 411 (2026). https://doi.org/10.1038/s41419-026-08658-5
Palavras-chave: câncer de mama, HASPIN, OTUB2, degradação de proteínas, terapia direcionada