Clear Sky Science · sv
DUSP12 främjar cellcykelns framåtskridande och skyddar celler från ZNF622-medierad apoptos
Varför cellers överlevnadsval spelar roll
Varje sekund fattar våra celler i tysthet beslut om de ska fortsätta växa eller självdö. När denna balans rubbas kan cancer uppstå eller livsviktiga celler gå förlorade vid skador. Denna studie utforskar två hittills relativt okända cellulära ”strömbrytare”, kallade DUSP12 och ZNF622, som hjälper avgöra om en stressad cell reparerar sig och delar sig, eller istället aktiverar ett inneboende dödsprogram. Att förstå hur dessa strömbrytare fungerar kan öppna nya möjligheter både för att döda cancerceller och för att skydda friska vävnader från skada.
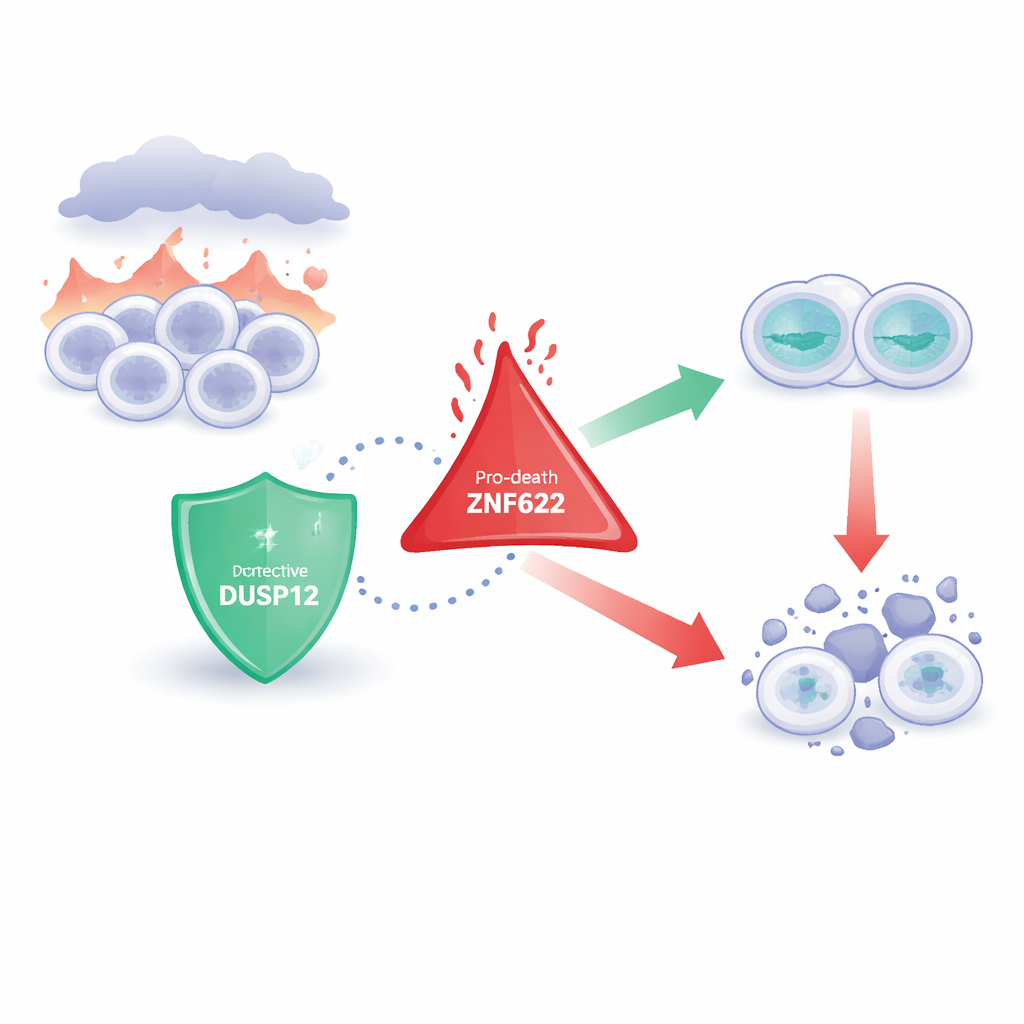
Två motsatta cellulära beskyddare
Forskarna fokuserar på en enzymfamilj som tar bort små kemiska märken från proteiner och därigenom subtilt ändrar hur dessa proteiner beter sig. DUSP12 är ett sådant enzym, länge misstänkt för att påverka celltillväxt och överlevnad men dåligt förstått. ZNF622 är däremot ett protein med ”fingerliknande” strukturer som hjälper det att interagera med många partners och har kopplats till celltillväxt, stressresponser och särskilt till att utlösa celldöd. Tidigare arbete antydde att båda molekylerna var viktiga i cancer, men hur de kan kommunicera med varandra — och vad det betydde för en cells öde — var okänt.
Att hitta ett dolt partnerskap
För att hitta DUSP12:s partners använde teamet biokemiska fiskemetoder i humana celler, där DUSP12 märktes så att alla proteiner som fastnade vid det kunde dras ut och identifieras med masspektrometri, en teknik som väger och katalogiserar proteinfragment. I celler som stod stilla under delning dök ZNF622 upp upprepade gånger tillsammans med DUSP12. Ytterligare tester bekräftade att de två proteinerna bildar ett komplex både inne i celler och i förenklade reaktionssystem. Kartläggning av DUSP12:s struktur visade att detta partnerskap beror på en speciell metallbindande region i ena änden av DUSP12 — zinkbindningsdomen — som fungerar som en dockningsplats för ZNF622.
Att hålla celldelningen på rätt spår
Celldelning är en känslig koreografi där kromosomer måste rada upp sig och separera rent. När forskarna sänkte DUSP12-nivåerna i humana cancerceller stannade fler celler upp under delningen och visade feljusterade kromosomer, och tiden det tog att slutföra delningen ökade. Celler samlades också i sena faser av cellcykeln, vilket tyder på att de hade svårt att gå vidare. När ZNF622 konstgjort ökades fick cellerna återigen allvarliga delningsproblem, inklusive sammantrasslad eller multipolär delningsmaskineri. Intressant nog kunde en specifik plats på ZNF622 antingen vara kemiskt märkt eller omärkt, och DUSP12-aktivitet försköt ZNF622 mot den omärkta formen. Endast den normala versionen av ZNF622, vars märkning kunde ändras fram och tillbaka, orsakade starka delningsdefekter; fasta ”alltid på” eller ”alltid av”-imiterande varianter gjorde det inte. Detta indikerar att DUSP12:s finjustering av denna enstaka plats hjälper till att hålla celldelningen ordnad.
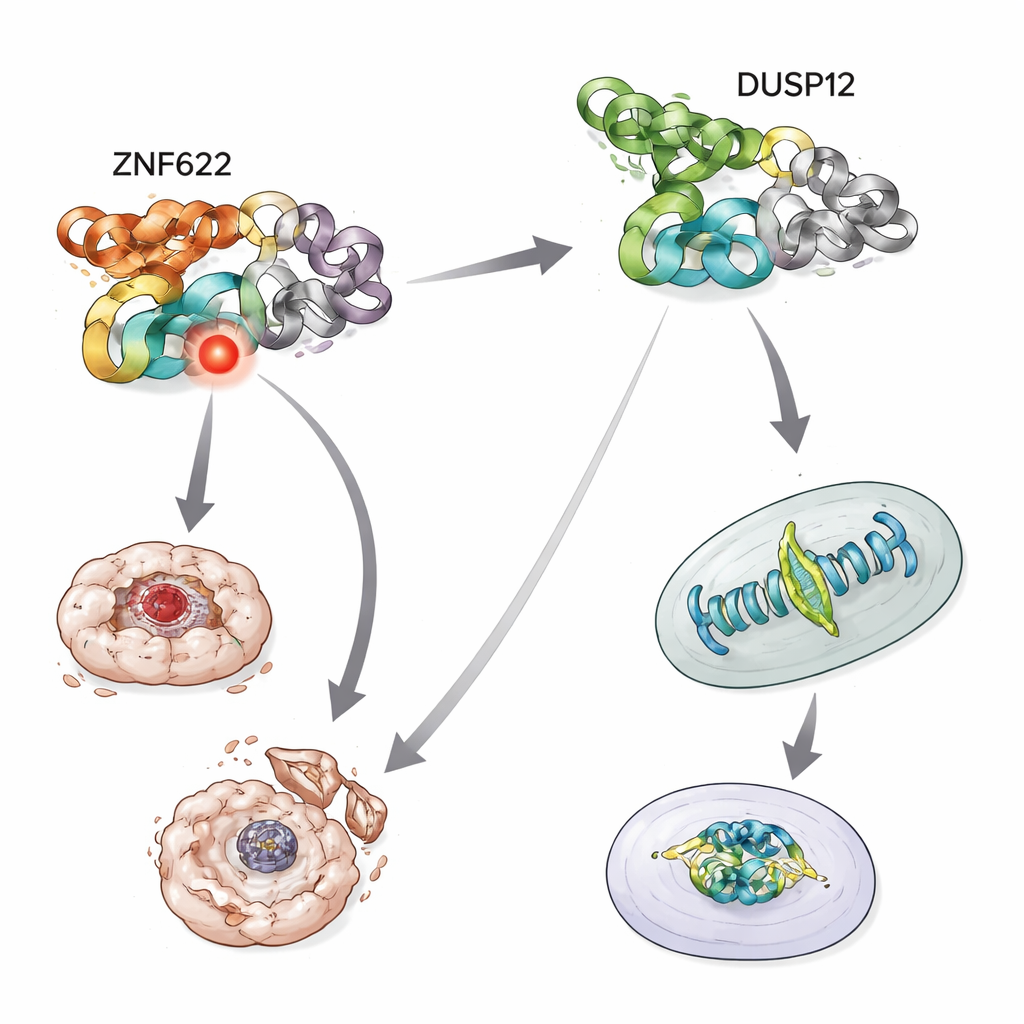
Att balansera liv och död under stress
Teamet frågade sedan vad som händer när celler utsätts för toxisk stress, såsom cytostatika som vanligen driver cancerceller mot självdöd. När DUSP12 utarmades blev cellerna mer benägna att dö som svar på flera anticancerläkemedel och visade högre aktivitet av enzymer som utför celldöd. Däremot gjorde minskning av ZNF622 celler mer motståndskraftiga mot död under samma behandlingar. I omvända experiment skyddade överproduktion av DUSP12 celler från dessa påfrestningar, medan överproduktion av ZNF622 ökade dödligheten. När båda ökades samtidigt dämpade DUSP12 ZNF622:s pro-döds-effekt, och att stegvis höja DUSP12 minskade successivt celldöd även i närvaro av konstant ZNF622. Detta nivåberoende dragkamp visar att de två proteinerna fungerar som motsatta rattar på samma överlevnadskrets.
Vad detta betyder för cancer och bortom
Dessa fynd målar upp DUSP12 som en cellulär livvakt som binder ZNF622 och håller tillbaka dess tendens att ställa till med celldelningsfel och utlösa död, särskilt under läkemedelsinducerad stress. I cancerformer där DUSP12 är onormalt högt kan detta skydd hjälpa tumörceller att överleva kemoterapi, vilket gör DUSP12 till ett attraktivt mål för läkemedel som avlägsnar det skyddet och låter cancerceller dö. Omvänt, i situationer där det är viktigt att bevara celler — såsom att skydda levern under operation eller bromsa nervcellsförlust i degenerativa sjukdomar — kan ökning av DUSP12 eller dämpning av ZNF622 hjälpa vävnader att uthärda skadliga förhållanden. Genom att klargöra hur dessa två proteiner samtalar vid en viktig vändpunkt mellan liv och död erbjuder studien ett nytt grepp för att styra cellöden både inom cancerterapi och vävnadsskydd.
Citering: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Nyckelord: cellcykel, apoptos, cancerterapiresistens, proteinfosfatask, stressrespons