Clear Sky Science · pt
DUSP12 promove a progressão do ciclo celular e protege células da apoptose mediada por ZNF622
Por que as escolhas de sobrevivência celular importam
A cada segundo, nossas células decidem silenciosamente se continuam crescendo ou se autodestroem. Quando esse equilíbrio é alterado, podem surgir cânceres ou células vitais podem ser perdidas durante lesões. Este estudo investiga dois “interruptores” celulares pouco conhecidos, chamados DUSP12 e ZNF622, que ajudam a decidir se uma célula estressada se repara e divide, ou ativa um programa interno de morte. Entender como esses interruptores funcionam pode abrir novas possibilidades tanto para eliminar células cancerosas quanto para proteger tecidos saudáveis de danos.
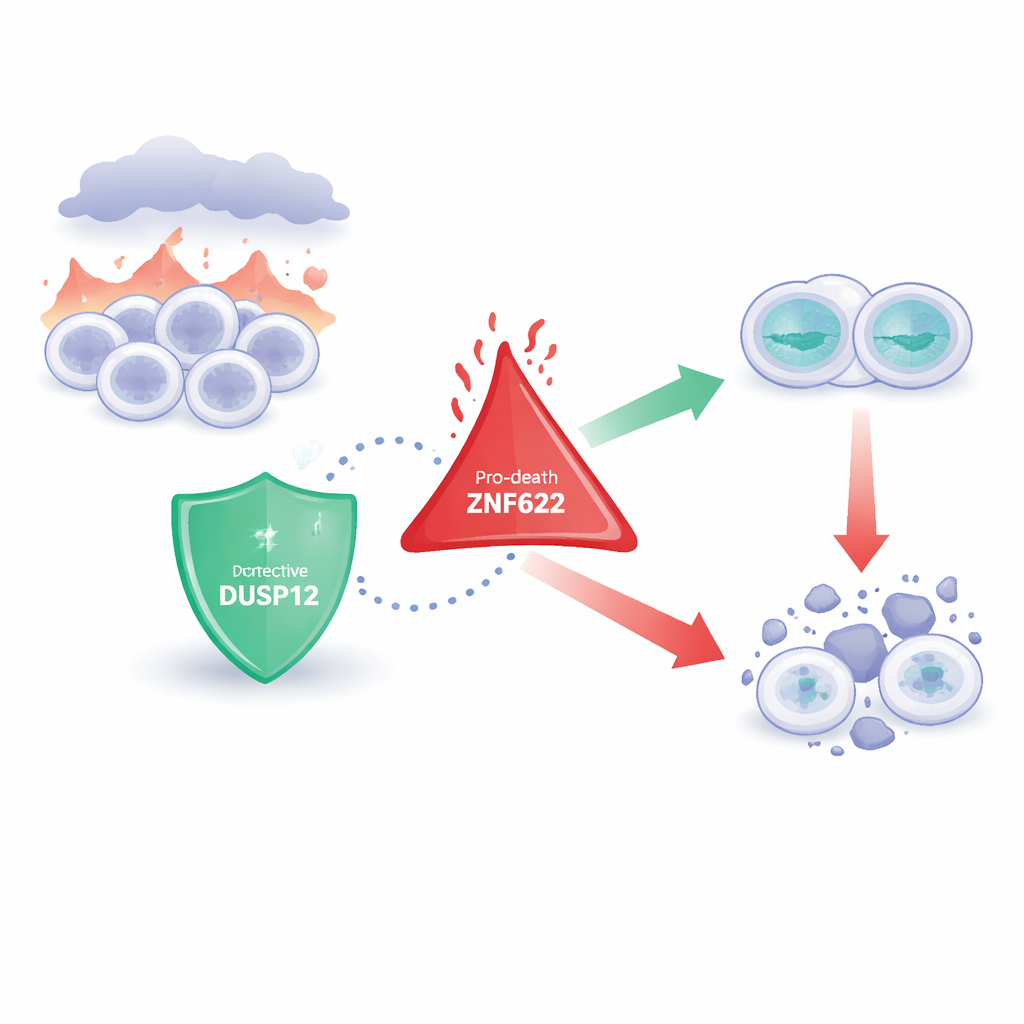
Dois guardiões celulares opostos
Os pesquisadores concentram-se em uma família de enzimas que removem pequenos marcadores químicos de proteínas, alterando sutilmente o comportamento dessas proteínas. DUSP12 é uma dessas enzimas, há muito tempo suspeita de influenciar o crescimento e a sobrevivência celular, mas pouco compreendida. ZNF622, em contraste, é uma proteína com estruturas semelhantes a “dedos” que facilitam a interação com muitos parceiros e tem sido associada ao crescimento celular, respostas ao estresse e, especialmente, ao acionamento da morte celular. Trabalhos anteriores sugeriam que ambas as moléculas eram importantes no câncer, mas como elas se comunicavam — e o que isso significava para o destino da célula — era desconhecido.
Encontrando uma parceria escondida
Para descobrir os parceiros de DUSP12, a equipe usou truques bioquímicos de “pescaria” em células humanas, marcando DUSP12 para que quaisquer proteínas que se ligassem a ela pudessem ser puxadas e identificadas por espectrometria de massas, uma técnica que pesa e cataloga fragmentos proteicos. Em células pausadas durante a divisão, ZNF622 apareceu repetidamente ao lado de DUSP12. Testes adicionais confirmaram que as duas proteínas formam um complexo tanto dentro das células quanto em sistemas simplificados em tubo de ensaio. Mapear a estrutura de DUSP12 mostrou que essa parceria depende de uma região especial que captura metais em uma das extremidades de DUSP12 — o domínio de ligação ao zinco — que atua como um local de ancoragem para ZNF622.
Mantendo a divisão celular no caminho certo
A divisão celular é uma coreografia delicada em que os cromossomos devem se alinhar e separar limpidamente. Quando os cientistas reduziram os níveis de DUSP12 em células cancerosas humanas, mais células ficaram travadas durante a divisão e apresentaram cromossomos desalinhados, e o tempo necessário para completar a divisão aumentou. As células também se acumularam nas fases finais do ciclo celular, sugerindo que tinham dificuldade em progredir. Quando ZNF622 foi artificialmente aumentado, as células novamente desenvolveram problemas graves de divisão, incluindo maquinaria de divisão emaranhada ou multipolar. Intrigantemente, um sítio específico em ZNF622 podia ser quimicamente marcado ou desmarcado, e a atividade de DUSP12 deslocava ZNF622 para a forma desmarcada. Apenas a versão normal de ZNF622, cujo marcador podia alternar, produziu fortes defeitos de divisão; imitações fixas “sempre ligada” ou “sempre desligada” não o fizeram. Isso indica que o ajuste fino de DUSP12 desse único sítio ajuda a manter a ordem na divisão celular.
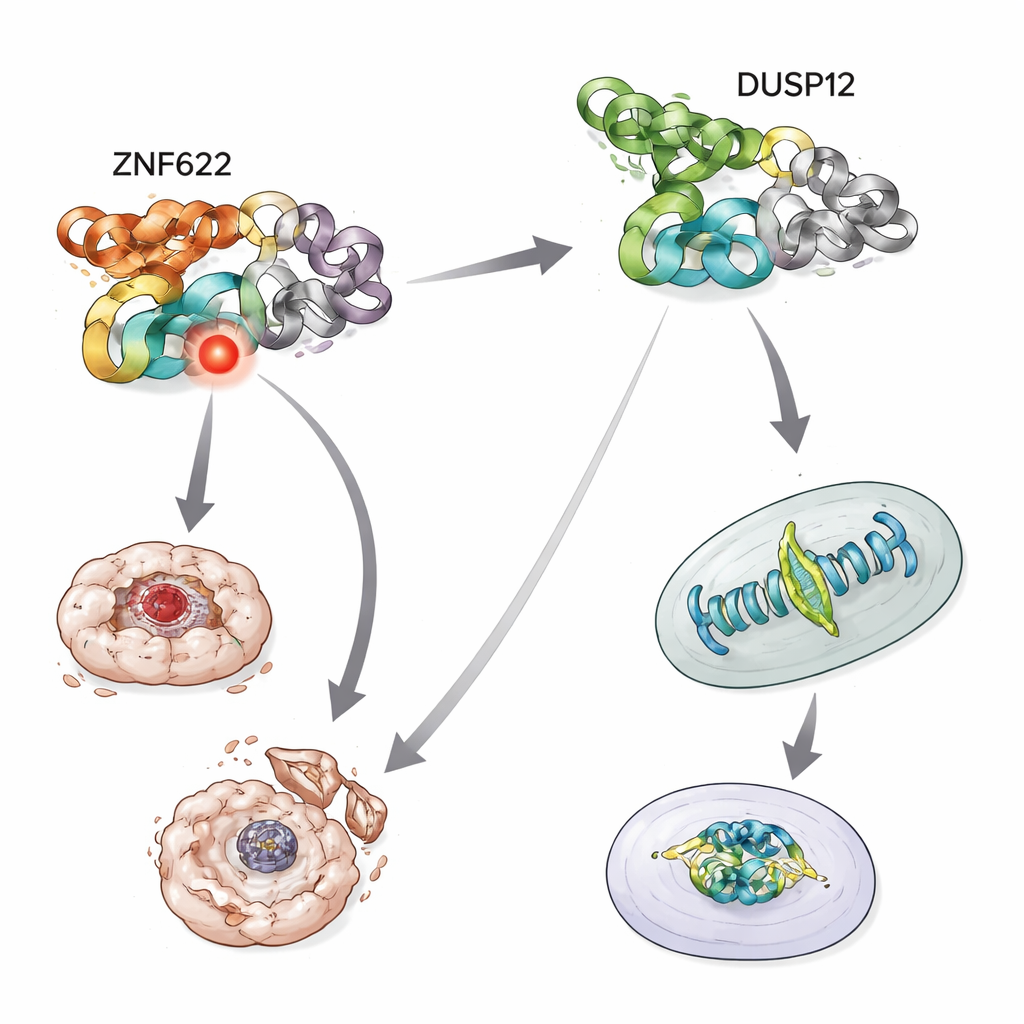
Equilibrando vida e morte sob estresse
A equipe então investigou o que acontece quando células são expostas a estresses tóxicos, como medicamentos quimioterápicos que normalmente empurram células cancerosas para a autodestituição. Quando DUSP12 foi depletada, as células tornaram-se mais propensas a morrer em resposta a vários agentes anticâncer, exibindo maior atividade de enzimas que executam a morte celular. Em contraste, reduzir ZNF622 tornou as células mais resistentes a morrer sob os mesmos tratamentos. Invertendo o experimento, superproduzir DUSP12 protegendo as células desses estresses, enquanto superproduzir ZNF622 tornou a morte mais provável. Quando ambos foram aumentados juntos, DUSP12 atenuou o efeito pró-morte de ZNF622, e aumentar DUSP12 de forma gradual reduziu progressivamente a morte celular mesmo na presença de ZNF622 constante. Essa disputa dependente de nível mostra que as duas proteínas atuam como botões opostos no mesmo circuito de sobrevivência.
O que isso significa para o câncer e além
Essas descobertas pintam DUSP12 como um guarda-costas celular que se liga a ZNF622 e contém sua tendência a descarrilar a divisão celular e a desencadear a morte, especialmente sob estresse induzido por drogas. Em cânceres onde DUSP12 está anormalmente alto, essa proteção pode ajudar células tumorais a sobreviver à quimioterapia, tornando DUSP12 um alvo atraente para fármacos projetados para remover esse escudo e permitir que células cancerosas morram. Por outro lado, em situações onde preservar células é crucial — como proteger o fígado durante cirurgia ou desacelerar a perda de neurônios em doenças degenerativas — aumentar DUSP12 ou diminuir ZNF622 pode ajudar os tecidos a resistir a condições danosas. Ao esclarecer como essas duas proteínas conversam em um ponto decisório chave entre vida e morte, o estudo oferece um novo ponto de alavancagem para ajustar o destino celular tanto na terapia do câncer quanto na proteção tecidual.
Citação: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Palavras-chave: ciclo celular, apoptose, resistência à terapia do câncer, fosfatase de proteína, resposta ao estresse