Clear Sky Science · es
DUSP12 promueve la progresión del ciclo celular y protege a las células de la apoptosis mediada por ZNF622
Por qué importan las decisiones sobre la supervivencia celular
Cada segundo, nuestras células deciden en silencio si seguir creciendo o autodestruirse. Cuando este equilibrio se altera, pueden aparecer cánceres o perderse células que salvan vidas durante una lesión. Este estudio explora dos “interruptores” celulares poco conocidos, llamados DUSP12 y ZNF622, que ayudan a decidir si una célula estresada se repara y se divide o activa un programa de muerte incorporado. Entender cómo funcionan estos interruptores podría abrir nuevas vías tanto para eliminar células cancerosas como para proteger tejidos sanos del daño.
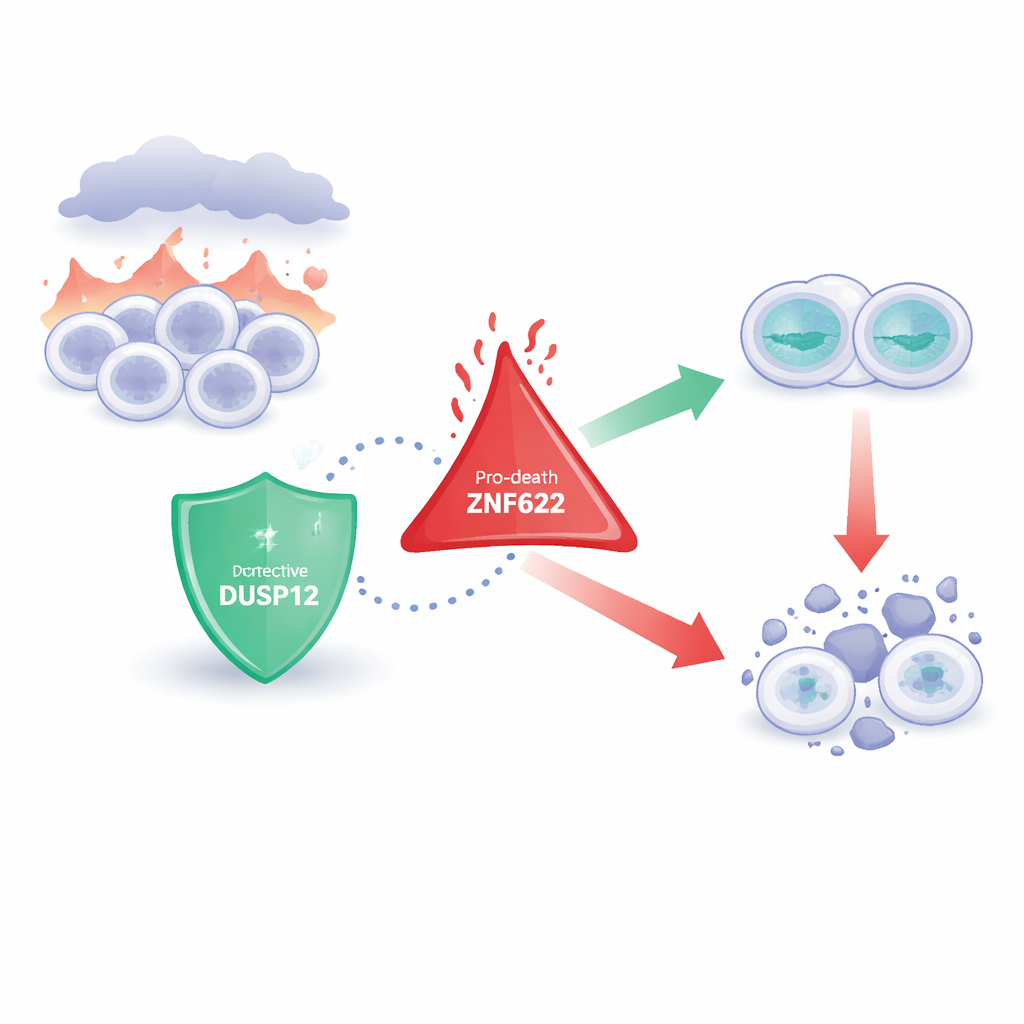
Dos guardianes celulares opuestos
Los investigadores se centran en una familia de enzimas que eliminan pequeñas etiquetas químicas de las proteínas, cambiando sutilmente su comportamiento. DUSP12 es una de esas enzimas, sospechada desde hace tiempo de influir en el crecimiento y la supervivencia celular, pero poco comprendida. ZNF622, en contraste, es una proteína con estructuras en forma de “dedo” que le permiten interactuar con muchos socios y se ha vinculado al crecimiento celular, las respuestas al estrés y, en especial, a desencadenar la muerte celular. Trabajos anteriores sugerían que ambas moléculas eran importantes en el cáncer, pero se desconocía cómo podrían comunicarse entre sí y qué implicaba eso para el destino de la célula.
Descubriendo una asociación oculta
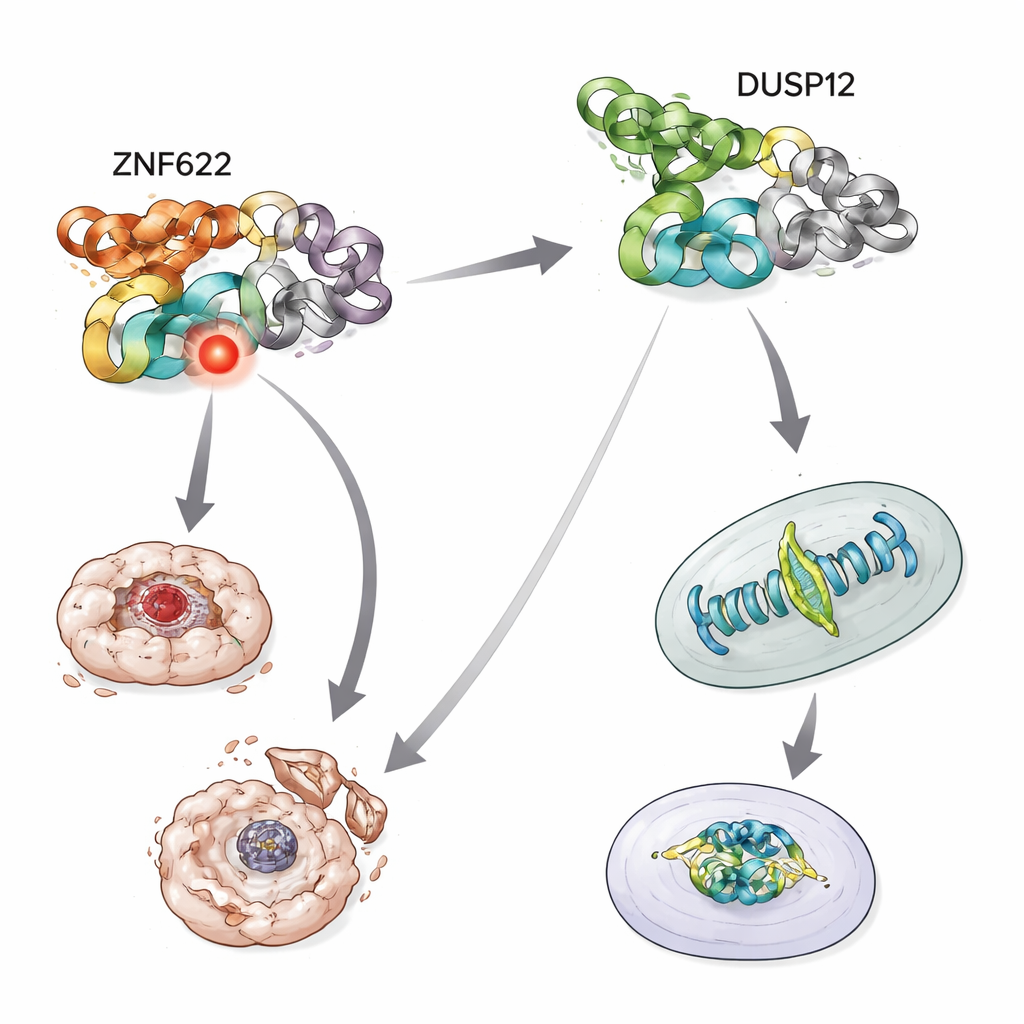
Para identificar los socios de DUSP12, el equipo empleó trucos bioquímicos de pesca en células humanas, etiquetando DUSP12 para que las proteínas que se unieran a ella pudieran extraerse e identificarse mediante espectrometría de masas, una técnica que pesa y cataloga fragmentos proteicos. En células detenidas durante la división, ZNF622 apareció repetidamente junto a DUSP12. Pruebas adicionales confirmaron que las dos proteínas forman un complejo tanto dentro de las células como en sistemas simplificados in vitro. El mapeo de la estructura de DUSP12 mostró que esta asociación depende de una región especial que captura metales en uno de los extremos de DUSP12 —el dominio de unión al zinc— que actúa como sitio de acoplamiento para ZNF622.
Manteniendo la división celular en orden
La división celular es una coreografía delicada en la que los cromosomas deben alinearse y separarse con precisión. Cuando los científicos redujeron los niveles de DUSP12 en células cancerosas humanas, más células se quedaron atascadas durante la división y mostraron cromosomas desalineados, y el tiempo necesario para completar la división aumentó. Las células también se acumularon en las fases tardías del ciclo celular, lo que sugiere que tenían dificultades para progresar. Cuando ZNF622 se elevó artificialmente, las células volvieron a desarrollar problemas graves de división, incluyendo el enredo o la formación de husos multipolares. De forma intrigante, un sitio específico en ZNF622 podía estar químicamente etiquetado o no, y la actividad de DUSP12 desplazaba a ZNF622 hacia la forma no etiquetada. Solo la versión normal de ZNF622, cuya etiqueta podía cambiar de ida y vuelta, produjo defectos de división pronunciados; los imitadores fijos de “siempre activado” o “siempre desactivado” no lo hicieron. Esto indica que el ajuste fino de DUSP12 sobre ese único sitio ayuda a mantener el orden en la división celular.
Equilibrando la vida y la muerte bajo estrés
El equipo preguntó entonces qué ocurre cuando las células se exponen a estreses tóxicos, como fármacos quimioterapéuticos que habitualmente empujan a las células cancerosas hacia la autodestrucción. Cuando DUSP12 se agotó, las células se volvieron más propensas a morir en respuesta a varios agentes anticancerígenos, mostrando mayor actividad de enzimas que ejecutan la muerte celular. En contraste, reducir ZNF622 hizo que las células fueran más resistentes a morir con los mismos tratamientos. Al invertir el experimento, sobreproducir DUSP12 protegió a las células de estos estreses, mientras que sobreproducir ZNF622 aumentó la probabilidad de muerte. Cuando ambos se incrementaron juntos, DUSP12 atenuó el efecto pro-muerte de ZNF622, y aumentar DUSP12 de forma escalonada redujo progresivamente la muerte celular incluso en presencia de ZNF622 constante. Esta lucha por niveles muestra que las dos proteínas actúan como perillas opuestas en el mismo circuito de supervivencia.
Qué significa esto para el cáncer y más allá
Estos hallazgos dibujan a DUSP12 como un guardaespaldas celular que se une a ZNF622 y modera su tendencia a descarrilar la división celular y desencadenar la muerte, especialmente bajo estrés inducido por fármacos. En cánceres donde DUSP12 está anormalmente alto, esta protección puede ayudar a las células tumorales a sobrevivir a la quimioterapia, lo que convierte a DUSP12 en un objetivo atractivo para fármacos diseñados para despojar esa protección y permitir que las células cancerosas mueran. Por el contrario, en situaciones donde preservar células es crucial —como proteger el hígado durante una cirugía o frenar la pérdida de neuronas en enfermedades degenerativas— potenciar DUSP12 o reducir ZNF622 podría ayudar a los tejidos a resistir condiciones dañinas. Al aclarar cómo conversan estas dos proteínas en un punto clave de decisión entre la vida y la muerte, el estudio ofrece una nueva palanca para ajustar el destino celular tanto en terapia contra el cáncer como en protección de tejidos.
Cita: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Palabras clave: ciclo celular, apoptosis, resistencia a la terapia contra el cáncer, fosfatasa de proteínas</keyword:f> <keyword>respuesta al estrés