Clear Sky Science · fr
DUSP12 favorise la progression du cycle cellulaire et protège les cellules de l’apoptose médiée par ZNF622
Pourquoi les choix de survie cellulaire comptent
À chaque seconde, nos cellules décident discrètement de continuer à se diviser ou de s’autodétruire. Quand cet équilibre est perturbé, des cancers peuvent apparaître ou des cellules vitales peuvent être perdues lors d’une lésion. Cette étude examine deux « interrupteurs » cellulaires peu connus, DUSP12 et ZNF622, qui participent à la décision d’un cellule stressée : se réparer et se diviser, ou activer un programme mortel interne. Comprendre le fonctionnement de ces interrupteurs pourrait ouvrir de nouvelles voies, à la fois pour éliminer les cellules cancéreuses et pour protéger les tissus sains contre les dommages.
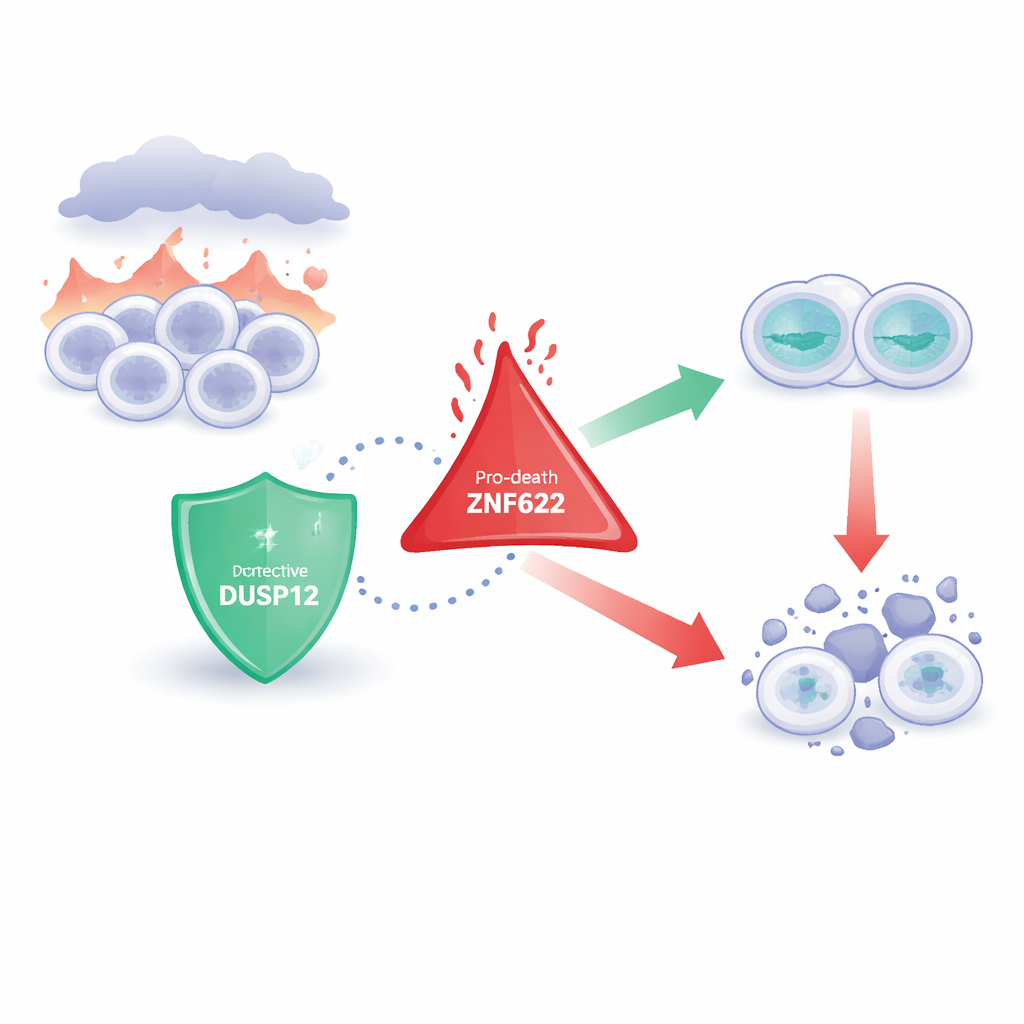
Deux gardiens cellulaires opposés
Les chercheurs se concentrent sur une famille d’enzymes qui retirent de petites balises chimiques des protéines, modifiant subtilement leur comportement. DUSP12 est l’une de ces enzymes, longtemps soupçonnée d’influencer la croissance et la survie cellulaire mais mal comprise. ZNF622, en revanche, est une protéine dotée de structures « en doigt » qui lui permettent d’interagir avec de nombreux partenaires et a été liée à la croissance cellulaire, aux réponses au stress, et surtout au déclenchement de la mort cellulaire. Des travaux antérieurs suggéraient que les deux molécules étaient importantes en cancérologie, mais la façon dont elles communiquent entre elles — et ce que cela implique pour le destin d’une cellule — restait inconnue.
Découvrir un partenariat caché
Pour révéler les partenaires de DUSP12, l’équipe a utilisé des méthodes biochimiques de type pêche dans des cellules humaines, marquant DUSP12 afin que les protéines qui s’y lient puissent être isolées et identifiées par spectrométrie de masse, une technique qui pèse et répertorie des fragments protéiques. Dans des cellules bloquées pendant la division, ZNF622 est apparu à plusieurs reprises aux côtés de DUSP12. Des tests complémentaires ont confirmé que les deux protéines forment un complexe à la fois dans les cellules et dans des systèmes simplifiés en éprouvette. La cartographie de la structure de DUSP12 a montré que ce partenariat dépend d’une région spéciale capable de capturer un métal à une extrémité de DUSP12 — le domaine de liaison au zinc — qui sert de site d’ancrage pour ZNF622.
Maintenir la division cellulaire sur la bonne voie
La division cellulaire est une chorégraphie délicate où les chromosomes doivent s’aligner et se séparer proprement. Lorsque les chercheurs ont réduit les niveaux de DUSP12 dans des cellules cancéreuses humaines, davantage de cellules ont bloqué leur division et présenté des chromosomes mal alignés, et le temps nécessaire pour achever la division a augmenté. Les cellules s’accumulaient également dans les phases tardives du cycle cellulaire, suggérant des difficultés de progression. Lorsque ZNF622 était surexprimé artificiellement, les cellules développaient à nouveau de graves problèmes de division, y compris des machineries de division emmêlées ou multipolaires. De façon intrigante, un site spécifique sur ZNF622 pouvait être soit marqué chimiquement soit non marqué, et l’activité de DUSP12 orientait ZNF622 vers la forme non marquée. Seule la version normale de ZNF622, dont la marque pouvait changer alternativement, provoquait de forts défauts de division ; des mimétiques « toujours activés » ou « toujours désactivés » ne le faisaient pas. Cela indique que le réglage fin par DUSP12 de ce site unique aide à maintenir l’ordre de la division cellulaire.
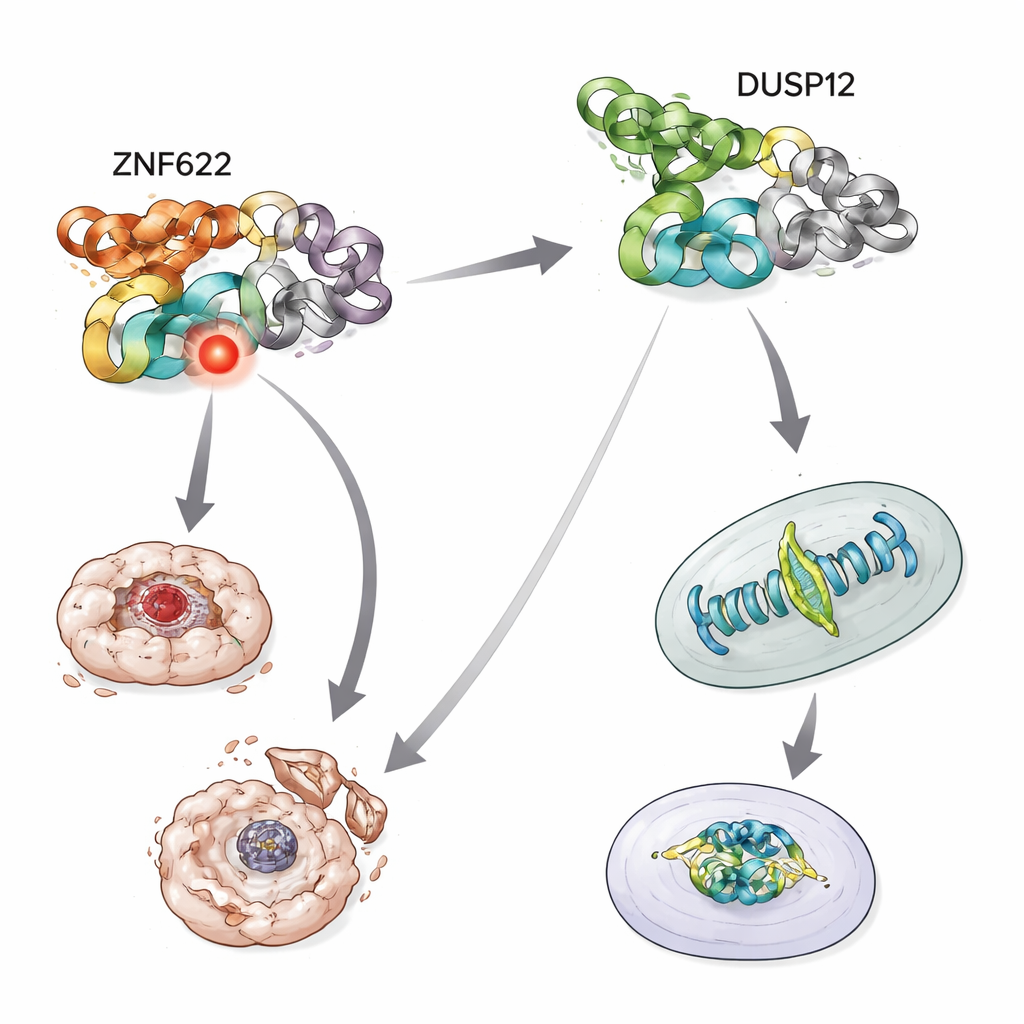
Équilibrer vie et mort sous stress
Les auteurs se sont ensuite demandé ce qui se passe lorsque les cellules sont exposées à des stress toxiques, tels que des chimiothérapies qui poussent généralement les cellules cancéreuses vers l’autodestruction. Lorsque DUSP12 était éliminé, les cellules devenaient plus susceptibles de mourir en réponse à plusieurs agents anticancéreux, montrant une activité accrue des enzymes exécutrices de la mort cellulaire. Par contraste, diminuer ZNF622 rendait les cellules plus résistantes à la mort sous les mêmes traitements. Inversement, la surexpression de DUSP12 protégeait les cellules contre ces stress, tandis que la surexpression de ZNF622 favorisait la mort. Lorsque les deux protéines étaient augmentées simultanément, DUSP12 atténuait l’effet pro‑mort de ZNF622, et une augmentation progressive de DUSP12 réduisait graduellement la mort cellulaire même en présence d’un ZNF622 constant. Ce bras de fer dépendant du dosage montre que les deux protéines agissent comme des boutons opposés sur le même circuit de survie.
Ce que cela signifie pour le cancer et au‑delà
Ces résultats décrivent DUSP12 comme une sentinelle cellulaire qui se lie à ZNF622 et freine sa tendance à perturber la division cellulaire et à déclencher la mort, notamment sous stress induit par les médicaments. Dans les cancers où DUSP12 est anormalement élevé, cette protection peut aider les cellules tumorales à survivre à la chimiothérapie, faisant de DUSP12 une cible attractive pour des médicaments visant à supprimer ce bouclier et laisser les cellules cancéreuses mourir. À l’inverse, dans des situations où préserver les cellules est crucial — comme protéger le foie pendant une chirurgie ou ralentir la perte des neurones dans des maladies dégénératives — renforcer DUSP12 ou atténuer ZNF622 pourrait aider les tissus à résister aux conditions dommageables. En clarifiant la manière dont ces deux protéines dialoguent à un point clé de décision entre la vie et la mort, l’étude offre une nouvelle poignée pour ajuster le destin cellulaire, tant en thérapie anticancéreuse qu’en protection tissulaire.
Citation: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Mots-clés: cycle cellulaire, apoptose, résistance aux traitements du cancer, protéine phosphatase, réponse au stress