Clear Sky Science · nl
DUSP12 bevordert de voortgang van de celcyclus en beschermt cellen tegen ZNF622-gemedieerde apoptose
Waarom keuzes voor celsurvival ertoe doen
Elke seconde beslissen onze cellen stilletjes of ze blijven groeien of zichzelf vernietigen. Wanneer dit evenwicht verstoord raakt, kunnen kankers ontstaan of kunnen levensreddende cellen verloren gaan bij letsel. Deze studie onderzoekt twee weinig bekende cellulaire “schakelaars”, DUSP12 en ZNF622, die helpen bepalen of een gestreste cel zichzelf herstelt en deelt, of in plaats daarvan een ingebouwd doodsprogramma activeert. Begrijpen hoe deze schakelaars werken kan nieuwe wegen openen om zowel kankercellen te doden als gezonde weefsels te beschermen tegen schade.
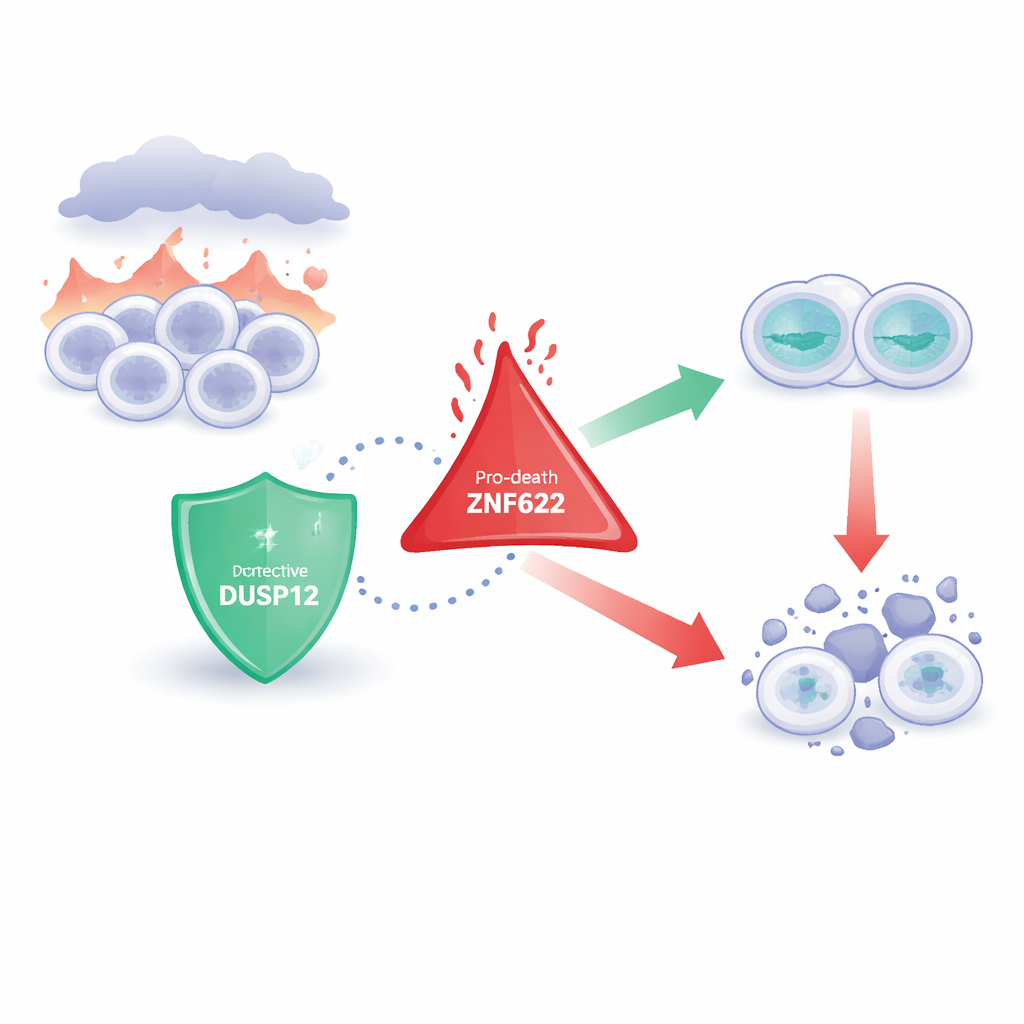
Twee tegenovergestelde cellulaire bewakers
De onderzoekers richten zich op een familie enzymen die kleine chemische labels van eiwitten verwijderen, waardoor het gedrag van die eiwitten subtiel verandert. DUSP12 is zo’n enzym, al langer vermoed van invloed op celgroei en overleving maar slecht begrepen. ZNF622 daarentegen is een eiwit met ‘vingerachtige’ structuren die het in staat stellen met veel partners te interageren en dat in verband is gebracht met celgroei, stressresponsen en vooral met het activeren van celdood. Eerder werk suggereerde dat beide moleculen belangrijk zijn bij kanker, maar hoe ze met elkaar zouden communiceren — en wat dat voor het lot van een cel betekende — was onbekend.
Een verborgen partnerschap opsporen
Om de partners van DUSP12 te vinden, gebruikte het team biochemische ‘vangst’-trucs in menselijke cellen, waarbij DUSP12 werd gemarkeerd zodat alle eraan vastzittende eiwitten konden worden gevangen en geïdentificeerd met massaspectrometrie, een techniek die eiwitfragmenten weegt en catalogiseert. In cellen die tijdens de deling gepauzeerd waren, verscheen ZNF622 herhaaldelijk samen met DUSP12. Verdere tests bevestigden dat de twee eiwitten een complex vormen zowel binnen cellen als in vereenvoudigde reageerbuis systemen. Het in kaart brengen van DUSP12’s structuur toonde aan dat dit partnerschap afhankelijk is van een speciale metaal-vastgrijpende regio aan één uiteinde van DUSP12 — het zink-bindende domein — dat fungeert als aanmeerplaats voor ZNF622.
De celdeling op koers houden
Celdeling is een delicate choreografie waarbij chromosomen zich netjes moeten opstellen en scheiden. Toen de wetenschappers DUSP12-niveaus verlaagden in menselijke kankercellen, raakten meer cellen vastgelopen tijdens de deling en vertoonden ze verkeerd uitgelijnde chromosomen, en de tijd die nodig was om de deling te voltooien nam toe. Cellen stapelden zich ook op in de late stadia van de celcyclus, wat suggereert dat ze moeite hadden met voortgang. Toen ZNF622 kunstmatig werd verhoogd, ontwikkelden cellen opnieuw ernstige delingsproblemen, inclusief verward of multipolair delingsapparaat. Intrigerend was dat een specifieke plaats op ZNF622 chemisch gelabeld of niet gelabeld kon zijn, en DUSP12-activiteit verschuift ZNF622 naar de niet-gelabelde vorm. Alleen de normale versie van ZNF622, waarvan het label heen en weer kon veranderen, veroorzaakte sterke delingsdefecten; vaste ’altijd aan’ of ’altijd uit’ imitaties deden dat niet. Dit wijst erop dat DUSP12’s fijnafstemming van die enkele site helpt om de celdeling ordelijk te houden.
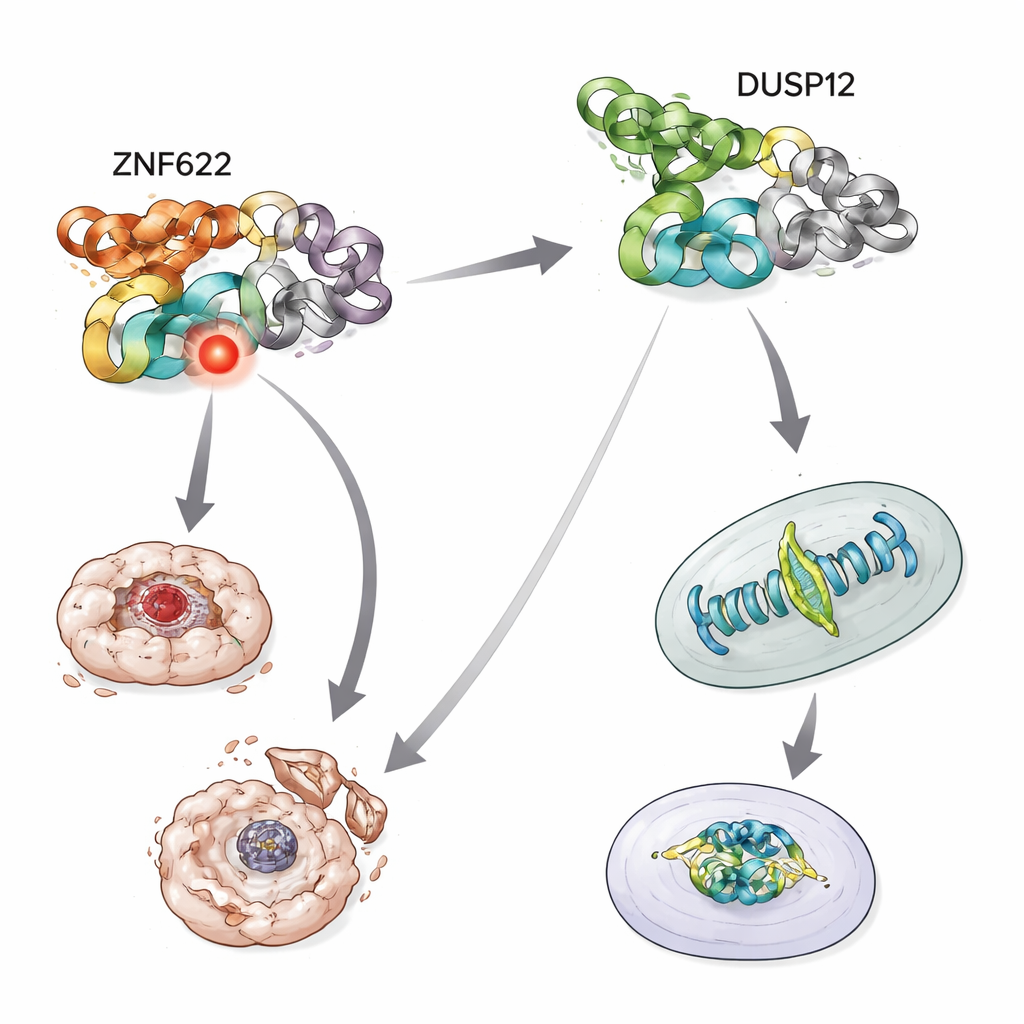
Balanceren tussen leven en dood onder stress
Het team onderzocht vervolgens wat er gebeurt wanneer cellen worden blootgesteld aan toxische stressoren, zoals chemotherapie middelen die kankercellen doorgaans naar zelfvernietiging duwen. Wanneer DUSP12 uitgeput was, werden cellen gevoeliger om te sterven als reactie op verschillende anti-kankermiddelen, met een hogere activiteit van enzymen die celdood uitvoeren. Daarentegen maakte het verminderen van ZNF622 cellen resistenter tegen sterven onder dezelfde behandelingen. Omgekeerd beschermde overproductie van DUSP12 cellen tegen deze stressoren, terwijl overproductie van ZNF622 de kans op celdood vergrootte. Toen beide tegelijk werden verhoogd, dempte DUSP12 het pro-dood effect van ZNF622, en het stapsgewijs verhogen van DUSP12 zette de celdood geleidelijk terug, zelfs in aanwezigheid van constante ZNF622. Dit dosisafhankelijke touwtrekken laat zien dat de twee eiwitten werken als tegengestelde knoppen op hetzelfde overlevingscircuit.
Wat dit betekent voor kanker en verder
Deze bevindingen schetsen DUSP12 als een cellulaire lijfwacht die ZNF622 bindt en de neiging ervan om de celdeling te ontsporen en celdood te veroorzaken, afremt, vooral onder medicijn-geïnduceerde stress. In kankers waar DUSP12 abnormaal hoog is, kan deze bescherming tumorcellen helpen chemotherapie te overleven, waardoor DUSP12 een aantrekkelijk doelwit is voor geneesmiddelen die dat schild willen wegnemen en kankercellen laten sterven. Omgekeerd, in situaties waar het bewaren van cellen cruciaal is — zoals het beschermen van de lever tijdens chirurgie of het vertragen van verlies van zenuwcellen bij degeneratieve ziekten — kan het versterken van DUSP12 of het dempen van ZNF622 weefsels helpen om beschadigende omstandigheden te weerstaan. Door te verduidelijken hoe deze twee eiwitten communiceren bij een sleutelbeslissing tussen leven en dood, biedt de studie een nieuwe mogelijkheid om het celfortuin te sturen in zowel kankertherapie als weefselbescherming.
Bronvermelding: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Trefwoorden: celcyclus, apoptose, weerstand tegen kankertherapie, eiwitfosfatase, stressrespons