Clear Sky Science · de
DUSP12 fördert den Zellzyklus und schützt Zellen vor ZNF622-vermittelter Apoptose
Warum Entscheidungen über Zellüberleben wichtig sind
Sekunde für Sekunde entscheiden unsere Zellen stillschweigend, ob sie weiterwachsen oder sich selbst zerstören sollen. Wenn dieses Gleichgewicht gestört ist, kann Krebs entstehen oder es können bei Verletzungen lebenswichtige Zellen verloren gehen. Diese Studie untersucht zwei wenig bekannte zelluläre „Schalter“, DUSP12 und ZNF622, die mitbestimmen, ob eine gestresste Zelle sich repariert und teilt oder stattdessen ein eingebautes Todesprogramm aktiviert. Zu verstehen, wie diese Schalter funktionieren, könnte neue Möglichkeiten eröffnen – sowohl um Krebszellen gezielt zu töten als auch um gesundes Gewebe vor Schaden zu schützen.
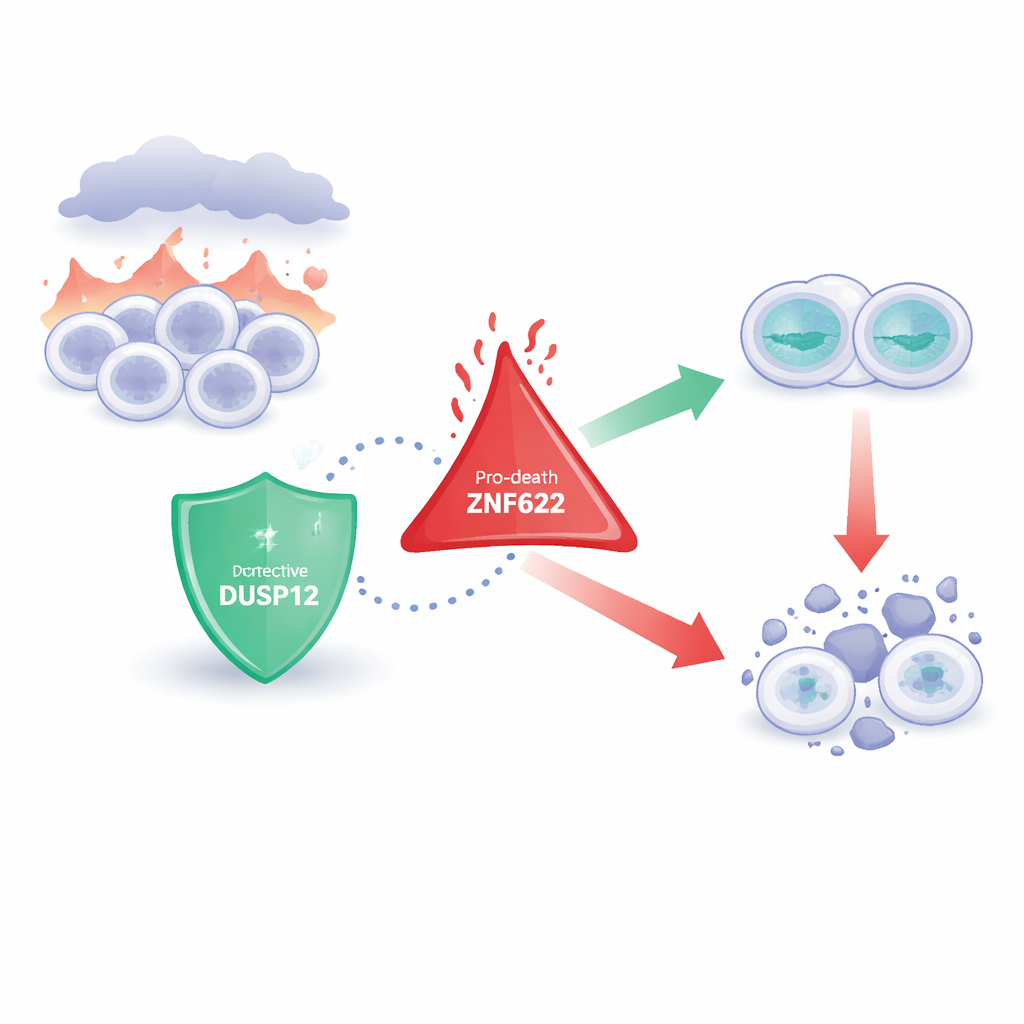
Zwei entgegengesetzte zelluläre Wächter
Die Forschenden konzentrieren sich auf eine Enzymfamilie, die winzige chemische Markierungen von Proteinen entfernt und damit ihr Verhalten subtil verändert. DUSP12 ist ein solches Enzym, dem man seit Langem einen Einfluss auf Zellwachstum und -überleben zuschreibt, das aber bislang wenig verstanden ist. ZNF622 hingegen ist ein Protein mit „fingerartigen“ Strukturen, die ihm erlauben, mit vielen Partnern zu interagieren; es wurde mit Zellwachstum, Stressantworten und besonders mit dem Auslösen von Zelltod in Verbindung gebracht. Frühere Arbeiten deuteten an, dass beide Moleküle in Krebs eine Rolle spielen, aber wie sie miteinander kommunizieren — und was das für das Schicksal einer Zelle bedeutet — war unbekannt.
Eine verborgene Partnerschaft finden
Um DUSP12-Partner aufzuspüren, nutzte das Team biochemische „Angel“-Methoden in menschlichen Zellen: DUSP12 wurde markiert, sodass jede daran haftende Proteinbegleitung herausgezogen und mittels Massenspektrometrie — einer Technik, die Proteinfragmente misst und katalogisiert — identifiziert werden konnte. In Zellen, die während der Teilung angehalten waren, tauchte ZNF622 wiederholt gemeinsam mit DUSP12 auf. Weitere Tests bestätigten, dass die beiden Proteine einen Komplex sowohl in Zellen als auch in vereinfachten Reagenzglaserien bilden. Die Strukturkartierung von DUSP12 zeigte, dass diese Partnerschaft von einer speziellen, metallbindenden Region an einem Ende von DUSP12 — der Zinkbindedomäne — abhängt, die als Andockstelle für ZNF622 fungiert.
Die Zellteilung im Takt halten
Die Zellteilung ist eine empfindliche Choreographie, bei der Chromosomen sich korrekt ausrichten und sauber trennen müssen. Reduzierten die Wissenschaftler DUSP12 in menschlichen Krebszellen, stockte die Teilung in mehr Zellen, Chromosomen waren fehl ausgerichtet, und die Dauer der Teilung verlängerte sich. Zellen sammelten sich auch in späten Stadien des Zellzyklus an, was darauf hindeutet, dass sie Probleme beim Fortschreiten hatten. Eine künstliche Erhöhung von ZNF622 führte ebenfalls zu gravierenden Teilungsstörungen, einschließlich verhedderter oder multipolarer Teilungsmaschinerie. Auffällig war, dass eine spezifische Stelle auf ZNF622 chemisch markiert oder unmarkiert sein konnte, und die Aktivität von DUSP12 verschob ZNF622 in Richtung der unmarkierten Form. Nur die normale, umkehrbare Version von ZNF622 — deren Markierung sich verändern konnte — verursachte starke Teilungsdefekte; feste „immer an“ oder „immer aus“ Nachahmungen taten das nicht. Das deutet darauf hin, dass DUSP12s Feineinstellung dieser einzelnen Stelle dazu beiträgt, die Zellteilung geordnet zu halten.
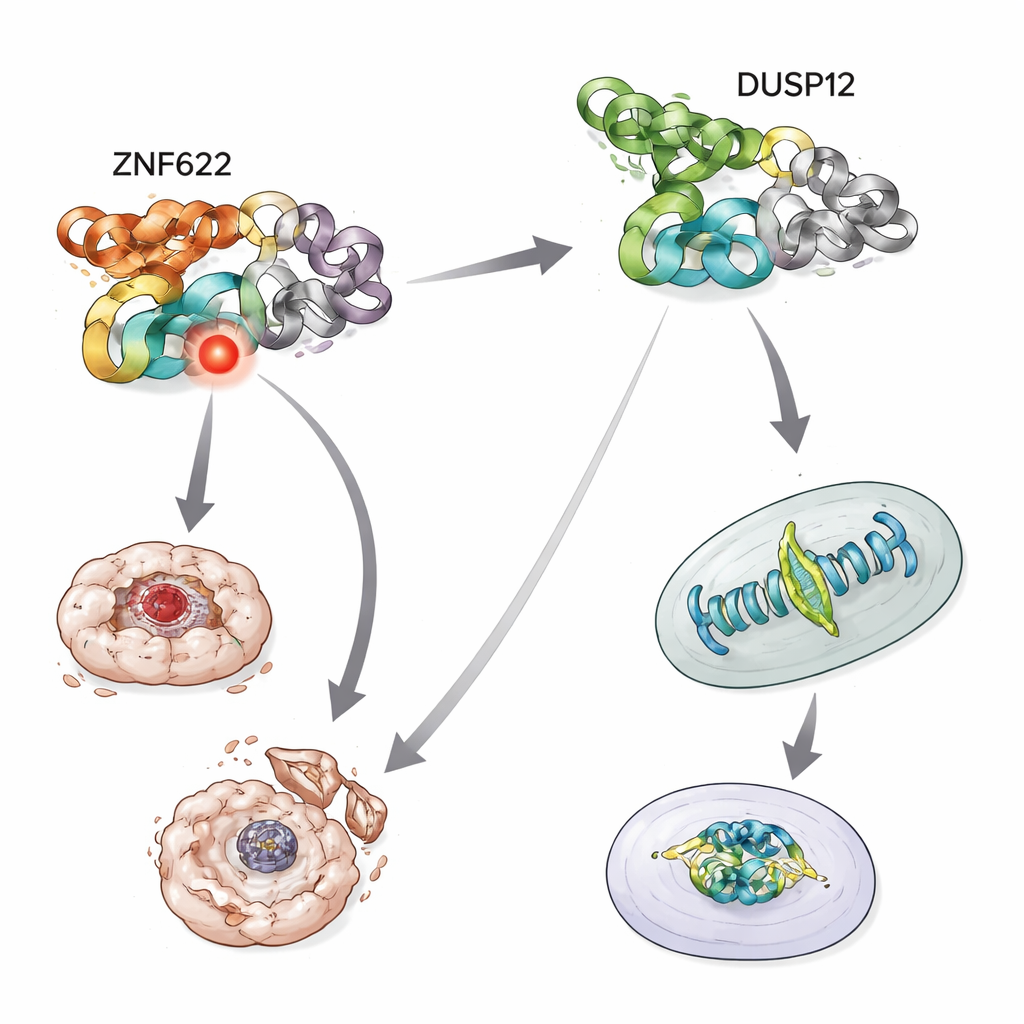
Leben und Tod im Stress austarieren
Anschließend untersuchte das Team, was passiert, wenn Zellen toxischen Stressfaktoren ausgesetzt werden, etwa Chemotherapeutika, die Krebszellen normalerweise zur Selbstzerstörung treiben. Bei DUSP12-Mangel wurden Zellen gegenüber mehreren Krebsmedikamenten anfälliger und zeigten eine höhere Aktivität von Enzymen, die den Zelltod ausführen. Im Gegensatz dazu machte die Reduktion von ZNF622 Zellen widerstandsfähiger gegenüber dem Absterben unter denselben Behandlungen. Umgekehrt schützte eine Überproduktion von DUSP12 Zellen vor diesen Stressoren, während eine Überproduktion von ZNF622 das Absterben wahrscheinlicher machte. Wenn beide Proteine gemeinsam erhöht wurden, schwächte DUSP12 den pro-apoptotischen Effekt von ZNF622 ab, und eine stufenweise Erhöhung von DUSP12 drosselte den Zelltod schrittweise, selbst bei konstant hohem ZNF622. Dieses mengenabhängige Tauziehen zeigt, dass die beiden Proteine als entgegengesetzte Regler desselben Überlebenskreises agieren.
Was das für Krebs und darüber hinaus bedeutet
Die Ergebnisse zeichnen DUSP12 als zellulären Bodyguard, der ZNF622 bindet und dessen Neigung bremst, die Zellteilung zu entgleisen und Zelltod auszulösen, besonders unter medikamentös induziertem Stress. In Tumoren mit ungewöhnlich hohem DUSP12 kann dieser Schutz Tumorzellen helfen, Chemotherapie zu überstehen, wodurch DUSP12 selbst zu einem attraktiven Ziel für Wirkstoffe werden könnte, die diesen Schutz aufheben und Krebszellen zugänglich für den Tod machen. Umgekehrt könnten in Situationen, in denen der Erhalt von Zellen entscheidend ist — etwa beim Schutz der Leber während einer Operation oder beim Verlangsamen des Verlusts von Nervenzellen bei degenerativen Erkrankungen — eine Stärkung von DUSP12 oder eine Dämpfung von ZNF622 Gewebe helfen, schädliche Bedingungen besser zu überstehen. Indem die Studie klärt, wie diese beiden Proteine an einem zentralen Entscheidungspunkt zwischen Leben und Tod miteinander kommunizieren, bietet sie einen neuen Ansatzpunkt, um das Schicksal von Zellen sowohl in der Krebstherapie als auch beim Gewebeschutz gezielt zu steuern.
Zitation: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Schlüsselwörter: Zellzyklus, Apoptose, Resistenz gegen Krebstherapie, Proteinphosphatase, Stressreaktion