Clear Sky Science · ar
تعزيز DUSP12 لتقدّم دورة الخلية وحماية الخلايا من الاستماتة المحرِّضة بواسطة ZNF622
لماذا تهمّ خيارات بقاء الخلية
تتخذ خلايانا، كل ثانية، قرارًا صامتًا بشأن الاستمرار في النمو أو الدخول في عملية الانتحار المبرمجة. عند اختلال هذا التوازن، قد تنشأ سرطانات أو تُفقد خلايا حيوية أثناء الإصابة. تستكشف هذه الدراسة مفاتيحين خلويين قليلَي الشهرة، يُدعَيان DUSP12 وZNF622، يساعدان على تقرير ما إذا كانت الخلية المضطربة ستُصلح نفسها وتنسخ، أم ستشغّل برنامج موت مُدمَج. فهم كيفية عمل هذين المفتاحين قد يفتح آفاقًا جديدة لقتل خلايا السرطان أو لحماية الأنسجة السليمة من الضرر.
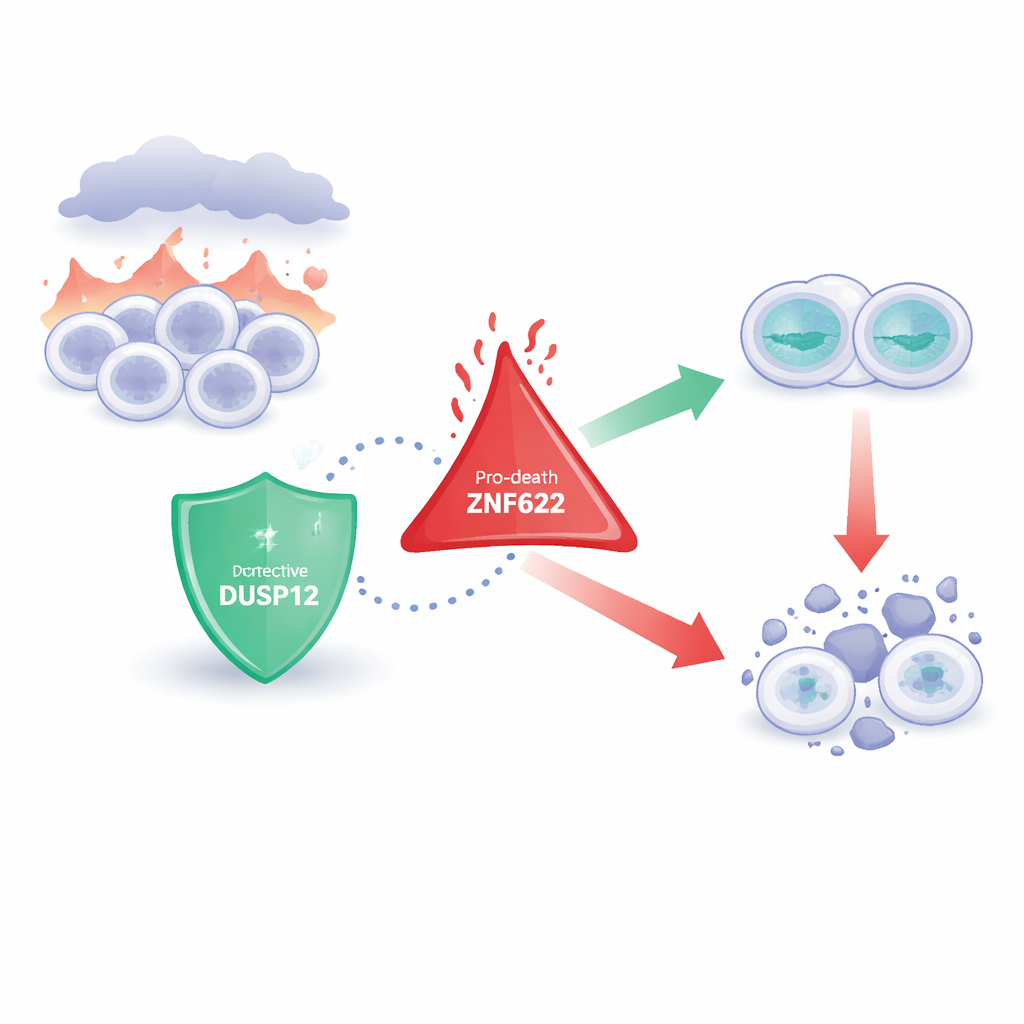
حارسان خلويان متعارضان
تركّز الباحثون على عائلة من الإنزيمات التي تزيل وسمات كيميائية دقيقة من البروتينات، ما يغيّر سلوك تلك البروتينات بطرق دقيقة. يعدُّ DUSP12 أحد هذه الإنزيمات، وقد وقع عليه الظن منذ زمن بأنه يؤثر في نمو وبقاء الخلية لكنه ظل قليل الفهم. وعلى النقيض، ZNF622 هو بروتين ذو هياكل «شبيهة بالأصابع» تساعده على التفاعل مع شركاء كثيرين، وقد رُبط بنمو الخلايا واستجابات الإجهاد، وبشكل خاص بتحفيز موت الخلية. أشارت أعمال سابقة إلى أهمية الجزيئين في السرطان، لكن كيف يتواصلان مع بعضهما—وماذا يعني ذلك لمصير الخلية—كان غير معروف.
اكتشاف شراكة مخفية
لكشف شركاء DUSP12، استخدم الفريق حيلًا بيوكيميائية في خلايا بشرية، حيث وُسِم DUSP12 بحيث يمكن سحب أي بروتينات تلتصق به وتحديدها عبر مطيافية الكتلة، وهي تقنية تزن وتفهرس شظايا البروتين. في خلايا متوقفة أثناء الانقسام، ظهر ZNF622 مرارًا إلى جانب DUSP12. وأكدت اختبارات إضافية أن البروتينين يشكلان مركبًا داخل الخلايا وفي أنظمة مبسطة في القصبة الزجاجية. بيّن تخطيط بنية DUSP12 أن هذه الشراكة تعتمد على منطقة خاصة لالتقاط معدن في أحد طرفي DUSP12—مجال ربط الزنك—الذي يعمل كموقع ارتكاز لZNF622.
الحفاظ على انتظام انقسام الخلية
الانقسام الخلوي هو رقص دقيق يجب أن تنصف فيه الكروموسومات وتنفصل بسلاسة. عندما قلّل العلماء مستويات DUSP12 في خلايا سرطانية بشرية، توقفت نسبة أكبر من الخلايا أثناء الانقسام وظهرت كروموسومات غير مصطفة، كما ازداد الزمن اللازم لإكمال الانقسام. تراكمت الخلايا أيضًا في المراحل المتأخرة من دورة الخلية، ما يشير إلى أنها كانت تكافح للتقدّم. عند تعزيز ZNF622 اصطناعيًا، ظهرت مشكلات انقسام حادة مجددًا، بما في ذلك آلات انقسام متشابكة أو متعددة الأقطاب. ومن المثير أن موقعًا محددًا على ZNF622 يمكن أن يكون إما موسومًا كيميائيًا أو غير موسوم، ونشاط DUSP12 أزاح ZNF622 نحو الشكل غير الموسوم. فقط النسخة الطبيعية من ZNF622، التي يمكن أن يتبدل وسمها ذهابًا وإيابًا، سببت عيوب انقسام قوية؛ بينما لم تفعل المحاكيات الثابتة «مشتعلة دائمًا» أو «مطفأة دائمًا» ذلك. هذا يشير إلى أن تعديل DUSP12 الدقيق لموقع واحد يساعد في إبقاء انقسام الخلية منظّمًا.
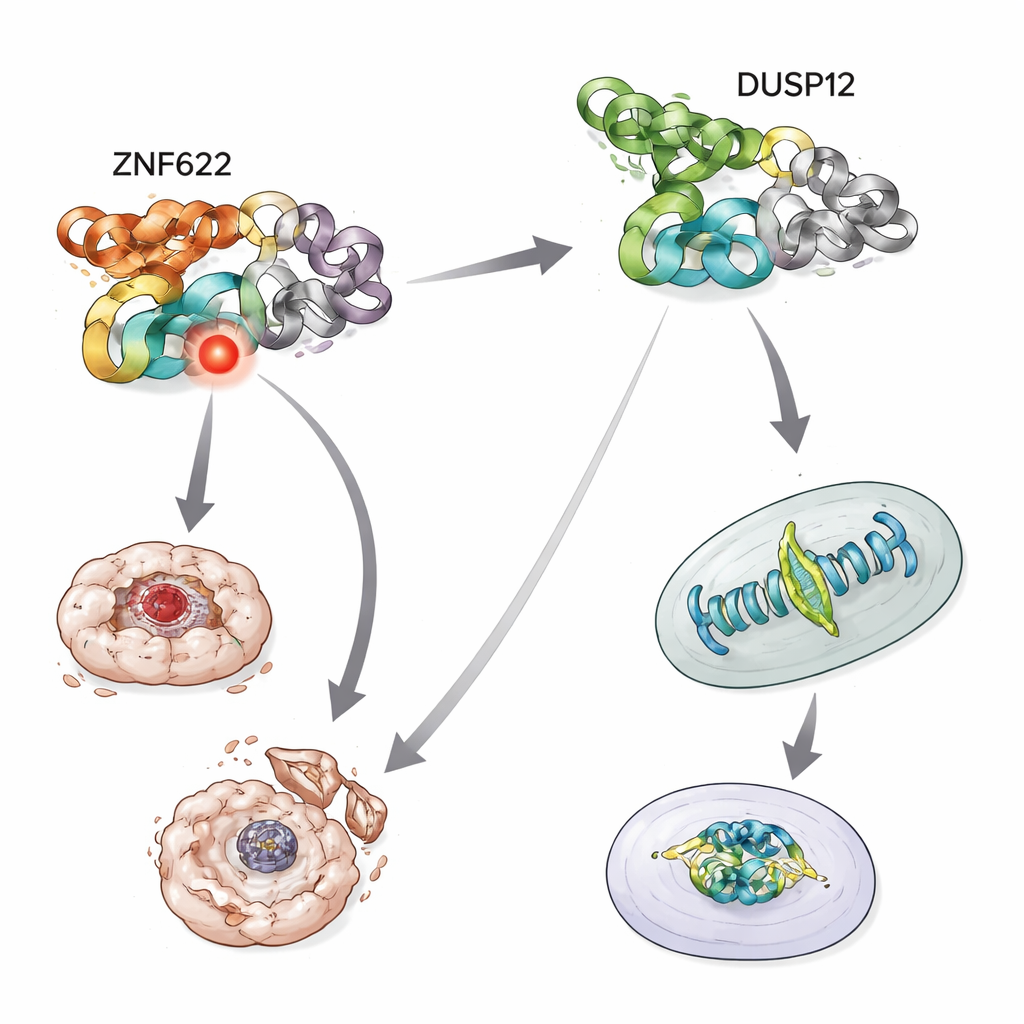
موازنة الحياة والموت تحت الضغط
سأل الفريق بعد ذلك ماذا يحدث عندما تتعرض الخلايا لإجهادات سامة، مثل أدوية العلاج الكيميائي التي تدفع خلايا السرطان عادة نحو الانتحار الخلوي. عندما أُرهق DUSP12، أصبحت الخلايا أكثر ميلاً للموت استجابةً لعدة عوامل مضادة للسرطان، مع زيادة نشاط الإنزيمات التي تنفّذ الموت الخلوي. وعلى النقيض، جعل خفض ZNF622 الخلايا أكثر مقاومة للموت تحت نفس المعالجات. وعند قلب التجربة، حما إنتاج DUSP12 المفرط الخلايا من هذه الضغوط، بينما جعل إنتاج ZNF622 المفرط الوفاة أكثر احتمالًا. عندما ارتفع كلاهما معًا، خفّف DUSP12 من تأثير ZNF622 المحفّز للموت، ومع زيادة DUSP12 تدريجيًا انخفضت نسبة الخلايا الميتة حتى في وجود ZNF622 المستمر. تُظهر هذه المواجهة المعتمِدة على المستوى أن البروتينين يعملان كأزرار متعارضة على نفس دائرة البقاء.
ماذا يعني هذا بالنسبة للسرطان وما وراءه
تصوِّر هذه النتائج DUSP12 كحارس خلوي يربط ZNF622 ويقيّ من ميله إلى تعطيل انقسام الخلية وتحفيز الموت، خصوصًا تحت ضغوط الأدوية. في السرطانات التي يكون فيها DUSP12 مرتفعًا بشكل غير طبيعي، قد تُساعد هذه الحماية خلايا الورم على النجاة من العلاج الكيميائي، مما يجعل DUSP12 هدفًا جذابًا لأدوية تهدف إلى نزع هذا الدرع وترك خلايا السرطان لتهاوى. وعلى العكس، في مواقف تكون فيها حماية الخلايا ضرورية—مثل حماية الكبد أثناء الجراحة أو إبطاء فقدان الخلايا العصبية في الأمراض التنكسية—قد يساعد تعزيز DUSP12 أو كبح ZNF622 الأنسجة على تحمل الظروف الضارة. من خلال توضيح كيفية تواصُل هذين البروتينين عند نقطة قرار محورية بين الحياة والموت، تقدم الدراسة مقبضًا جديدًا لضبط مصير الخلية سواء في علاج السرطان أو في حماية الأنسجة.
الاستشهاد: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
الكلمات المفتاحية: دورة الخلية, الاستماتة, مقاومة علاج السرطان, فوسفاتاز بروتيني, استجابة الإجهاد