Clear Sky Science · it
DUSP12 promuove la progressione del ciclo cellulare e protegge le cellule dall’apoptosi mediata da ZNF622
Perché le scelte di sopravvivenza cellulare contano
Ogni secondo, le nostre cellule decidono silenziosamente se continuare a crescere o autodistruggersi. Quando questo equilibrio viene disturbato, possono insorgere tumori oppure cellule vitali possono andare perse in seguito a lesioni. Questo studio esplora due “interruttori” cellulari poco noti, chiamati DUSP12 e ZNF622, che aiutano a determinare se una cellula sotto stress si ripara e si divide oppure attiva invece un programma di morte incorporato. Capire come funzionano questi interruttori potrebbe aprire nuove strade sia per uccidere le cellule tumorali sia per proteggere i tessuti sani dai danni.
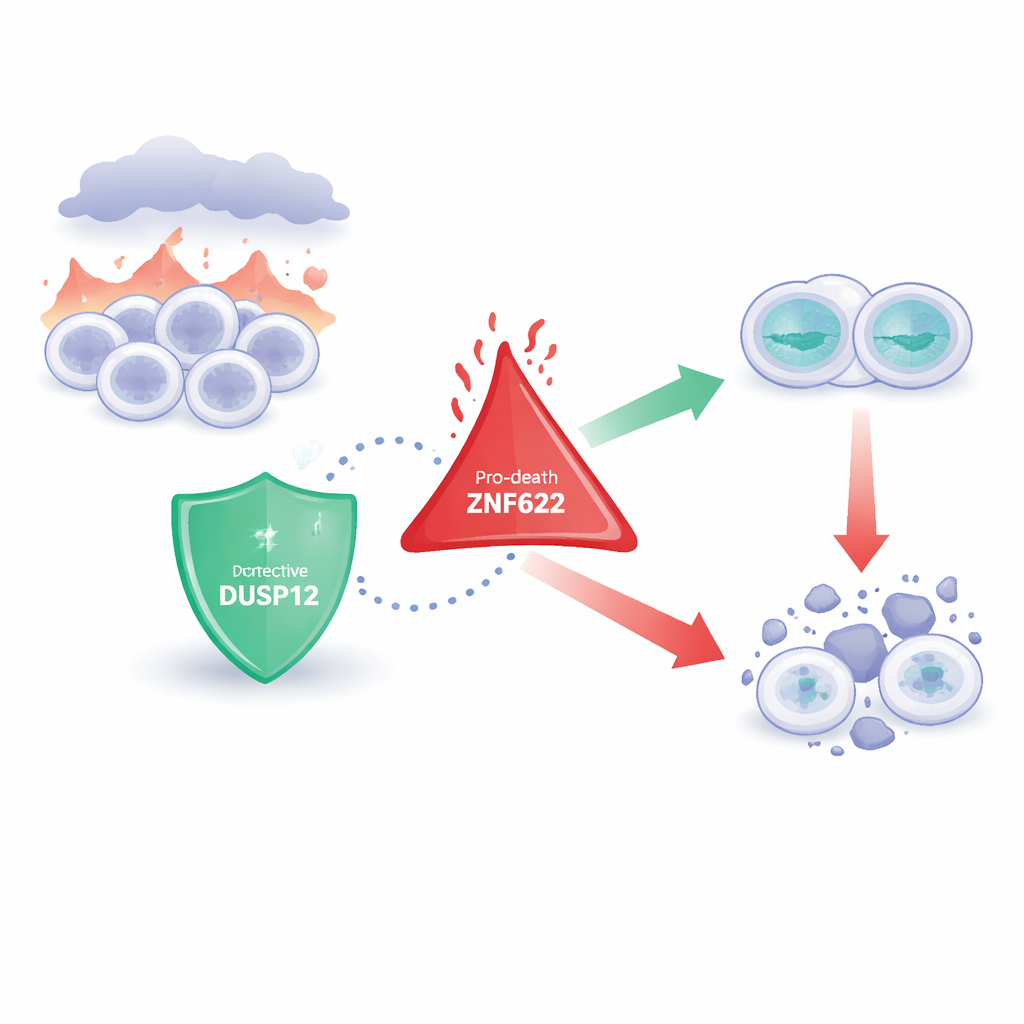
Due guardiani cellulari opposti
I ricercatori si concentrano su una famiglia di enzimi che rimuovono piccole etichette chimiche dalle proteine, modificando sottilmente il comportamento di quelle proteine. DUSP12 è uno di questi enzimi, da tempo sospettato di influenzare la crescita e la sopravvivenza cellulare ma ancora poco compreso. ZNF622, al contrario, è una proteina con strutture «a dita» che le permettono di interagire con molti partner ed è stata collegata alla crescita cellulare, alle risposte allo stress e in particolare all’attivazione della morte cellulare. Studi precedenti suggerivano che entrambe le molecole fossero importanti nel cancro, ma come potessero comunicare tra loro — e cosa ciò significasse per il destino della cellula — era sconosciuto.
Scoprire una partnership nascosta
Per identificare i partner di DUSP12, il gruppo ha usato stratagemmi biochimici nelle cellule umane, marcando DUSP12 in modo che le proteine che vi si legano potessero essere isolate e identificate mediante spettrometria di massa, una tecnica che pesa e cataloga i frammenti proteici. Nelle cellule bloccate durante la divisione, ZNF622 è apparso ripetutamente in associazione con DUSP12. Test successivi hanno confermato che le due proteine formano un complesso sia all’interno delle cellule sia in sistemi semplificati in provetta. La mappatura della struttura di DUSP12 ha mostrato che questa associazione dipende da una regione speciale che cattura metalli a un’estremità di DUSP12 — il dominio legante lo zinco — che funge da sito di ancoraggio per ZNF622.
Mantenere ordinata la divisione cellulare
La divisione cellulare è una coreografia delicata in cui i cromosomi devono allinearsi e separarsi in modo pulito. Quando gli scienziati hanno ridotto i livelli di DUSP12 in cellule tumorali umane, più cellule si sono bloccate durante la divisione e hanno mostrato cromosomi disallineati, e il tempo necessario per completare la divisione è aumentato. Le cellule si sono anche accumulate nelle fasi tardive del ciclo cellulare, suggerendo difficoltà nel progredire. Quando ZNF622 è stato aumentato artificialmente, le cellule hanno nuovamente sviluppato gravi problemi di divisione, compresi apparati divisionali aggrovigliati o multipolari. È interessante che un sito specifico su ZNF622 potesse essere sia marcato chimicamente sia non marcato, e l’attività di DUSP12 spostava ZNF622 verso la forma non marcata. Solo la versione normale di ZNF622, il cui marchio poteva cambiare avanti e indietro, ha provocato gravi difetti di divisione; i mimetici bloccati in una condizione «sempre attiva» o «sempre inattiva» non lo hanno fatto. Ciò indica che la fine regolazione di questo singolo sito da parte di DUSP12 aiuta a mantenere ordinata la divisione cellulare.
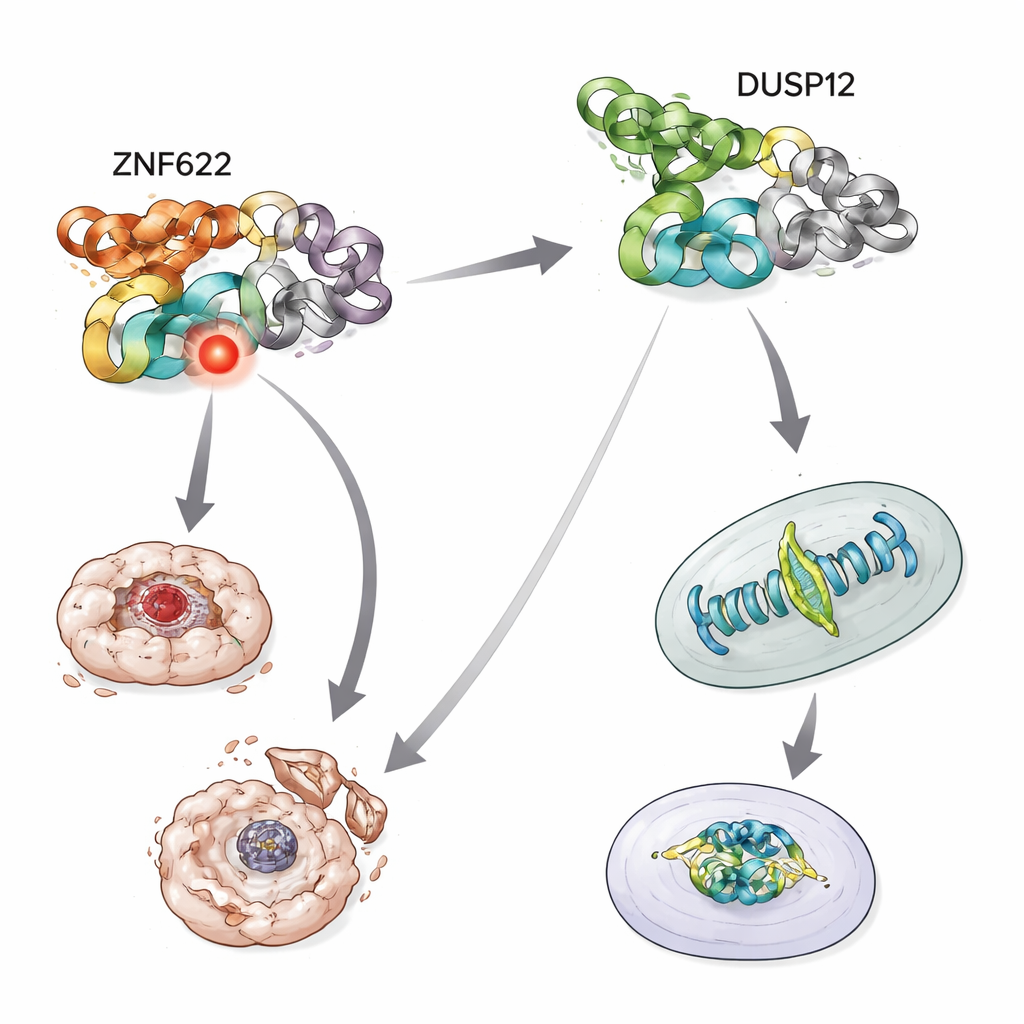
Equilibrare vita e morte sotto stress
Il gruppo ha poi indagato cosa accade quando le cellule vengono esposte a stress tossici, come i farmaci chemioterapici che solitamente spingono le cellule tumorali verso l’autodistruzione. Quando DUSP12 è stato depletato, le cellule sono diventate più propense a morire in risposta a diversi agenti anticancro, mostrando una maggiore attività di enzimi che eseguono la morte cellulare. Al contrario, ridurre ZNF622 ha reso le cellule più resistenti alla morte sotto gli stessi trattamenti. Ribaltando l’esperimento, la sovrapproduzione di DUSP12 ha protetto le cellule da questi stress, mentre la sovrapproduzione di ZNF622 ha reso la morte più probabile. Quando entrambi sono stati aumentati insieme, DUSP12 ha attenuato l’effetto pro‑morte di ZNF622, e aumentare DUSP12 in modo graduale ha progressivamente ridotto la morte cellulare anche in presenza di ZNF622 costante. Questa competizione dipendente dalla dose mostra che le due proteine agiscono come manopole opposte sullo stesso circuito di sopravvivenza.
Cosa significa per il cancro e oltre
Questi risultati dipingono DUSP12 come una guardia del corpo cellulare che si lega a ZNF622 e frena la sua tendenza a mandare in tilt la divisione cellulare e a innescare la morte, specialmente sotto stress indotto dai farmaci. Nei tumori in cui DUSP12 è anormalmente elevato, questa protezione potrebbe aiutare le cellule tumorali a sopravvivere alla chemioterapia, rendendo DUSP12 un bersaglio interessante per farmaci progettati per rimuovere questo scudo e permettere la morte delle cellule tumorali. Al contrario, in situazioni in cui preservare le cellule è cruciale — come proteggere il fegato durante un intervento chirurgico o rallentare la perdita dei neuroni nelle malattie degenerative — potenziare DUSP12 o attenuare ZNF622 potrebbe aiutare i tessuti a resistere a condizioni dannose. Chiarendo come queste due proteine comunichino in un punto decisionale chiave tra vita e morte, lo studio offre una nuova leva per regolare il destino cellulare sia nella terapia del cancro sia nella protezione dei tessuti.
Citazione: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Parole chiave: ciclo cellulare, apoptosi, resistenza alla terapia del cancro, fosfatasi proteica, risposta allo stress