Clear Sky Science · pl
DUSP12 sprzyja postępowi cyklu komórkowego i chroni komórki przed apoptozą wywołaną przez ZNF622
Dlaczego wybory dotyczące przeżycia komórek mają znaczenie
Co sekundę nasze komórki w ciszy decydują, czy dalej rosnąć, czy uruchomić samobójczy program. Gdy ta równowaga zostaje zachwiana, może pojawić się rak albo podczas urazu tracimy komórki niezbędne do ratowania organizmu. W tym badaniu przeanalizowano dwie mało poznane „przełączniki” komórkowe, DUSP12 i ZNF622, które wpływają na to, czy komórka poddana stresowi naprawia się i dzieli, czy uruchamia wbudowany program śmierci. Zrozumienie działania tych przełączników może otworzyć nowe możliwości zarówno w zabijaniu komórek nowotworowych, jak i w ochronie zdrowych tkanek przed uszkodzeniem.
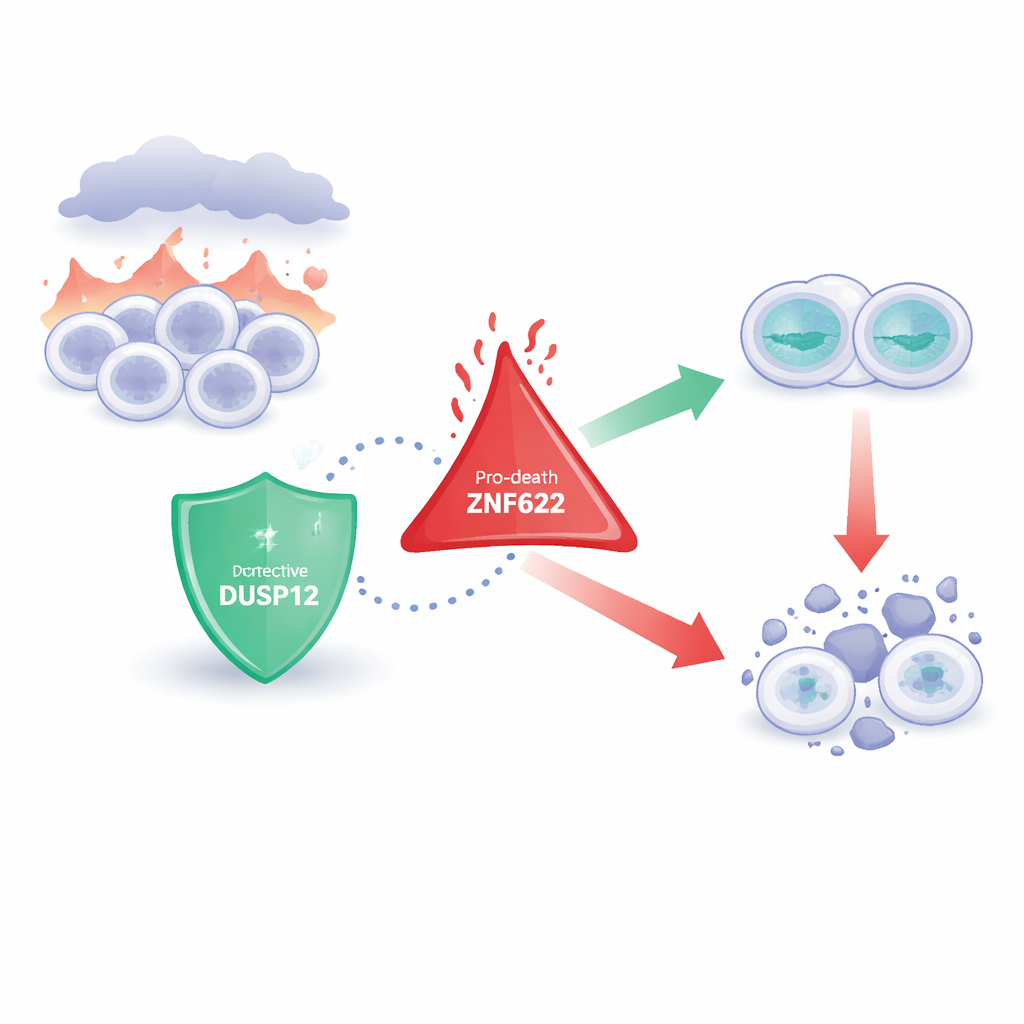
Dwie przeciwstawne straże komórkowe
Naukowcy skupili się na rodzinie enzymów usuwających drobne chemiczne znaczniki z białek, co subtelnie zmienia ich funkcję. DUSP12 jest jednym z takich enzymów, od dawna podejrzewanym o wpływ na wzrost i przeżycie komórek, ale słabo poznanym. Z kolei ZNF622 to białko z „palcowatymi” domenami ułatwiającymi interakcje z wieloma partnerami; powiązano je z wzrostem komórek, reakcjami na stres i w szczególności z uruchamianiem śmierci komórkowej. Wcześniejsze prace sugerowały rolę obu cząsteczek w nowotworach, jednak nie wiadomo było, czy i jak ze sobą współpracują — i co to oznacza dla losu komórki.
Odnalezienie ukrytego partnerstwa
Aby odnaleźć partnerów DUSP12, zespół zastosował biochemiczne „metody na ryby” w komórkach ludzkich: znakowano DUSP12, żeby wyławiać białka do niego przyczepione i identyfikować je za pomocą spektrometrii mas, techniki ważącej i katalogującej fragmenty białek. W komórkach zatrzymanych w trakcie podziału ZNF622 wielokrotnie pojawiało się razem z DUSP12. Dalsze testy potwierdziły, że oba białka tworzą kompleks zarówno wewnątrz komórek, jak i w uproszczonych systemach in vitro. Mapowanie struktury DUSP12 wykazało, że to partnerstwo zależy od specjalnego regionu chwytającego metal na jednym końcu DUSP12 — domeny wiążącej cynk — która działa jako miejsce dokowania dla ZNF622.
Utrzymanie porządku podczas podziału komórkowego
Podział komórkowy to delikatna choreografia, w której chromosomy muszą się poprawnie ustawić i oddzielić. Gdy naukowcy zmniejszyli poziom DUSP12 w ludzkich komórkach nowotworowych, więcej komórek zatrzymywało się podczas podziału i wykazywało nieprawidłowo ustawione chromosomy, a czas potrzebny do zakończenia podziału się wydłużył. Komórki gromadziły się także w późnych etapach cyklu komórkowego, co sugeruje trudności z jego postępem. Sztuczne zwiększenie poziomu ZNF622 wywołało ponownie poważne problemy z podziałem, w tym splątane lub wielobiegunowe struktury rozdzielające. Co ciekawe, określone miejsce na ZNF622 mogło być chemicznie oznaczone lub nie, a aktywność DUSP12 przesuwała ZNF622 w stronę formy nieoznakowanej. Tylko normalna wersja ZNF622, której znacznik mógł się odwracać, powodowała silne defekty podziału; stałe wersje „zawsze włączone” lub „zawsze wyłączone” tego efektu nie wywoływały. To wskazuje, że drobne dostrajanie przez DUSP12 jednego miejsca pomaga utrzymać porządek podczas podziału komórkowego.
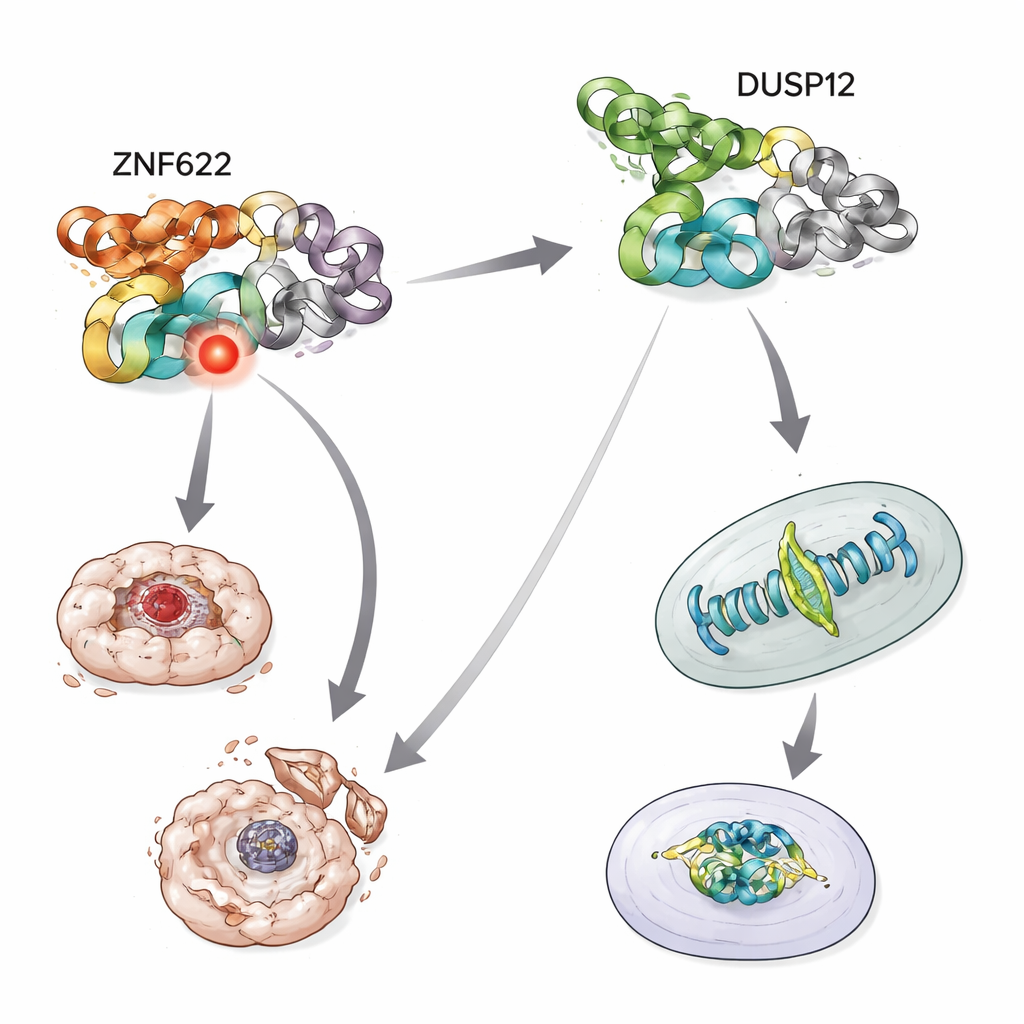
Równoważenie życia i śmierci w warunkach stresu
Zespół sprawdził następnie, co się dzieje, gdy komórki są wystawione na toksyczne stresy, takie jak leki chemioterapeutyczne, które zwykle popychają komórki nowotworowe w stronę samozniszczenia. Po wyczerpaniu DUSP12 komórki stawały się bardziej skłonne do umierania w odpowiedzi na kilka leków przeciwnowotworowych, wykazując wyższą aktywność enzymów wykonujących śmierć komórkową. W przeciwieństwie do tego, zmniejszenie ZNF622 uczyniło komórki bardziej opornymi na śmierć pod tymi samymi terapiami. Odwracając układ, nadprodukcja DUSP12 chroniła komórki przed tymi stresami, podczas gdy nadprodukcja ZNF622 zwiększała prawdopodobieństwo zgonu. Gdy oba białka zwiększono jednocześnie, DUSP12 osłabiło pro-śmiercionośny efekt ZNF622, a stopniowe zwiększanie DUSP12 coraz bardziej tłumiło śmierć komórek nawet w obecności stałego poziomu ZNF622. Ten zależny od dawki pojedynek ukazuje, że oba białka działają jak przeciwstawne regulatory tej samej ścieżki przeżycia.
Co to oznacza dla nowotworów i nie tylko
Wyniki przedstawiają DUSP12 jako komórkowego ochroniarza, który wiąże ZNF622 i hamuje jego skłonność do zaburzania podziału komórek i wywoływania śmierci, szczególnie pod wpływem leków. W nowotworach, w których DUSP12 jest nieprawidłowo podwyższone, ta ochrona może pomagać komórkom guza przetrwać chemioterapię, co czyni DUSP12 atrakcyjnym celem dla leków mających usunąć tę tarczę i umożliwić śmierć komórek nowotworowych. Odwrotnie, w sytuacjach, w których zachowanie komórek jest kluczowe — na przykład ochrona wątroby podczas zabiegu chirurgicznego lub spowolnienie utraty komórek nerwowych w chorobach zwyrodnieniowych — zwiększenie DUSP12 lub stłumienie ZNF622 może pomóc tkankom przetrwać szkodliwe warunki. Poprzez wyjaśnienie, jak te dwa białka rozmawiają w kluczowym punkcie decyzyjnym między życiem a śmiercią, badanie daje nowy punkt uchwytu do regulacji losu komórek zarówno w terapii przeciwnowotworowej, jak i ochronie tkanek.
Cytowanie: Abdusamad, M., Guo, X., Ramirez, I. et al. DUSP12 promotes cell cycle progression and protects cells from ZNF622 mediated apoptosis. Cell Death Dis 17, 315 (2026). https://doi.org/10.1038/s41419-026-08618-z
Słowa kluczowe: cykl komórkowy, apoptoza, oporność na terapię przeciwnowotworową, fosfataza białkowa, odpowiedź na stres