Clear Sky Science · sv
Småmolekylskanning identifierar cytotoxiska hämmare av ER‑associerad nedbrytning i multipelt myelom
Att göra en svaghet hos cancerceller till ett nytt mål
Multipelt myelom är en blodcancer som uppstår i plasmaceller, kroppens antikroppsfabriker. Dessa celler producerar ständigt proteiner, vilket gör dem ovanligt beroende av ett internt kvalitetskontrollsystem som upptäcker och förstör felveckade proteiner. Denna studie undersöker om den inneboende sårbarheten kan utnyttjas med en småmolekylär drog för att döda myelomceller, inklusive sådana som slutat svara på befintlig behandling.
En dold städpatrull inne i överansträngda cancerceller
Inuti varje cell fungerar det endoplasmatiska nätverket som ett monteringsband för proteiner. När proteiner bildas felaktigt märks de för borttagning av en process kallad ER‑associerad nedbrytning, eller ERAD, och skickas till cellens avfalls‑ och återvinningssystem. Myelomceller, som tillverkar enorma mängder antikroppar, är starkt beroende av ERAD för att överleva. Befintliga läkemedel, så kallade proteasominhibitorer, blockerar det sista steget i detta avfallssystem och har förbättrat överlevnaden hos patienter, men de flesta tumörer utvecklar så småningom resistens. Forskarna sökte därför efter läkemedel som slår tidigare i städprocessen, direkt på ERAD, i hopp om att kunna stänga ner myelomceller på ett annat sätt.
Skanning av gamla läkemedel för ett nytt syfte
Teamet utvecklade ett cellbaserat test som rapporterar hur snabbt ett modell‑"dåligt" protein bryts ned av ERAD. Med detta assay skannade de cirka 2 200 befintliga föreningar från ett FDA‑bibliotek för omplacering av läkemedel. Bland flera kandidater identifierade de omaveloxolon (också känt som RTA408), ett läkemedel redan godkänt för en sällsynt neurologisk sjukdom, som en potent hämmare av ERAD. RTA408 försenade nedbrytningen av flera proteiner som normalt är beroende av ERAD, både lösliga proteiner i den intracellulära kompartmenten och membranbundna proteiner. Samtidigt lämnades många viktiga fria (cytosoliska) proteiner relativt opåverkade och cellens huvudsakliga avfallshanteringsmaskineri stördes inte i större utsträckning, vilket tyder på en riktad verkan på ER:s kvalitetskontroll istället för en generell nedstängning av proteinomsättningen.
Snabb, selektiv död av myelomceller
När forskarna behandlade en panel av myelomcellinjer med RTA408 sjönk cellöverlevnaden kraftigt inom några timmar vid låga läkemedelskoncentrationer, oberoende av om cellerna var känsliga eller resistenta mot proteasominhibitorer. En närbesläktad förening, RTA402, visade liknande effekter. Viktigt är att drogens förmåga att döda cancerceller inte berodde på dess kända roll i att förstärka en antioxidantregulator kallad NRF2, vilket antyder en tidigare okänd verkningsmekanism. I celler från patienter utplånade RTA408 effektivt maligna plasmaceller från både nyupptäckta och tungt förbehandlade individer, samtidigt som majoriteten av T‑celler och myeloida celler sparades och normala B‑celler påverkades endast måttligt. Hos möss med mänskliga myelomtumörer bromsade upprepad dosering med RTA408 tydligt eller förhindrade tumörtillväxt, vilket stöder dess potential som terapi i verkliga världen.
En oväntad väg till celldöd
Eftersom blockering av ERAD förväntas orsaka protein‑"trafikstockningar" och stress inne i cellen antog många forskare att den följande celldöden skulle drivas av en välkänd stressväg kallad den ofullständigt vikta proteinresponsen. Författarna bekräftade att denna stressrespons aktiverades efter RTA408‑behandling, men noggranna experiment visade att den inte var den huvudsakliga drivkraften bakom den snabba vågen av celldöd. Istället aktiverade läkemedlet snabbt en annan väg: den så kallade extrinsiska dödsvägen, som normalt svarar på farosignaler vid cellytan. RTA408 slog snabbt på ett enzym kallat caspas‑8 och dess efterföljande partners, och att blockera dessa enzymer kemiskt eller genom att ta bort viktiga adaptorproteiner (FADD och RIPK1) skyddade cellerna från att dö. Förvånande nog räddade inte borttagning av enskilda dödsreceptorer på cellytan cellerna, vilket pekar på en mer global störning i hur dessa receptorer är organiserade.
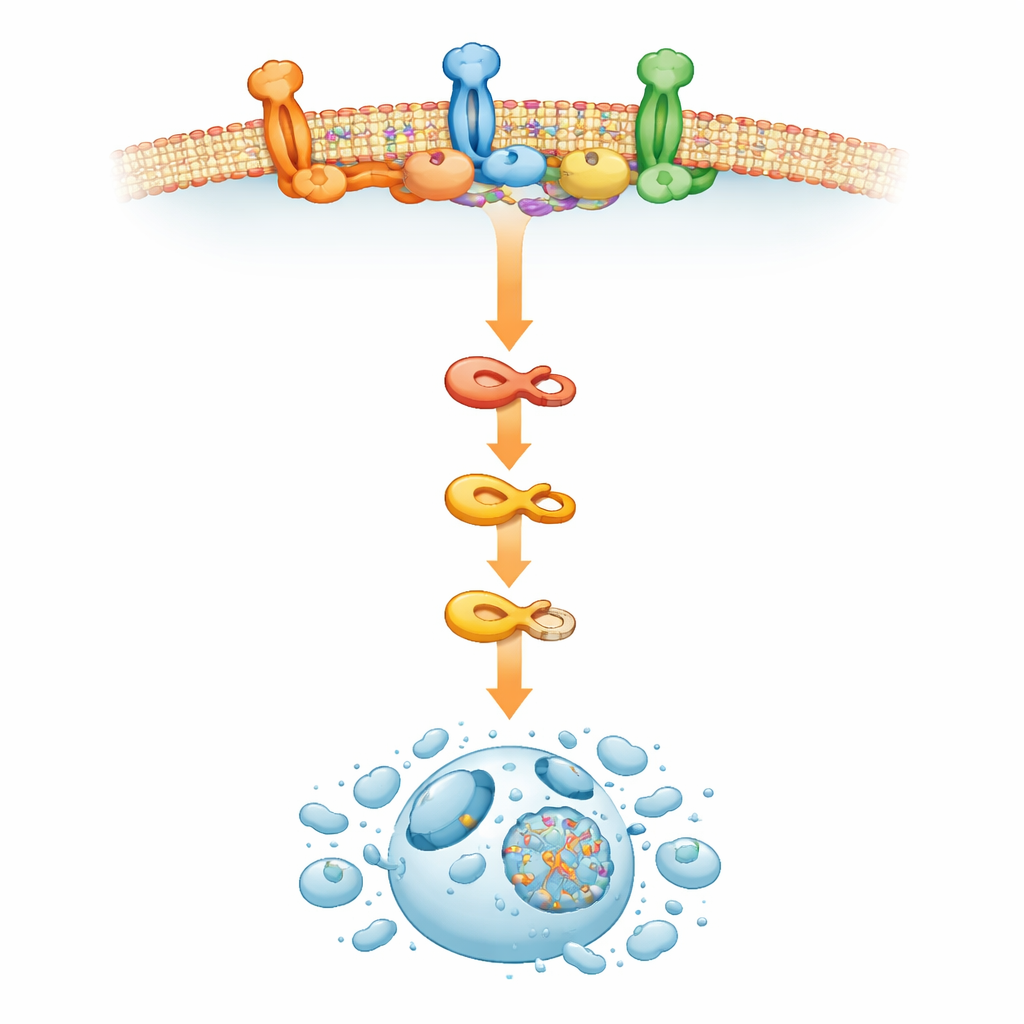
Hur cellmembranets "öar" tippar cellerna över kanten
För att förstå vad som drev denna ovanliga aktivering av dödsmaskineriet vände sig teamet till cellens yttre membran. Där fungerar specialiserade kolesterolrika områden, kända som lipidraftar, som små signalbearbetande plattformar. Studien fann att ERAD‑hämning med RTA408 omformade dessa raftar, vilket ledde till en ackumulering av raftmarkörer och främjade monteringen av den dödsinducerande signaleringskomplexet som aktiverar caspas‑8. När forskarna störde lipidraftarna eller blockerade kolesterolproduktionen kunde RTA408 inte längre utlösa tidig celldöd, även om tecken på intern stress i cellen kvarstod. Detta tyder på att störning av ERAD i myelomceller sätter igång vågor som omorganiserar membranet och för samman komponenter i dödsvägen på ett sätt som får cancercellen att självförstöra.
Vad detta kan betyda för patienter
Enkelt uttryckt identifierar detta arbete ett godkänt läkemedel som selektivt sabotera ett avgörande hushållssystem i myelomceller och driver dem mot en form av programmerad död som beror på hur proteiner och lipider är ordnade i deras yttre membran. Eftersom RTA408 fungerar annorlunda än nuvarande proteasomhämmande läkemedel och förblir effektivt i resistenta celler och i djurmodeller erbjuder det en lovande ny vinkel för behandling av denna fortfarande obotliga cancer. Samtidigt avslöjar studien en oväntad koppling mellan cellens interna kvalitetskontroll och organiseringen av ytliga "dödsomkopplare", vilket öppnar nya vägar för att designa terapier som utnyttjar de unika påfrestningar som antikroppsproducerande cancerceller utsätts för.
Citering: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
Nyckelord: multipelt myelom, protein‑kvalitetskontroll, ER‑associerad nedbrytning, caspas‑8‑apoptos, läkemedelsomplacering