Clear Sky Science · ja
小分子スクリーニングにより、多発性骨髄腫における細胞毒性を示す小胞体関連分解(ERAD)阻害剤を同定
がん細胞の弱点を新たな標的に変える
多発性骨髄腫は抗体を大量に産生する形質細胞に由来する血液のがんです。これらの細胞は常にタンパク質を大量に合成しているため、誤って折りたたまれたタンパク質を発見して除去する内部の品質管理システムに異常に依存しています。本研究は、その内在する脆弱性を小分子薬で利用して、現在の治療に反応しなくなった細胞を含む骨髄腫細胞を死滅させられるかどうかを調べています。
過労状態のがん細胞内にある隠れた清掃部隊
すべての細胞内で小胞体はタンパク質の組み立てラインとして機能します。タンパク質が誤って作られたとき、小胞体関連分解(ERAD)と呼ばれるプロセスがそれらを識別して廃棄のために細胞の処理機構へ送ります。大量の抗体タンパク質を産生する骨髄腫細胞は、生存のためにERADに強く依存しています。既存のプロテアソーム阻害剤はこの廃棄システムの最終段階を阻害し、患者の生存率を改善しましたが、多くの腫瘍は最終的に耐性を獲得します。したがって、研究者たちは清掃プロセスのより早い段階、すなわちERAD自体を直接標的にする薬剤を見つけ、骨髄腫細胞を別の方法で閉塞させられるかを探りました。
既存薬を新たな目的でスクリーニング
チームは、モデルとなる「不良」タンパク質がERADによってどれだけ速く分解されるかを報告する細胞ベースのアッセイを構築しました。このアッセイを用いて、FDAのリポジショニングライブラリから約2,200の既存化合物をスクリーニングしました。いくつかの候補の中で、まれな神経疾患で既に承認されているオマベロキソロン(別名RTA408)がERADの強力な阻害剤として同定されました。RTA408は通常ERADに依存する複数のタンパク質の分解を遅らせ、細胞区画内を浮遊するタンパク質や膜に埋め込まれたタンパク質の両方に影響しました。一方で、多くの主要な細胞質内の遊離タンパク質は比較的保たれ、細胞の主要なゴミ処理機構であるプロテアソームを大きく攪乱することはなく、タンパク質ターンオーバーの全般的な停止ではなく小胞体のタンパク質品質管理系に焦点を当てた作用を示していました。
迅速かつ選択的な骨髄腫細胞の死滅
研究者たちがRTA408で複数の骨髄腫細胞株を処理すると、薬物濃度が低くても数時間以内に細胞生存率が急激に低下しました。これはプロテアソーム阻害剤に対して感受性か耐性かに関係ありませんでした。関連化合物のRTA402も同様の効果を示しました。重要な点として、がん細胞を死滅させる薬剤の能力は、抗酸化調節因子NRF2を活性化するという既知の作用に依存しておらず、これまで認識されていなかった作用機序を示唆します。患者由来の細胞では、RTA408は新規診断例でも多剤既治療例でも悪性形質細胞を効率的に除去し、ほとんどのT細胞や骨髄系細胞は温存され、正常B細胞には中等度の影響しか与えませんでした。ヒト骨髄腫腫瘍を移植したマウスでは、RTA408の反復投与が腫瘍成長を著しく遅延または抑制し、実臨床での治療可能性を支持しました。
予想外の細胞死への経路
ERADを阻害するとタンパク質の“交通渋滞”や細胞内ストレスが生じると考えられており、多くの研究者はそれに続く細胞死が折りたたみ異常タンパク質応答(UPR)と呼ばれる良く知られたストレス経路によって駆動されるだろうと想定していました。著者らはRTA408処理後にこのストレス応答が確かにオンになることを確認しましたが、慎重な実験によりそれが迅速な細胞死の主な引き金ではないことが示されました。代わりに、薬剤は速やかに別の経路を作動させました:外因性(extrinsic)死経路で、通常は細胞表面の危険信号に応答します。RTA408は迅速にカスパーゼ‑8とその下流のパートナーを活性化し、これらの酵素を化学的に阻害するか主要なアダプタータンパク質(FADDおよびRIPK1)を欠失させると細胞死は防がれました。驚いたことに、個々の細胞表面の死受容体を除去しても細胞は救われず、これら受容体の配置がより広範に乱れていることを示唆しています。
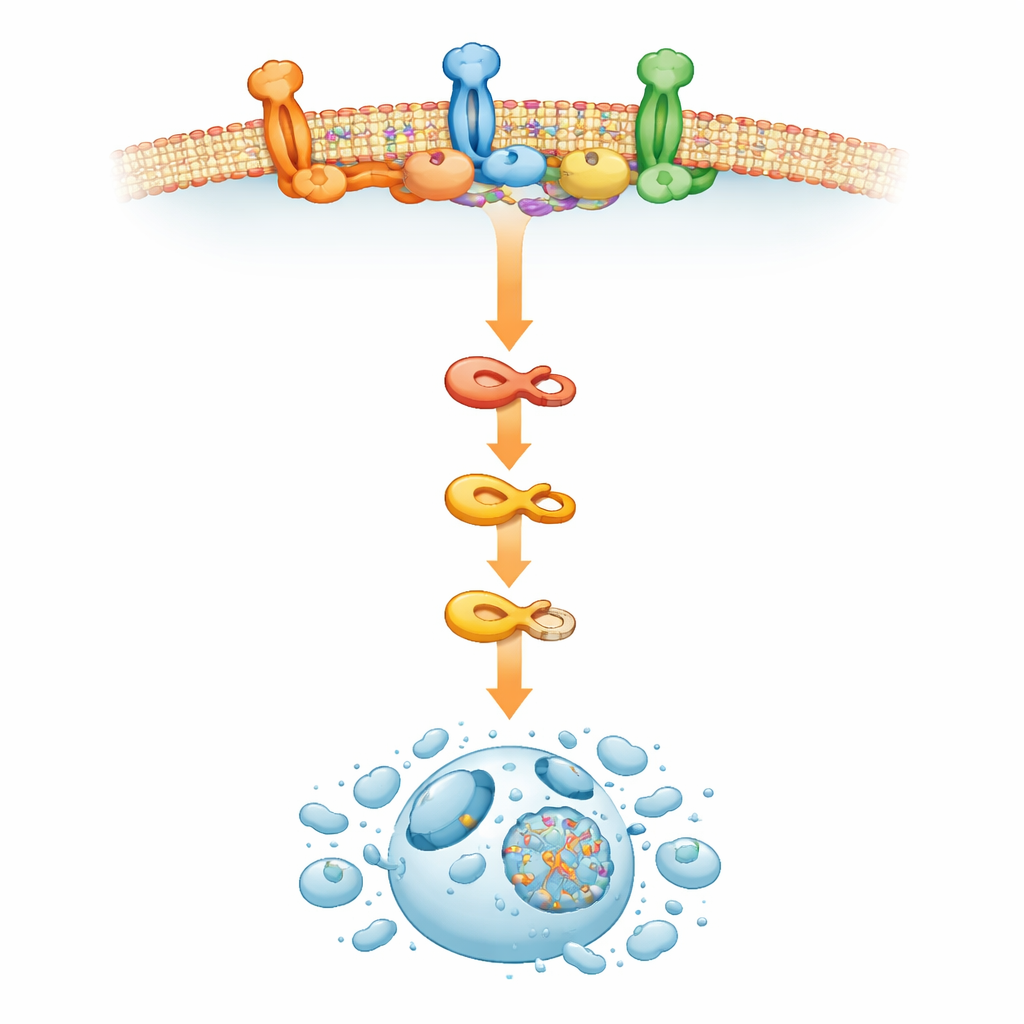
細胞膜の“島”が細胞を瀬戸際に追い込む仕組み
この異常な死の機構の活性化を駆動しているものを理解するために、チームは細胞の外膜に注目しました。そこではコレステロールを豊富に含む特殊なパッチ、いわゆるリピッドラフトが小さなシグナル処理プラットフォームとして機能します。研究は、RTA408によるERAD阻害がこれらのラフトを再構築し、ラフトマーカーの蓄積を引き起こし、カスパーゼ‑8を活性化する死誘導シグナリング複合体の組み立てを促進することを明らかにしました。研究者たちがリピッドラフトを破壊するかコレステロール産生を阻害すると、細胞内に残るストレスの兆候があってもRTA408は早期の細胞死を引き起こせなくなりました。これは、骨髄腫細胞ではERADの撹乱が膜を再編成する波紋を送り、死経路構成要素を集合させてがん細胞を自己破壊へと導くことを示しています。
患者への意味
端的に言えば、本研究は承認済み薬剤が骨髄腫細胞の重要なハウスキーピングシステムを選択的に攪乱し、外膜におけるタンパク質と脂質の配置に依存する形のプログラム細胞死へと押し進めることを示しています。RTA408は現在のプロテアソーム阻害薬とは異なる作用を持ち、耐性細胞や動物モデルでも有効性を保つため、この未だ根治困難ながんに対する有望な新たな治療角度を提供します。同時に、本研究は細胞内の品質管理機構と表面の“死スイッチ”の配置との間に予想外の連関を明らかにし、抗体産生がん細胞が直面する特有のストレスを利用する治療設計の新たな道を開きます。
引用: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
キーワード: 多発性骨髄腫, タンパク質品質管理, 小胞体関連分解(ERAD), カスパーゼ‑8によるアポトーシス, ドラッグリポジショニング