Clear Sky Science · pt
Triagem de pequenas moléculas identifica inibidores citotóxicos da degradação associada ao retículo endoplasmático em mieloma múltiplo
Transformando uma Vulnerabilidade das Células Cancerígenas em um Novo Alvo
O mieloma múltiplo é um câncer do sangue que surge de células plasmáticas, as fábricas de anticorpos do corpo. Essas células estão constantemente produzindo proteínas, o que as torna incomumente dependentes de um sistema interno de controle de qualidade que encontra e elimina proteínas mal dobradas. Este estudo investiga se essa vulnerabilidade intrínseca pode ser explorada com uma droga de pequena molécula para matar células de mieloma, incluindo aquelas que deixaram de responder aos tratamentos atuais.
Uma Equipe de Limpeza Oculta dentro de Células Cancerígenas Sobrecarregadas
Dentro de cada célula, o retículo endoplasmático funciona como uma linha de montagem de proteínas. Quando proteínas são produzidas incorretamente, um processo chamado degradação associada ao retículo endoplasmático, ou ERAD, as marca para descarte e as envia para a maquinaria de processamento de resíduos da célula. As células de mieloma, que fabricam enormes quantidades de proteínas anticorpo, dependem fortemente do ERAD para sobreviver. Drogas existentes chamadas inibidores do proteassoma bloqueiam a etapa final desse sistema de limpeza e melhoraram a sobrevida dos pacientes, mas a maioria dos tumores eventualmente desenvolve resistência. Pesquisadores, portanto, buscaram encontrar drogas que atinjam etapas mais precoces do processo de limpeza, diretamente no ERAD, na esperança de eliminar células de mieloma por um mecanismo diferente.
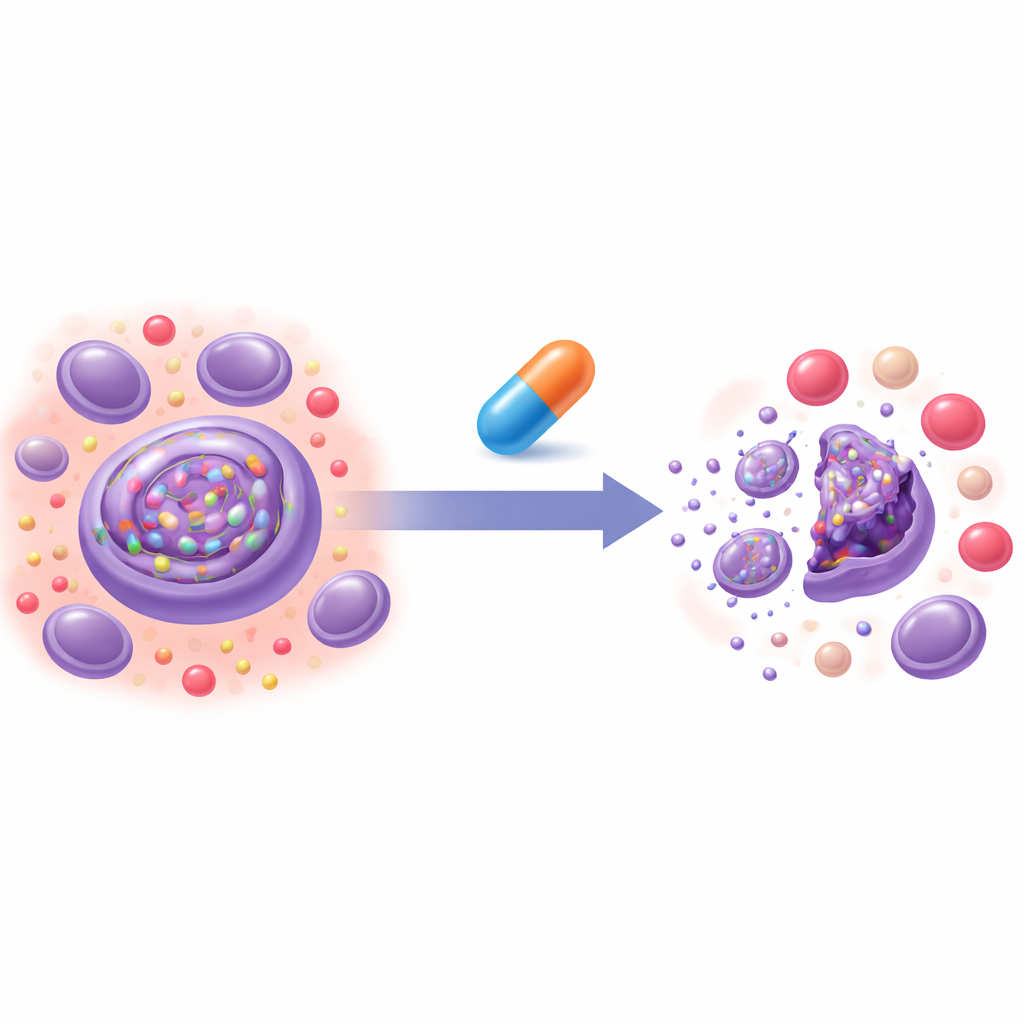
Triando Medicamentos Antigos para um Novo Propósito
A equipe construiu um teste em células que informa com que rapidez uma proteína modelo “defeituosa” é degradada pelo ERAD. Usando esse ensaio, eles triagem cerca de 2.200 compostos existentes de uma biblioteca de repropósito da FDA. Entre vários candidatos, identificaram omaveloxolona (também conhecida como RTA408), uma droga já aprovada para uma doença neurológica rara, como um potente bloqueador do ERAD. RTA408 desacelerou a degradação de múltiplas proteínas que normalmente dependem do ERAD, incluindo proteínas tanto soltas dentro do compartimento celular quanto aquelas incorporadas em sua membrana. Ao mesmo tempo, deixou muitas proteínas citosólicas livres relativamente intactas e não perturbou de forma significativa a principal maquinaria de descarte da célula, indicando uma ação focalizada no sistema de controle de qualidade de proteínas do RE, em vez de uma paralisação ampla do turnover proteico.
Morte Rápida e Seletiva de Células de Mieloma
Quando os pesquisadores trataram um painel de linhas celulares de mieloma com RTA408, a sobrevivência celular caiu rapidamente em poucas horas com baixas concentrações do fármaco, independentemente de as células serem sensíveis ou resistentes a inibidores do proteassoma. Um composto relacionado, RTA402, mostrou efeitos semelhantes. Importante, a capacidade da droga de matar células cancerígenas não dependia de seu papel conhecido em aumentar um regulador antioxidante chamado NRF2, o que implica um modo de ação até então não reconhecido. Em células de pacientes, RTA408 eliminou de forma eficiente células plasmáticas malignas tanto de indivíduos recém-diagnosticados quanto de pacientes fortemente pré-tratados, poupando a maior parte das células T e das células mieloides e mostrando apenas efeitos intermediários sobre células B normais. Em camundongos portadores de tumores humanos de mieloma, doses repetidas de RTA408 retardaram ou impediram marcadamente o crescimento tumoral, apoiando seu potencial como terapia no mundo real.
Uma Rota Inesperada para a Morte Celular
Como o bloqueio do ERAD é pensado para causar “engarrafamentos” de proteínas e estresse dentro da célula, muitos cientistas supuseram que a morte celular resultante seria conduzida por uma via de estresse bem conhecida chamada resposta a proteínas desnaturadas. Os autores confirmaram que essa resposta de estresse foi ativada após o tratamento com RTA408, mas experimentos cuidadosos mostraram que ela não era o gatilho principal para a onda rápida de morte celular. Em vez disso, a droga ativou rapidamente outra rota: a chamada via extrínseca da morte, que normalmente responde a sinais de perigo na superfície celular. RTA408 ativou rapidamente uma enzima chamada caspase-8 e seus parceiros a jusante, e bloquear essas enzimas quimicamente ou deletando proteínas adaptadoras chave (FADD e RIPK1) protegeu as células da morte. Surpreendentemente, remover receptores de morte individuais na superfície celular não resgatou as células, apontando para uma perturbação mais global em como esses receptores são organizados.
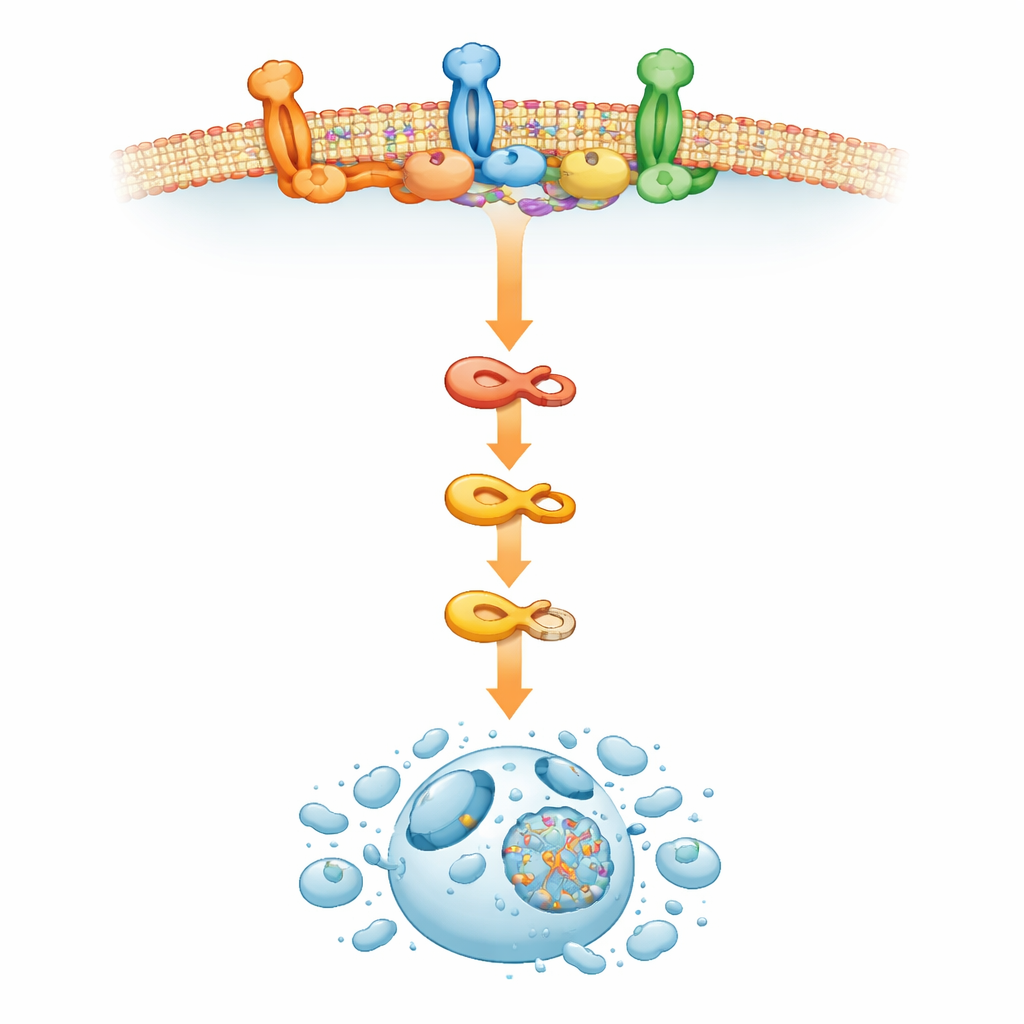
Como “Ilhas” na Membrana Celular Levam as Células Além do Limite
Para entender o que estava impulsionando essa ativação incomum da maquinaria de morte, a equipe voltou sua atenção para a membrana externa da célula. Ali, manchas especializadas ricas em colesterol, conhecidas como balsas lipídicas, atuam como miniplataformas de processamento de sinais. O estudo descobriu que a inibição do ERAD por RTA408 remodelou essas balsas, causando um acúmulo de marcadores de balsa e promovendo a montagem do complexo de sinalização indutor de morte que ativa a caspase-8. Quando os pesquisadores perturbaram as balsas lipídicas ou bloquearam a produção de colesterol, RTA408 não conseguiu mais desencadear a morte celular precoce, embora sinais de estresse interno na célula permanecessem. Isso indica que, em células de mieloma, interferir com o ERAD envia ondas que reorganizam a membrana, reunindo componentes da via de morte de uma forma que leva a célula cancerígena a se autodestruir.
O Que Isso Pode Significar para Pacientes
Em termos simples, este trabalho identifica uma droga aprovada que pode sabotar seletivamente um sistema crucial de manutenção das células de mieloma, empurrando-as para uma forma de morte programada que depende de como proteínas e lipídios estão organizados em sua membrana externa. Como RTA408 atua de maneira diferente dos atuais fármacos que bloqueiam o proteassoma e permanece eficaz em células resistentes e em modelos animais, ele oferece um novo ângulo promissor para tratar esse câncer ainda incurável. Ao mesmo tempo, o estudo revela uma ligação inesperada entre a maquinaria interna de controle de qualidade da célula e a organização de “interruptores de morte” na superfície, abrindo novas vias para projetar terapias que explorem os estresses únicos enfrentados por células cancerígenas produtoras de anticorpos.
Citação: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
Palavras-chave: mieloma múltiplo, controle de qualidade de proteínas, degradação associada ao RE, apoptose por caspase-8, repropósito de medicamentos