Clear Sky Science · ar
مسح الجزيئات الصغيرة يحدد مثبطات مؤذية مرتبطة بالتخلص من البروتين في الشبكة الإندوبلازمية في المايلوما المتعددة
تحويل نقطة ضعف خلايا السرطان إلى هدف جديد
المايلوما المتعددة هي سرطان دموي ينشأ من الخلايا البلازمية، وهي معامل الأجسام المضادة في الجسم. هذه الخلايا تنتج البروتينات باستمرار، مما يجعلها تعتمد بشكل غير عادي على نظام داخلي لمراقبة الجودة يجد البروتينات المشوهة ويدمرها. تستقصي هذه الدراسة ما إذا كان بالإمكان استغلال هذه الحساسية المدمجة باستخدام دواء جزيئي صغير لقتل خلايا المايلوما، بما في ذلك تلك التي توقفت عن الاستجابة للعلاجات الحالية.
طواقم تنظيف خفية داخل خلايا السرطان المجهدة
داخل كل خلية، تعمل الشبكة الإندوبلازمية كسطر تجميع للبروتينات. عندما تُنتَج البروتينات بشكل غير صحيح، تقوم عملية تسمى «التخلص المرتبط بالشبكة الإندوبلازمية» (ERAD) بوضع علامة عليها للتخلص وإرسالها إلى آليات معالجة النفايات في الخلية. خلايا المايلوما، التي تصنّع كميات هائلة من بروتينات الأجسام المضادة، تعتمد بشدة على ERAD للبقاء على قيد الحياة. الأدوية الحالية المسماة مثبطات البروتيازوم تحول دون الخطوة النهائية في هذا النظام، وقد حسنت البقاء على قيد الحياة للمرضى، لكن معظم الأورام تصبح مقاومة في نهاية المطاف. لذلك سعى الباحثون إلى إيجاد أدوية تضرب في وقت أبكر من عملية التنظيف، مباشرة عند ERAD، على أمل إيقاف خلايا المايلوما بطريقة مختلفة.
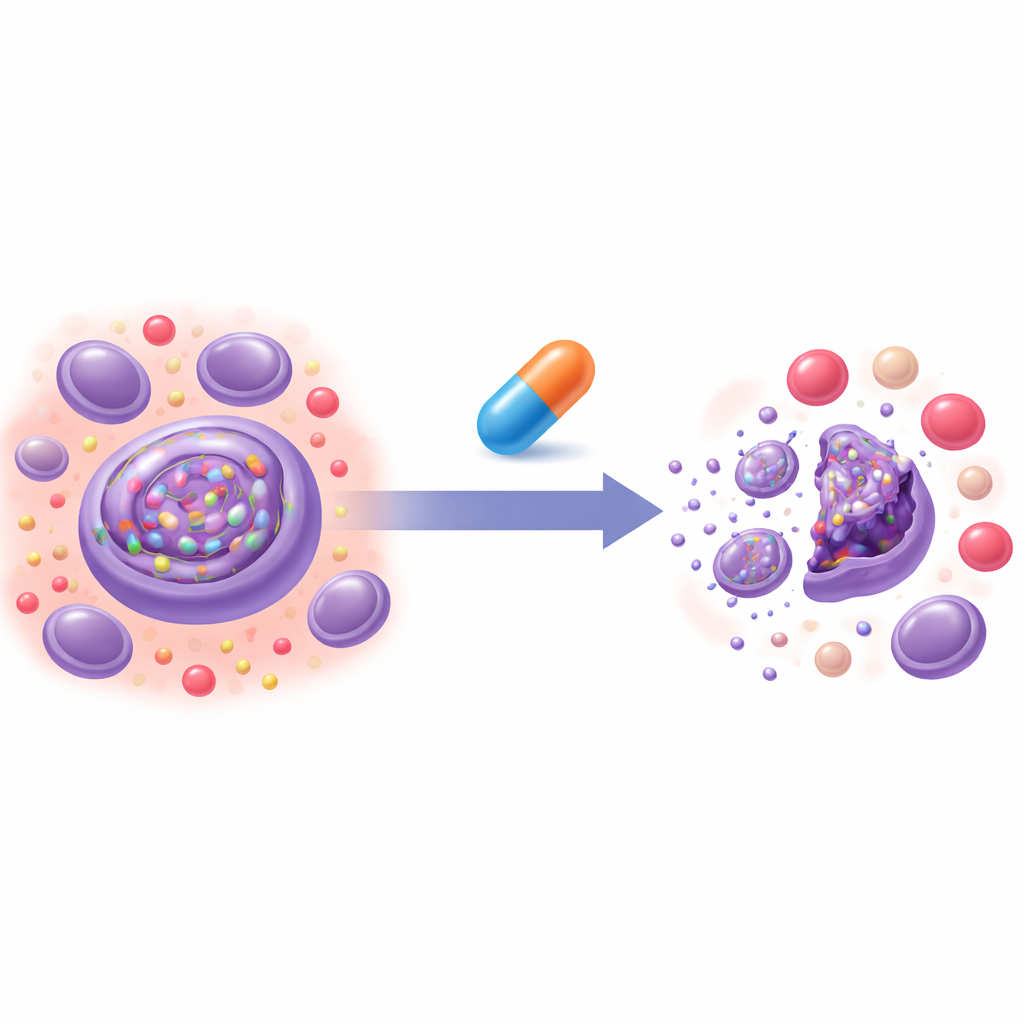
فحص أدوية قديمة لغرض جديد
بنى الفريق اختبارًا خلويًا يبلغ عن سرعة تحلل بروتين «سيء» نموذجي بواسطة ERAD. باستخدام هذا الاختبار، فحصوا نحو 2200 مركب موجود مسبقًا من مكتبة إعادة توظيف مرخَّصة من إدارة الغذاء والدواء. من بين عدة مرشحين، حدّدوا أومافيلوكسولون (المعروف أيضًا باسم RTA408)، وهو دواء معتمد بالفعل لمرض عصبي نادر، كمثبط قوي لـ ERAD. أبطأ RTA408 تكسير عدة بروتينات تعتمد عادة على ERAD، بما في ذلك البروتينات الحرة داخل الحجرة الخلوية وتلك المدمجة في غشائها. في الوقت نفسه، ترك العديد من البروتينات الحرة في السيتوسول سليمة إلى حد كبير ولم يعطل بشكل كبير آلية التخلص الرئيسية في الخلية، مما يشير إلى تأثير مركز على نظام مراقبة جودة بروتينات الشبكة الإندوبلازمية بدلاً من إيقاف واسع لتحلل البروتينات.
قتل سريع وانتقائي لخلايا المايلوما
عندما عالج الباحثون لوحة من خطوط خلايا المايلوما بـ RTA408، انخفض بقاء الخلايا بشكل حاد خلال ساعات عند تركيزات منخفضة من الدواء، بغض النظر عما إذا كانت الخلايا حساسة أم مقاومة لمثبطات البروتيازوم. أظهر مركب ذو صلة، RTA402، تأثيرات مماثلة. والأهم من ذلك، أن قدرة الدواء على قتل الخلايا السرطانية لم تعتمد على دوره المعروف في تعزيز منظم مضاد للأكسدة يسمى NRF2، مما يوحي بآلية عمل لم تُعرف سابقًا. في خلايا مأخوذة من مرضى، قضى RTA408 بفعالية على الخلايا البلازمية الخبيثة من كل من المرضى المشخصين حديثًا ومن أولئك الذين تلقوا علاجات مكثفة سابقًا، مع حفاظه على معظم خلايا T والخلايا النخاعية وظهور تأثيرات متوسطة فقط على الخلايا B الطبيعية. في فئران حاملة لأورام مايلوما بشرية، أدت الجرعات المتكررة من RTA408 إلى إبطاء نمو الورم بشكل ملحوظ أو منعه، مما يدعم إمكاناته كعلاج عملي.
طريق غير متوقع للموت الخلوي
نظرًا لأنه يُعتقد أن حجب ERAD يسبب «ازدحامًا» في حركة البروتينات وإجهادًا داخل الخلية، افترض كثير من العلماء أن أي موت خَلَوي ناتج سيكون مدفوعًا بمسار الإجهاد المعروف باسم استجابة البروتين المطوي بشكل خاطئ. أكد المؤلفون أن استجابة الإجهاد هذه فُعِّلت بعد علاج RTA408، لكن تجارب دقيقة أظهرت أنها لم تكن العامل الرئيسي للموجة السريعة للموت الخلوي. بدلًا من ذلك، فعَّل الدواء بسرعة مسارًا آخر: المسار الخارجي للموت، الذي يستجيب عادةً لإشارات الخطر على سطح الخلية. شغّل RTA408 بسرعة إنزيمًا يسمى كاسبيز‑8 وشركاءه اللاحقين، وحماية الخلايا من الموت كانت ممكنة بإعاقة هذه الإنزيمات كيميائيًا أو بحذف بروتينات ناقلة رئيسية (FADD وRIPK1). ومن المدهش أن إزالة مستقبلات الموت الفردية على سطح الخلية لم تنقذ الخلايا، مما يشير إلى اضطراب أوسع في كيفية تنظيم هذه المستقبلات.
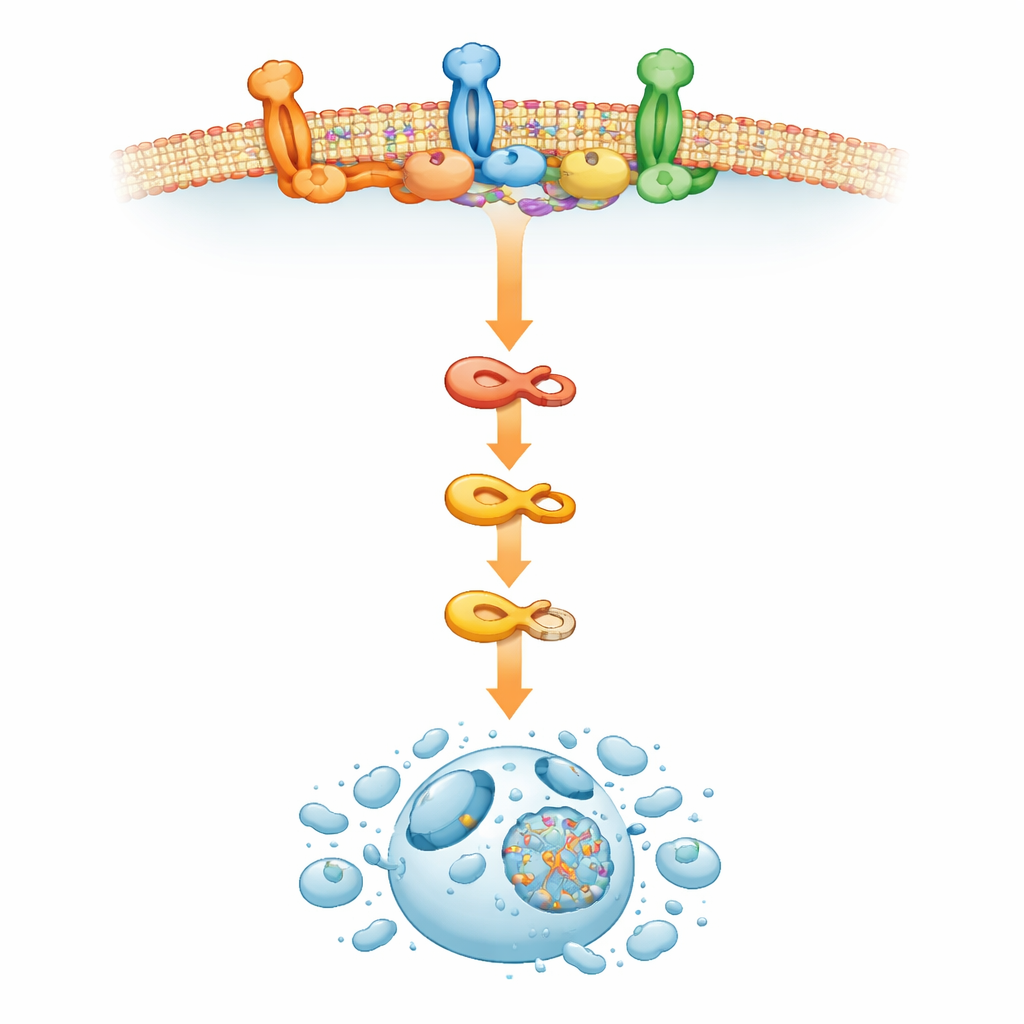
كيف تطيح «جزر» غشاء الخلية بالخلايا
لفهم ما الذي دفع هذا التفعيل غير المعتاد للماكينة المسببة للموت، توجه الفريق إلى غشاء الخلية الخارجي. هناك، تعمل بقع متخصصة غنية بالكوليسترول تُعرف بـ «الرافتات الدهنية» كمنصات صغيرة لمعالجة الإشارات. وجدت الدراسة أن تثبيط ERAD بواسطة RTA408 أعاد تشكيل هذه الرافتات، مما تسبب في تراكم علامات الرافت وتعزيز تجميع معقد إشارات تحريض الموت الذي ينشط كاسبيز‑8. عندما عطل الباحثون الرافتات الدهنية أو أعاقوا إنتاج الكوليسترول، لم يعد RTA408 قادرًا على تحفيز الموت المبكر للخلايا، رغم استمرار علامات الإجهاد الداخلي داخل الخلية. وهذا يشير إلى أنه في خلايا المايلوما، يؤدي التدخل في ERAD إلى موجات تعيد تنظيم الغشاء، مجمعة مكونات مسار الموت بطريقة تدفع الخلية السرطانية إلى الانتحار المبرمج.
ماذا قد يعني هذا للمرضى
بعبارة بسيطة، تحدد هذه الدراسة دواءً معتمدًا يمكنه تخريب نظام تنظيف حيوي حاسم في خلايا المايلوما بشكل انتقائي، دافعًا إياها نحو شكل من أشكال الموت المبرمج الذي يعتمد على كيفية ترتيب البروتينات والدهون في غشاءها الخارجي. وبما أن RTA408 يعمل بطريقة مختلفة عن أدوية حجب البروتيازوم الحالية ويظل فعالًا في الخلايا المقاومة وفي نماذج حيوانية، فإنه يوفر زاوية واعدة جديدة لعلاج هذا السرطان الذي لا يزال لا يُشفى. وفي الوقت ذاته، تكشف الدراسة عن صلة غير متوقعة بين آلية مراقبة الجودة الداخلية للخلية وتنظيم «مفاتيح الموت» السطحية، فاتحة سبلًا جديدة لتصميم علاجات تستغل الضغوط الخاصة بخلايا السرطان المنتجة للأجسام المضادة.
الاستشهاد: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
الكلمات المفتاحية: المايلوما المتعددة, مراقبة جودة البروتين, التخلص المرتبط بالشبكة الإندوبلازمية, استماتة كاسبيز-8, إعادة استخدام الأدوية