Clear Sky Science · pl
Przesiew małych cząsteczek identyfikuje cytotoksyczne inhibitory degradacji związanej z retikulum endoplazmatycznym w szpiczaku mnogim
Przekształcenie słabości komórek nowotworowych w nowy cel
Szpiczak mnogi to nowotwór krwi wywodzący się z komórek plazmatycznych, fabryk przeciwciał organizmu. Komórki te nieustannie produkują białka, przez co są wyjątkowo zależne od wewnętrznego systemu kontroli jakości, który wykrywa i usuwa źle złożone białka. W badaniu tym sprawdzono, czy tę wrodzoną podatność można wykorzystać za pomocą małocząsteczkowego leku do zabicia komórek szpiczaka, także tych, które przestały reagować na dostępne terapie.
Ukryty zespół sprzątający w przeciążonych komórkach nowotworowych
W każdej komórce retikulum endoplazmatyczne pełni rolę taśmy montażowej białek. Gdy białka są wytwarzane nieprawidłowo, proces zwany degradacją związaną z ER (ERAD) oznacza je do usunięcia i kieruje do „odpadów” komórkowych. Komórki szpiczaka, które syntetyzują ogromne ilości białek przeciwciał, w dużym stopniu polegają na ERAD, by przetrwać. Dostępne leki z grupy inhibitorów proteasomu blokują końcowy etap tego systemu oczyszczania i poprawiły przeżywalność pacjentów, ale większość guzów w końcu nabywa oporność. Naukowcy postanowili więc znaleźć leki uderzające wcześniej w proces sprzątania, bezpośrednio w ERAD, w nadziei na unikalne wyłączenie komórek szpiczaka.
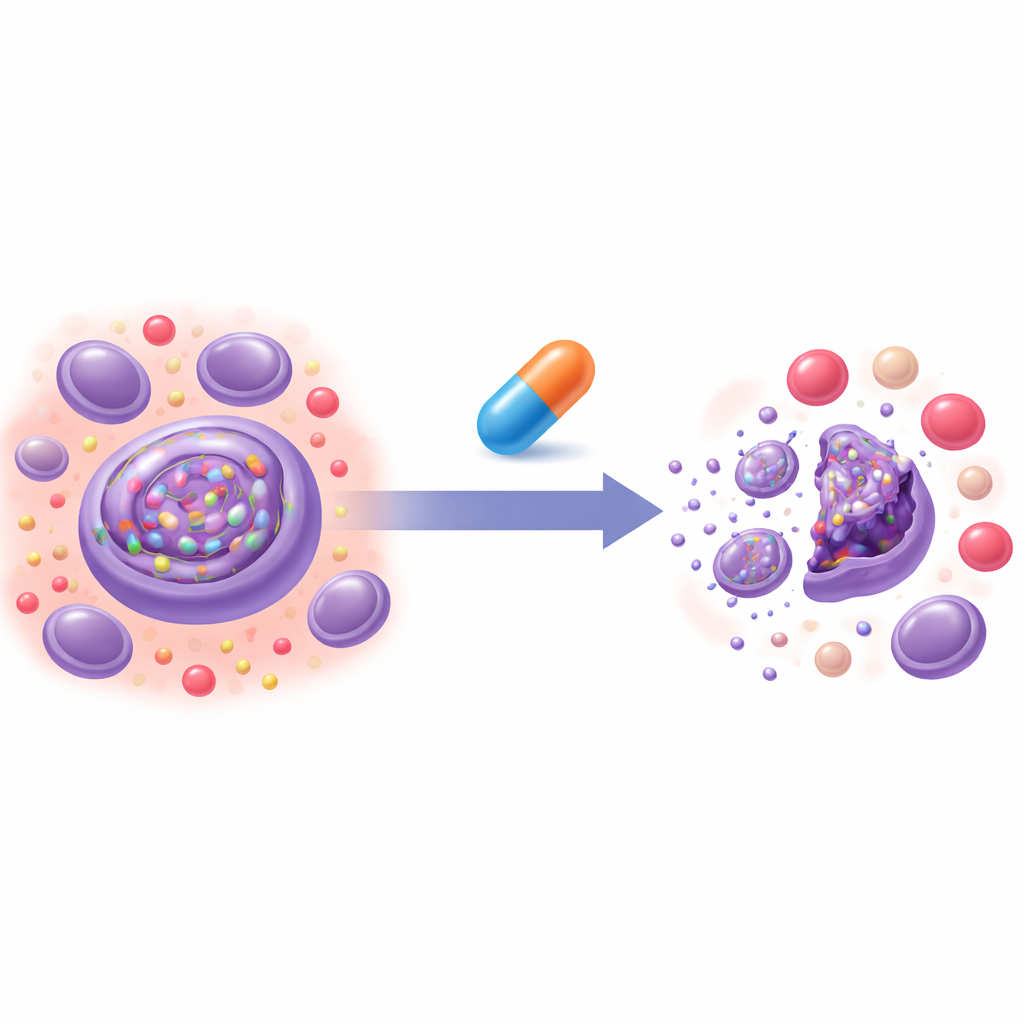
Przesiewanie starych leków w nowym celu
Zespół opracował test komórkowy, który raportuje, jak szybko modelowe „złe” białko jest rozkładane przez ERAD. Przy użyciu tego testu przesiano około 2200 istniejących związków z biblioteki przeznaczonej do ponownego zastosowania zatwierdzonych przez FDA. Wśród kilku kandydatów zidentyfikowano omaveloksolon (znany też jako RTA408), lek już zatwierdzony w rzadkiej chorobie neurologicznej, jako silny inhibitor ERAD. RTA408 spowolnił rozkład wielu białek, które normalnie zależą od ERAD, obejmując zarówno białka wolne w obrębie kompartmentu, jak i te osadzone w jego błonie. Jednocześnie pozostawił stosunkowo nietknięte wiele kluczowych białek cytosolowych i nie zakłócił znacząco głównego mechanizmu usuwania odpadów komórkowych, co wskazuje na skoncentrowane działanie na system kontroli jakości białek w ER, a nie na ogólną blokadę obrotu białek.
Szybkie, selektywne zabijanie komórek szpiczaka
Gdy badacze potraktowali panel linii komórkowych szpiczaka RTA408, przeżywalność komórek gwałtownie spadła w ciągu kilku godzin przy niskich stężeniach leku, niezależnie od wrażliwości na inhibitory proteasomu. Podobny związek, RTA402, wykazał zbliżone efekty. Co ważne, zdolność leku do zabijania komórek nowotworowych nie zależała od jego znanej roli w zwiększaniu aktywności regulatora antyoksydacyjnego NRF2, co sugeruje wcześniej nieznany mechanizm działania. W próbkach od pacjentów RTA408 skutecznie eliminował złośliwe komórki plazmatyczne zarówno od osób nowo zdiagnozowanych, jak i silnie wcześniej leczonych, przy jednoczesnym oszczędzaniu większości komórek T i mieloidalnych oraz wywoływaniu jedynie umiarkowanych skutków wobec normalnych komórek B. U myszy z ludzkimi guzami szpiczaka wielokrotne dawkowanie RTA408 znacznie spowalniało lub zapobiegało wzrostowi guza, wspierając jego potencjał terapeutyczny w warunkach in vivo.
Niespodziewana droga do śmierci komórki
Ponieważ blokada ERAD uważana jest za powodującą zatory białkowe i stres wewnątrz komórki, wielu naukowców zakładało, że powstała śmierć komórki będzie napędzana przez dobrze znaną ścieżkę stresową zwaną odpowiedzią na niezłożone białka (unfolded protein response). Autorzy potwierdzili, że ta odpowiedź stresowa rzeczywiście włączała się po leczeniu RTA408, lecz staranne eksperymenty wykazały, że nie była ona głównym wyzwalaczem szybkiej fali śmierci komórek. Zamiast tego lek szybko uruchamiał inną drogę: tzw. zewnętrzną ścieżkę śmierci, która zwykle reaguje na sygnały zagrożenia na powierzchni komórki. RTA408 błyskawicznie aktywował enzym kaspazę‑8 i jej następców, a blokowanie tych enzymów chemicznie lub przez usunięcie kluczowych białek adaptorowych (FADD i RIPK1) chroniło komórki przed śmiercią. Co zaskakujące, usuwanie pojedynczych receptorów śmierci na powierzchni komórki nie ratowało komórek, co wskazuje na bardziej globalne zaburzenie organizacji tych receptorów.
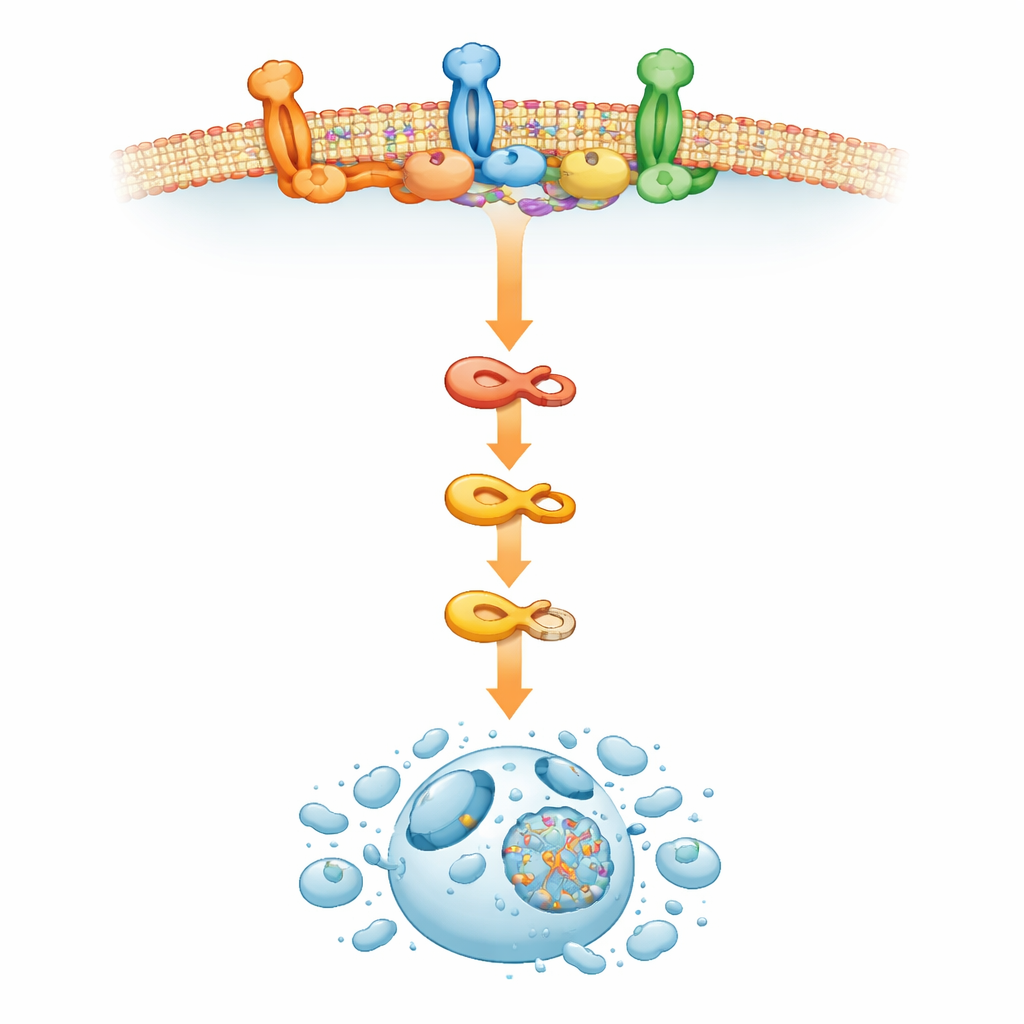
Jak „wyspy” w błonie komórkowej popychają komórki przez krawędź
Aby zrozumieć, co napędzało tę nietypową aktywację maszynerii śmierci, zespół zwrócił uwagę na błonę zewnętrzną komórki. Tam wyspecjalizowane cholesterol‑bogate pęcherzyki znane jako tratwy lipidowe służą jako mini platformy przetwarzania sygnałów. Badanie wykazało, że zahamowanie ERAD przez RTA408 przebudowywało te tratwy, powodując gromadzenie markerów tratw i sprzyjając tworzeniu kompleksu sygnałowego indukującego śmierć, który aktywuje kaspazę‑8. Gdy badacze zakłócili tratwy lipidowe lub zablokowali syntezę cholesterolu, RTA408 nie był już w stanie wywołać wczesnej śmierci komórek, mimo że oznaki wewnętrznego stresu wewnątrz komórki utrzymywały się. Wskazuje to, że w komórkach szpiczaka ingerencja w ERAD wysyła zaburzenia, które reorganizują błonę, zbliżając elementy ścieżki śmierci w sposób prowadzący do samobójczego programu komórkowego nowotworu.
Co to może znaczyć dla pacjentów
Mówiąc wprost, praca ta identyfikuje zatwierdzony lek, który może selektywnie sabotować kluczowy system porządkowy w komórkach szpiczaka, popychając je ku formie zaprogramowanej śmierci zależnej od organizacji białek i lipidów w ich błonie zewnętrznej. Ponieważ RTA408 działa inaczej niż obecne leki blokujące proteasom i pozostaje skuteczny w komórkach opornych oraz w modelach zwierzęcych, oferuje obiecujący nowy kierunek leczenia tego wciąż nieuleczalnego nowotworu. Jednocześnie badanie ujawnia niespodziewane powiązanie między wewnętrznym mechanizmem kontroli jakości a organizacją „włączników śmierci” na powierzchni, otwierając nowe drogi projektowania terapii wykorzystujących unikalne obciążenia, z jakimi borykają się komórki nowotworowe produkujące przeciwciała.
Cytowanie: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
Słowa kluczowe: szpiczak mnogi, kontrola jakości białek, degradacja związana z ER, apoptoza zależna od kaspazy‑8, ponowne zastosowanie leków