Clear Sky Science · he
מסך מולקולות קטנות מזהה מעכבים ציטוטוקסיים של פירוק חלבונים בתחלופה הקשורה לרשת האנדופלזמית במיאלומה מרובה
הפיכת חולשה של תאי סרטן למטרה חדשה
מיאלומה מרובה היא סרטן דם הנובע מתאים פלזמה, בתי החרושת של נוגדנים בגוף. תאים אלה מייצרים חלבונים באופן מתמיד, ולכן הם תלויים באופן בלתי רגיל במערכת בקרת איכות פנימית שמזהה ומחסלת חלבונים מקופלים בצורה שגויה. מחקר זה בוחן האם חולשה מובנת זו ניתנת לניצול באמצעות מולקולת־משנה כדי להרוג תאי מיאלומה, כולל כאלה שהפסיקו להגיב לטיפולים הנוכחיים.
צוות ניקיון חבוי בתוך תאי סרטן עמוסים
בתוך כל תא, הרשת האנדופלזמית פועלת כקו הרכבת לחלבונים. כשהחלבונים מיוצרים בצורה לא נכונה, תהליך שנקרא פירוק קשור ER (ER‑associated degradation, או ERAD) מסמן אותם להיפטרות ושולח אותם למכונות העיבוד של הפסולת התאית. תאי מיאלומה, המייצרים כמויות עצומות של חלבוני נוגדן, תלויים מאוד ב‑ERAD כדי לשרוד. תרופות קיימות הנקראות מעכבי פרוטאזום חוסמות את השלב האחרון של מערכת הפסולת הזו ושיפרו את תוחלת החיים של מטופלים, אך רוב הגידולים בסופו של דבר מפתחים עמידות. לכן החוקרים שאפו למצוא תרופות שפוגעות בשלבים מוקדמים יותר של תהליך הניקיון, ישירות ב‑ERAD, בתקווה לכבות את תאי המיאלומה בדרך שונה.
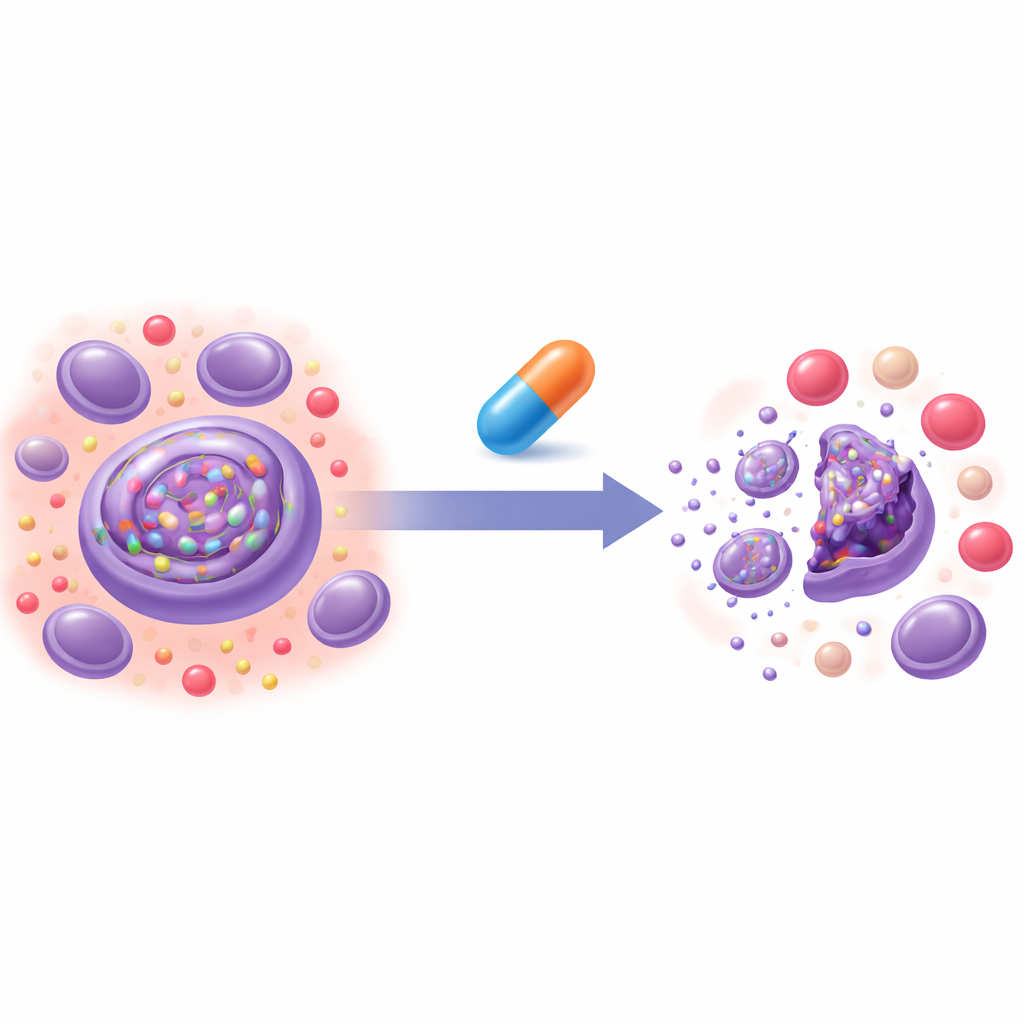
מסך של תרופות ישנות למטרה חדשה
הצוות בנה בדיקת תא שמדווחת על קצב פירוק של חלבון "רע" מדגם על‑ידי ERAD. באמצעות assay זה הם סרקו כ‑2,200 תרכובות קיימות מספרייה לשימוש חוזר שאושרה על‑ידי ה‑FDA. בין מספר מועמדים זוהתה אומאבלוקסולון (המוכר גם כ‑RTA408), תרופה שאושרה לשימוש במחלה נוירולוגית נדירה, כמחסום חזק של ERAD. RTA408 האט את פירוקם של מספר חלבונים שתלויים בדרך כלל ב‑ERAD, כולל חלבונים פרוטופלזמטיים וחלבונים מוטמעים בממברנה. במקביל, התרופה השאירה רבים מהחלבונים הציטוזוליים החופשיים יחסית בלתי מושפעים ולא שיבשה משמעותית את מכונת הפסולת הראשית של התא, מה שמעיד על פעולה ממוקדת במערכת בקרת איכות החלבונים של ה‑ER ולא על עצירה כוללת של מחזור החלבונים.
הרג מהיר וסלקטיבי של תאי מיאלומה
כשחוקרים טיפלו בלוח קווי תאי מיאלומה ב‑RTA408, הישרדות התאים ירדה בחדות בתוך שעות בריכוזי תרופה נמוכים, בלי תלות ברגישותם או בעמידותם למעכבי פרוטאזום. תרכובת קרובה, RTA402, הציגה אפקטים דומים. חשוב לציין, יכולת התרופה להרוג תאי סרטן לא הייתה תלויה בתפקידה הידוע בהגברה של רגולטור נוגד חמצון בשם NRF2, דבר המצביע על מנגנון פעולה שטרם זוהה קודם. בתאים ממטופלים, RTA408 השמיד ביעילות תאי פלזמה ממאירים הן ממטופלים שאובחנו זה עתה והן ממטופלים שטופלו בעבר בעוצמה, תוך שמירה על רוב תאי T ותאי מיואיד ועם השפעות בינוניות בלבד על תאי B נורמליים. בעכברים שנושאים גידולי מיאלומה אנושיים, מתן חוזר של RTA408 האט או מנע באופן משמעותי את צמיחת הגידול, תומך בפוטנציאל שלו כטיפול במציאות הקלינית.
נתיב מוות בלתי צפוי
מכיוון שחסימת ERAD נחשבת לייצר "פקקי תנועה" של חלבונים ולמתח פנימי בתא, רבים הניחו שמוות התאים הנובע יונע על‑ידי מסלול המתח הידוע בשם תגובת החלבון המקופל (unfolded protein response). המחברים איששו כי תגובת מתח זו הופעלה לאחר טיפול ב‑RTA408, אך ניסויים קפדניים הראו שהיא לא היתה הזרז העיקרי לגל המהיר של מות התאים. במקום זאת, התרופה הפעלה במהירות נתיב אחר: נתיב המוות החיצוני, שבדרך כלל מגיב לאותות סכנה על פני התא. RTA408 הפעיל במהירות את האנזים קספאז‑8 ואת השותפים המטה שלו, וחסימת האנזימים הללו כימית או על‑ידי מחיקה של חלבוני מתווך מרכזיים (FADD ו‑RIPK1) הגנה על התאים מפני מוות. באופן מפתיע, הסרת רצפטורים בודדים למוות על פני התא לא הצילה את התאים, מה שמצביע על הפרעה יותר גלובלית בארגון שלהם.
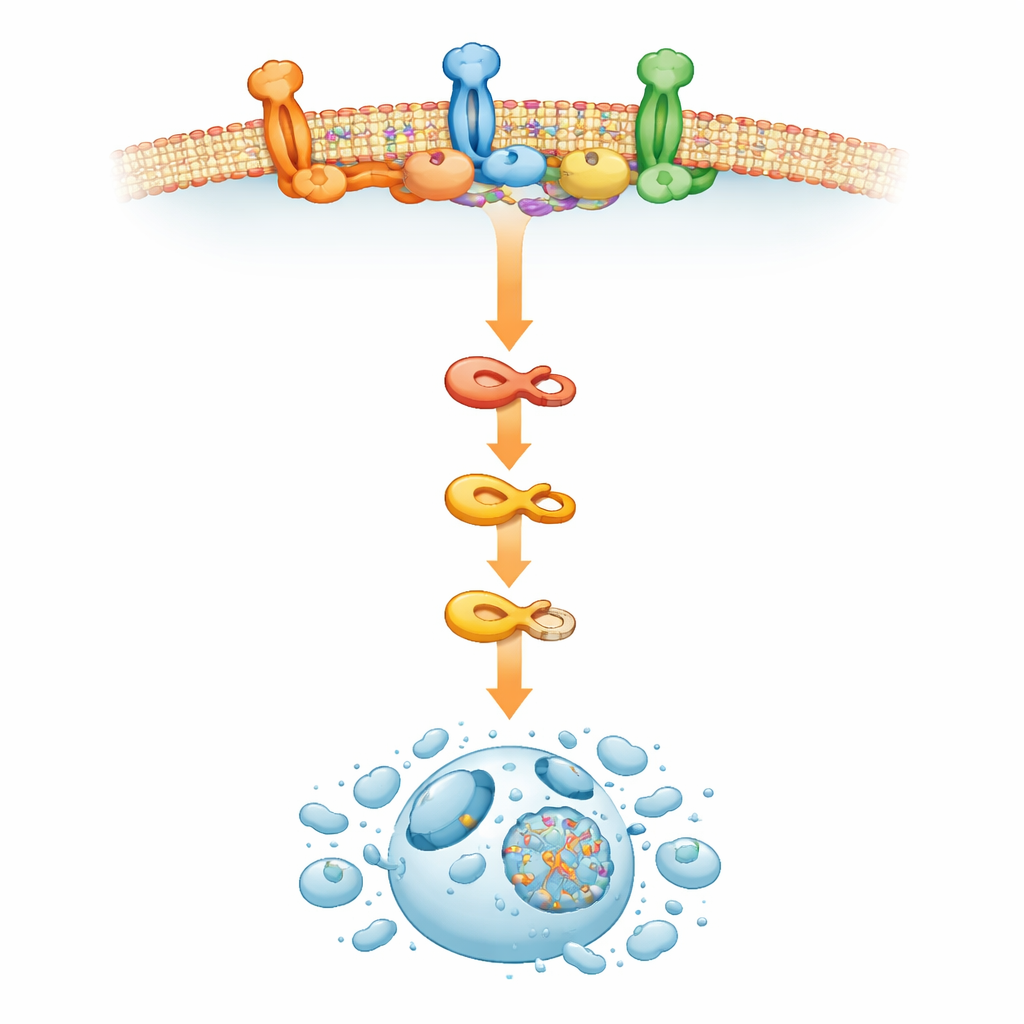
כיצד "איים" בממברנה התאית דוחפים את התאים מעבר לקו
כדי להבין מה הוביל להפעלה החריגה של מכונת המוות, הצוות פנה לממברנת התא החיצונית. שם, טלאים עשירים כולסטרול המכונים רצפות שומניות (lipid rafts) משמשים כפלטפורמות עיבוד אותות זעירות. המחקר מצא שחסימת ERAD על‑ידי RTA408 שינתה את צורת הרצפות האלה, גרמה להצטברות סימני רצפה וקידמה את ההרכבה של קומפלקס האיתות המגרה מוות שמפעיל את קספאז‑8. כאשר החוקרים הפריעו לרצפות השומניות או חסמו את ייצור הכולסטרול, RTA408 כבר לא הצליחה לגרום למות תאי מוקדם, אף על פי שסימני מתח פנימי בתא נותרו. זה מצביע על כך שבמיאלומה, הפרעה ל‑ERAD יוצרת גל שיפוצים שמארגן מחדש את הממברנה ומקרב יחד רכיבי נתיב המוות באופן שמוביל את תא הסרטן לאבדון עצמי.
מה זה עשוי למשמעות עבור מטופלים
במילים פשוטות, עבודה זו מזהה תרופה מאושרת שיכולה להכפיש באופן סלקטיבי מערכת תחזוקה מרכזית בתאי המיאלומה, ולדחוף אותם לצורת מוות מתוכנתת שתלויה באופן שבו חלבונים ושומנים מסודרים בממברנה החיצונית שלהם. מכיוון ש‑RTA408 פועל באופן שונה מתרופות חוסמות הפרוטאזום הנוכחיות ונשאר יעיל בתאים עמידים ובדגמי בעלי חיים, הוא מציע זווית מבט מבטיחה חדשה לטיפול בסרטן זה שעדיין נותר בלתי ניתן לריפוי. במקביל, המחקר חושף קישור מפתיע בין מערכת בקרת האיכות הפנימית של התא לארגון "מפסקים למוות" על פני השטח, פותח דרכים חדשות לעיצוב טיפולים המנצלים את המתח הייחודי שאופף תאי סרטן שמייצרים נוגדנים.
ציטוט: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
מילות מפתח: מיאלומה מרובה, בקרת איכות חלבונים, פירוק קשור ER (ER-associated degradation), אפופטוזה דרך קספאז‑8, שימוש חוזר בתרופות