Clear Sky Science · es
El cribado de pequeñas moléculas identifica inhibidores citotóxicos de la degradación asociada al retículo endoplásmico en el mieloma múltiple
Convertir una debilidad de las células cancerosas en un nuevo objetivo
El mieloma múltiple es un cáncer de la sangre que se origina en las células plasmáticas, las fábricas de anticuerpos del organismo. Estas células sintetizan proteínas de forma continua, lo que las hace particularmente dependientes de un sistema interno de control de calidad que detecta y elimina proteínas mal plegadas. Este estudio explora si esa vulnerabilidad incorporada puede explotarse con una pequeña molécula para matar las células de mieloma, incluidas aquellas que han dejado de responder a tratamientos actuales.
Un equipo de limpieza oculto dentro de las células cancerosas sobrecargadas
Dentro de cada célula, el retículo endoplásmico actúa como una línea de ensamblaje de proteínas. Cuando las proteínas se fabrican incorrectamente, un proceso llamado degradación asociada al retículo endoplásmico, o ERAD, las marca para su eliminación y las envía a la maquinaria celular de procesamiento de desechos. Las células de mieloma, que fabrican enormes cantidades de proteínas de anticuerpos, dependen en gran medida de ERAD para sobrevivir. Los fármacos existentes llamados inhibidores del proteasoma bloquean el paso final de este sistema de eliminación y han mejorado la supervivencia de los pacientes, pero la mayoría de los tumores acaban volviéndose resistentes. Por ello, los investigadores decidieron buscar fármacos que actúen más temprano en el proceso de limpieza, directamente sobre ERAD, con la esperanza de apagar las células de mieloma de una manera distinta.
Cribando fármacos antiguos para un nuevo propósito
El equipo desarrolló una prueba celular que informa de la rapidez con que una proteína modelo “defectuosa” es degradada por ERAD. Usando este ensayo, cribaron alrededor de 2.200 compuestos existentes procedentes de una biblioteca de reposicionamiento aprobada por la FDA. Entre varios candidatos identificaron omaveloxolona (también conocida como RTA408), un fármaco ya aprobado para una enfermedad neurológica rara, como un potente bloqueador de ERAD. RTA408 ralentizó la degradación de múltiples proteínas que normalmente dependen de ERAD, incluidas proteínas tanto solubles en el compartimento celular como integradas en su membrana. Al mismo tiempo, dejó relativamente intactas muchas proteínas citosólicas clave y no alteró de forma significativa la principal maquinaria de eliminación de desechos de la célula, lo que indica una acción focalizada sobre el sistema de control de calidad proteica del RE en lugar de un apagado general del recambio proteico.
Eliminación rápida y selectiva de células de mieloma
Cuando los investigadores trataron un panel de líneas celulares de mieloma con RTA408, la supervivencia celular cayó drásticamente en pocas horas con bajas concentraciones de fármaco, independientemente de si las células eran sensibles o resistentes a los inhibidores del proteasoma. Un compuesto relacionado, RTA402, mostró efectos similares. Es importante señalar que la capacidad del fármaco para matar células cancerosas no dependía de su papel conocido en la activación de un regulador antioxidante llamado NRF2, lo que sugiere un modo de acción hasta ahora no reconocido. En células procedentes de pacientes, RTA408 eliminó de forma eficaz las células plasmáticas malignas tanto de individuos diagnosticados recientemente como de pacientes muy pretratados, mientras que respetó en su mayoría a las células T y a las células mieloides y mostró efectos solo intermedios sobre las células B normales. En ratones con tumores humanos de mieloma, la dosificación repetida con RTA408 ralentizó de forma notable o impidió el crecimiento tumoral, respaldando su potencial como terapia en el mundo real.
Una vía inesperada hacia la muerte celular
Puesto que se piensa que bloquear ERAD causa «atascos» de proteínas y estrés dentro de la célula, muchos científicos supusieron que la muerte celular resultante estaría mediada por una conocida vía de estrés llamada respuesta a proteínas mal plegadas (unfolded protein response). Los autores confirmaron que esta respuesta de estrés se activó tras el tratamiento con RTA408, pero experimentos cuidadosos mostraron que no era el desencadenante principal de la rápida oleada de muerte celular. En su lugar, el fármaco activó con rapidez una vía distinta: la denominada vía extrínseca de muerte, que normalmente responde a señales de peligro en la superficie celular. RTA408 activó rápidamente una enzima llamada caspasa-8 y sus socios aguas abajo, y bloquear químicamente estas enzimas o eliminar proteínas adaptadoras clave (FADD y RIPK1) protegió a las células de la muerte. Sorprendentemente, la eliminación de receptores de muerte individuales en la superficie celular no rescató a las células, lo que apunta a una perturbación más global en la organización de estos receptores.
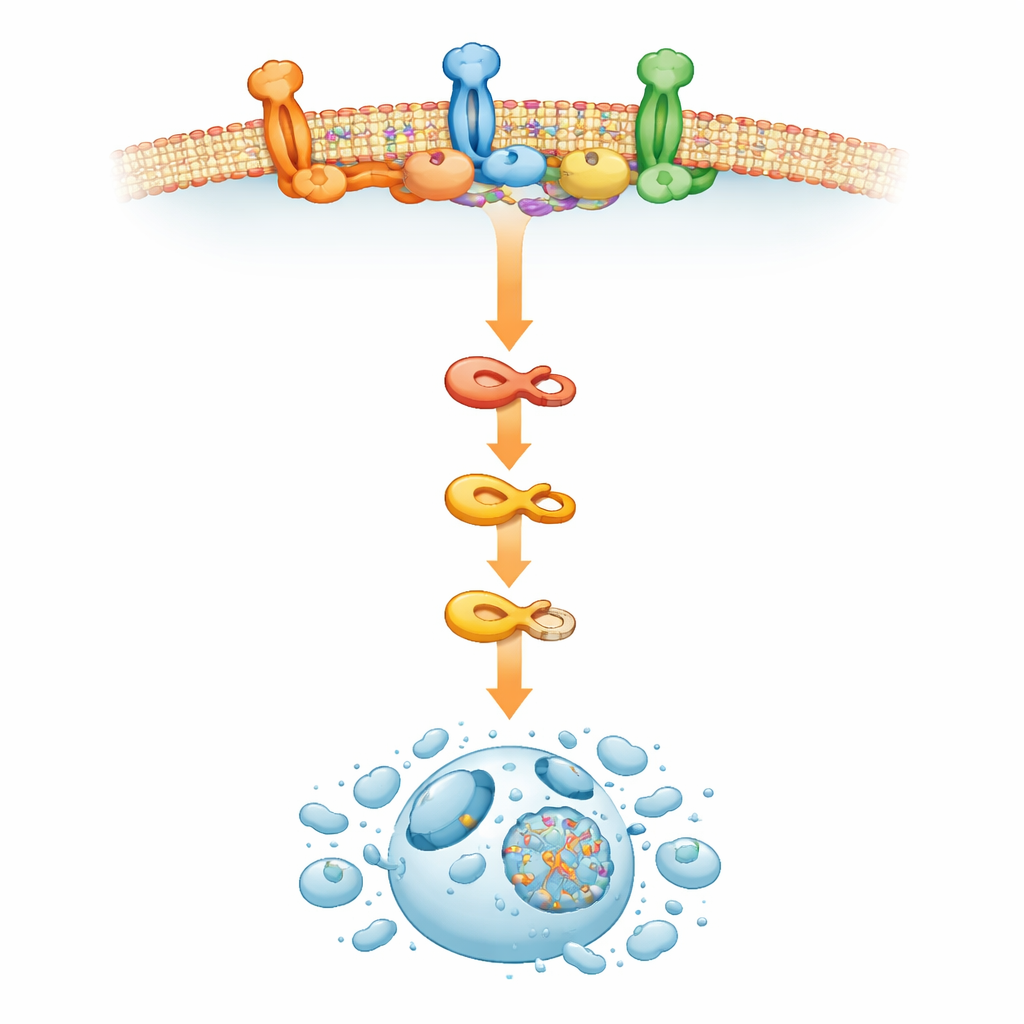
Cómo las “islas” de la membrana celular empujan a las células al límite
Para entender qué impulsaba esta inusual activación de la maquinaria de muerte, el equipo se centró en la membrana externa de la célula. Allí, parches especializados ricos en colesterol conocidos como balsas lipídicas actúan como pequeñas plataformas de procesamiento de señales. El estudio encontró que la inhibición de ERAD por RTA408 remodeló estas balsas, provocando una acumulación de marcadores de las mismas y promoviendo el ensamblaje del complejo señalizador inductor de muerte que activa la caspasa-8. Cuando los investigadores alteraron las balsas lipídicas o bloquearon la producción de colesterol, RTA408 ya no pudo desencadenar la muerte celular temprana, aunque persistían signos de estrés interno en la célula. Esto indica que, en las células de mieloma, interferir con ERAD envía ondas que reorganizan la membrana, reuniendo componentes de la vía de muerte de un modo que conduce a la autodestrucción de la célula cancerosa.
Qué podría significar esto para los pacientes
En términos sencillos, este trabajo identifica un fármaco aprobado que puede sabotear selectivamente un sistema de mantenimiento crucial en las células de mieloma, empujándolas hacia una forma de muerte programada que depende de cómo se organizan las proteínas y los lípidos en su membrana externa. Dado que RTA408 actúa de manera diferente a los actuales fármacos que bloquean el proteasoma y sigue siendo efectivo en células resistentes y en modelos animales, ofrece un enfoque prometedor para tratar este cáncer que aún no tiene cura. Al mismo tiempo, el estudio revela un vínculo inesperado entre la maquinaria interna de control de calidad celular y la organización de los «interruptores de muerte» en la superficie, abriendo nuevas vías para diseñar terapias que exploten las tensiones únicas de las células cancerosas productoras de anticuerpos.
Cita: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
Palabras clave: mieloma múltiple, control de calidad proteica, degradación asociada al RE, apoptosis por caspasa-8, reposicionamiento de fármacos