Clear Sky Science · it
Screening di piccole molecole individua inibitori citotossici della degradazione associata al reticolo endoplasmatico nel mieloma multiplo
Trasformare una debolezza delle cellule tumorali in un nuovo bersaglio
Il mieloma multiplo è un tumore del sangue che origina dalle plasmacellule, le “fabbriche” di anticorpi dell’organismo. Queste cellule producono costantemente proteine, il che le rende particolarmente dipendenti da un sistema interno di controllo di qualità che individua e distrugge le proteine mal ripiegate. Questo studio esplora se quella vulnerabilità intrinseca possa essere sfruttata con una piccola molecola per uccidere le cellule del mieloma, incluse quelle che hanno smesso di rispondere ai trattamenti attuali.
Una squadra di pulizia nascosta dentro cellule tumorali sovraccariche
All’interno di ogni cellula, il reticolo endoplasmatico funziona come una linea di montaggio delle proteine. Quando le proteine vengono sintetizzate in modo errato, un processo chiamato degradazione associata al reticolo endoplasmatico, o ERAD, le marca per lo smaltimento e le invia ai meccanismi di riciclo della cellula. Le plasmacellule del mieloma, che producono enormi quantità di proteine anticorpali, fanno grande affidamento su ERAD per sopravvivere. I farmaci esistenti chiamati inibitori del proteasoma bloccano il passo finale di questo sistema di smaltimento e hanno migliorato la sopravvivenza dei pazienti, ma la maggior parte dei tumori diventa alla fine resistente. I ricercatori si sono quindi proposti di trovare farmaci che colpiscano più a monte il processo di pulizia, direttamente su ERAD, nella speranza di bloccare le cellule del mieloma in modo differente.
Setacciare farmaci già noti per uno scopo nuovo
Il gruppo ha sviluppato un test cellulare che segnala la rapidità con cui una proteina modello “difettosa” viene degradato da ERAD. Usando questo saggio, hanno esaminato circa 2.200 composti esistenti provenienti da una library di rimodulazione approvata dalla FDA. Tra diversi candidati hanno identificato omaveloxolone (noto anche come RTA408), un farmaco già approvato per una rara malattia neurologica, come un potente inibitore di ERAD. RTA408 rallentava la degradazione di diverse proteine che normalmente dipendono da ERAD, incluse proteine sia solubili all’interno del compartimento cellulare sia integrate nella sua membrana. Allo stesso tempo, lasciava relativamente intatte molte proteine chiave citosoliche e non alterava in modo significativo la principale macchina di riciclo delle proteine della cellula, indicando un’azione mirata sul sistema di controllo della qualità proteica del reticolo piuttosto che uno spegnimento generalizzato del turnover proteico.
Uccisione rapida e selettiva delle cellule del mieloma
Quando i ricercatori hanno trattato una serie di linee cellulari di mieloma con RTA408, la sopravvivenza cellulare è calata nettamente nel giro di poche ore a basse concentrazioni di farmaco, indipendentemente dal fatto che le cellule fossero sensibili o resistenti agli inibitori del proteasoma. Un composto correlato, RTA402, ha mostrato effetti simili. È importante che la capacità del farmaco di uccidere le cellule tumorali non dipendesse dal suo noto ruolo nel potenziare un regolatore antiossidante chiamato NRF2, il che implica un meccanismo d’azione precedentemente non riconosciuto. In cellule provenienti da pazienti, RTA408 eliminava efficacemente le plasmacellule maligne sia nei casi di nuova diagnosi sia in pazienti pesantemente pretrattati, risparmiando la maggior parte delle cellule T e mieloidi e mostrando soltanto effetti intermedi sulle cellule B normali. In topi portatori di tumori umani di mieloma, dosaggi ripetuti di RTA408 rallentavano o impedivano in modo marcato la crescita tumorale, supportando il suo potenziale come terapia pratica.
Una via inaspettata verso la morte cellulare
Poiché bloccare ERAD si pensa provochi “ingorghi” proteici e stress all’interno della cellula, molti scienziati presumevano che la morte cellulare risultante fosse guidata da una ben nota via di stress chiamata risposta alle proteine non ripiegate. Gli autori hanno confermato che questa risposta di stress si attivava dopo il trattamento con RTA408, ma esperimenti accurati hanno mostrato che non era il principale innesco dell’ondata rapida di morte cellulare. Invece, il farmaco attivava velocemente un’altra via: la cosiddetta via estrinseca della morte, che normalmente risponde a segnali di pericolo sulla superficie cellulare. RTA408 attivava rapidamente un enzima chiamato caspasi‑8 e i suoi partner a valle, e bloccare questi enzimi chimicamente o eliminando adattatori chiave (FADD e RIPK1) proteggeva le cellule dalla morte. Sorprendentemente, rimuovere singoli recettori di morte sulla superficie cellulare non salvava le cellule, suggerendo una perturbazione più globale nell’organizzazione di questi recettori.
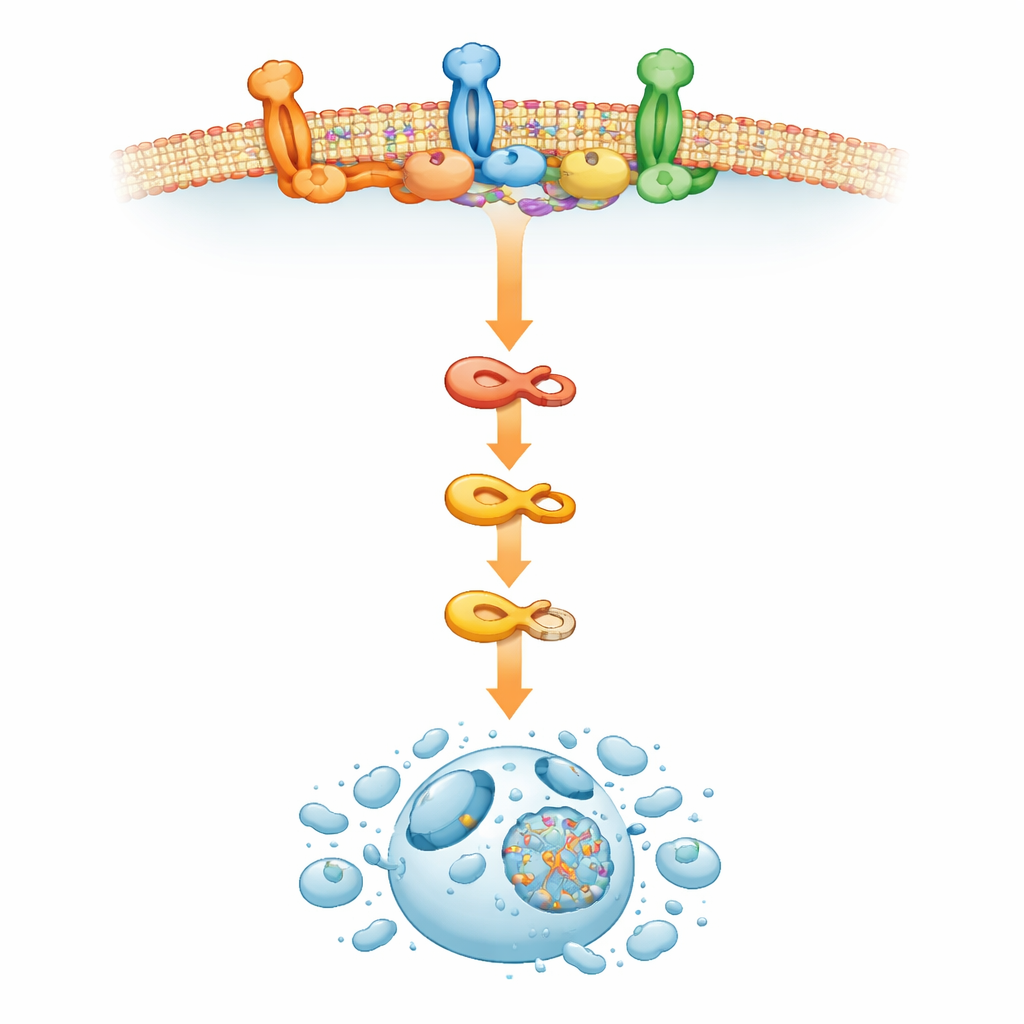
Come le “isole” della membrana cellulare spingono le cellule oltre il limite
Per capire cosa guidasse questa insolita attivazione del macchinario della morte, il gruppo si è concentrato sulla membrana esterna della cellula. Lì, patch specializzate ricche di colesterolo note come rade lipidiche funzionano come piccoli piattaforme di elaborazione dei segnali. Lo studio ha rilevato che l’inibizione di ERAD da parte di RTA408 rimodellava queste rade, causando un accumulo di marcatori di rada e favorendo l’assemblaggio del complesso segnalatore che induce la morte e attiva la caspasi‑8. Quando i ricercatori disturbavano le rade lipidiche o bloccavano la produzione di colesterolo, RTA408 non riusciva più a scatenare la morte cellulare precoce, benché rimanessero i segni di stress interno nella cellula. Ciò indica che, nelle cellule del mieloma, interferire con ERAD manda onde che riorganizzano la membrana, mettendo insieme i componenti della via della morte in modo da spingere la cellula tumorale all’autodistruzione.
Cosa potrebbe significare per i pazienti
In termini semplici, questo lavoro identifica un farmaco approvato che può sabotare selettivamente un fondamentale sistema di manutenzione nelle cellule del mieloma, spingendole verso una forma di morte programmata che dipende dall’organizzazione di proteine e lipidi nella loro membrana esterna. Poiché RTA408 agisce in modo diverso rispetto ai farmaci attuali che bloccano il proteasoma e rimane efficace in cellule resistenti e in modelli animali, offre un promettente nuovo approccio per il trattamento di questo cancro ancora incurabile. Allo stesso tempo, lo studio rivela un collegamento inaspettato tra la macchina interna di controllo qualità e l’organizzazione degli “interruttori di morte” di superficie, aprendo nuove strade per progettare terapie che sfruttino gli stress unici affrontati dalle cellule tumorali produttrici di anticorpi.
Citazione: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
Parole chiave: mieloma multiplo, controllo di qualità delle proteine, degradazione associata al reticolo endoplasmatico, apoptosi via caspasi‑8, rimodulazione di farmaci