Clear Sky Science · de
Kleine Molekül-Screenings identifizieren zytotoxische Inhibitoren des endoplasmatischen retikulums-assoziierten Abbaus bei multiplem Myelom
Eine Schwäche von Krebszellen in ein neues Ziel verwandeln
Das multiple Myelom ist eine Blutkrebserkrankung, die von Plasmazellen ausgeht – den Antikörperfabriken des Körpers. Diese Zellen produzieren ständig Proteine und sind dadurch ungewöhnlich abhängig von einem internen Qualitätskontrollsystem, das fehlgefaltete Proteine erkennt und eliminiert. In dieser Studie wird untersucht, ob diese eingebaute Verwundbarkeit mit einem kleinmolekularen Wirkstoff ausgenutzt werden kann, um Myelomzellen zu töten, auch solche, die nicht mehr auf aktuell verfügbare Therapien ansprechen.
Eine verborgene Aufräumtruppe in überlasteten Krebszellen
Im Inneren jeder Zelle fungiert das endoplasmatische Retikulum als Proteinfertigungsstraße. Werden Proteine fehlerhaft synthetisiert, markiert ein Prozess namens ER-assoziierter Abbau (ERAD) diese Proteine zur Entsorgung und leitet sie an die Abfallverarbeitungsmaschinerie der Zelle weiter. Myelomzellen, die große Mengen von Antikörpern herstellen, sind stark auf ERAD angewiesen, um zu überleben. Bestehende Medikamente, sogenannte Proteasom-Inhibitoren, blockieren den letzten Schritt dieses Entsorgungssystems und haben das Überleben von Patienten verbessert, doch die meisten Tumoren werden schließlich resistent. Deshalb suchten die Forschenden nach Wirkstoffen, die früher in diesem Aufräumprozess eingreifen, direkt am ERAD, in der Hoffnung, Myelomzellen auf eine andere Weise auszuschalten.
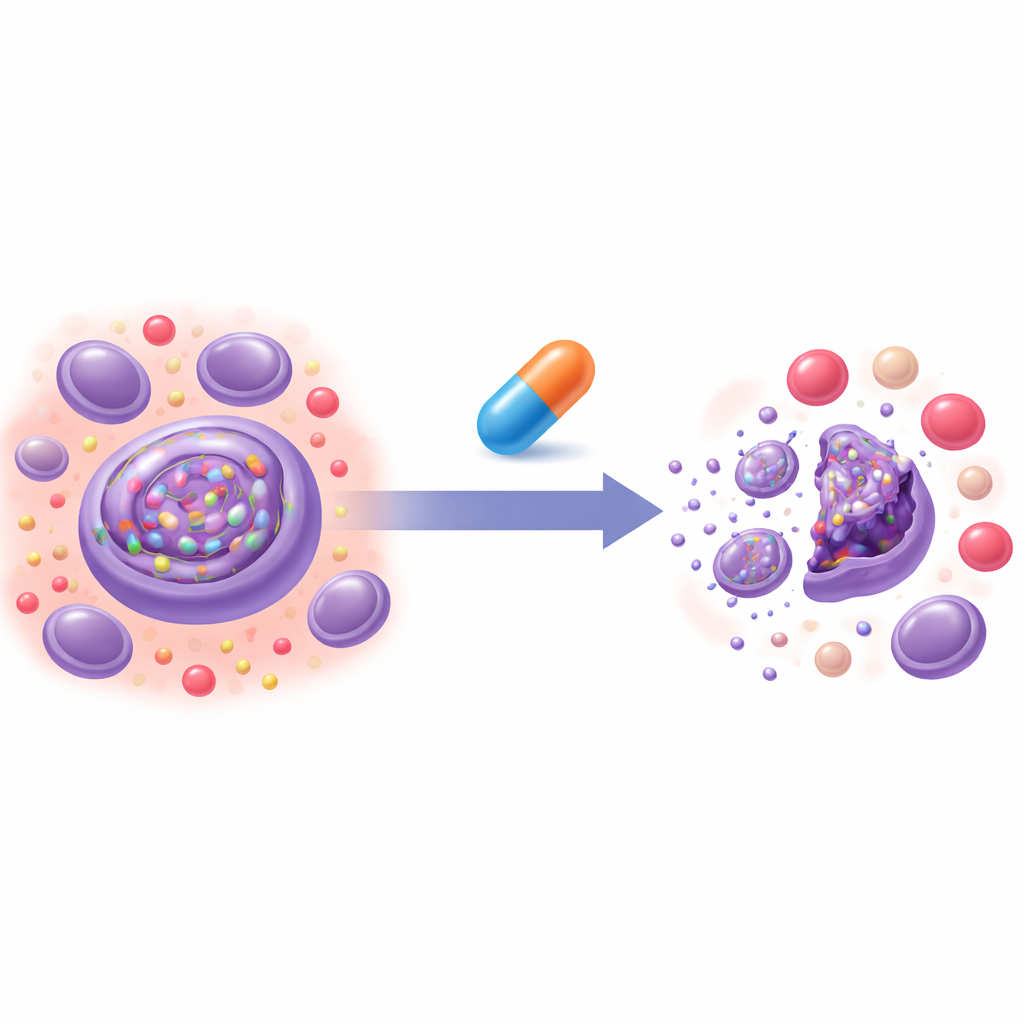
Alte Medikamente für einen neuen Zweck screenen
Das Team entwickelte einen zellbasierten Test, der anzeigt, wie schnell ein Modell-„schlechtes“ Protein durch ERAD abgebaut wird. Mit diesem Assay testeten sie rund 2.200 vorhandene Verbindungen aus einer FDA-Repurposing-Bibliothek. Unter mehreren Kandidaten identifizierten sie Omaveloxolon (auch bekannt als RTA408), ein bereits für eine seltene neurologische Erkrankung zugelassenes Medikament, als einen potenten ERAD-Blocker. RTA408 verlangsamte den Abbau mehrerer Proteine, die normalerweise von ERAD abhängig sind, einschließlich sowohl frei im Zellkompartiment befindlicher Proteine als auch in Membranen eingebetteter Proteine. Gleichzeitig ließ es viele wichtige cytosolische (freischwimmende) Proteine relativ unberührt und störte die Haupt-Proteinentsorgungsmaschinerie der Zelle nicht signifikant, was auf eine fokussierte Wirkung auf das ER-Qualitätskontrollsystem hinweist statt auf einen allgemeinen Stillstand des Proteinumsatzes.
Schnelles, selektives Töten von Myelomzellen
Behandelten die Forschenden eine Reihe von Myelomzelllinien mit RTA408, sank das Überleben der Zellen innerhalb von Stunden deutlich bei niedrigen Wirkstoffkonzentrationen, unabhängig davon, ob die Zellen empfindlich oder resistent gegenüber Proteasom-Inhibitoren waren. Eine verwandte Verbindung, RTA402, zeigte ähnliche Effekte. Wichtig ist, dass die Fähigkeit des Wirkstoffs, Krebszellen zu töten, nicht von seiner bekannten Rolle bei der Aktivierung eines antioxidativen Regulators namens NRF2 abhing, was auf einen bisher unbekannten Wirkmechanismus schließen lässt. In Patientenproben eliminierte RTA408 effizient maligne Plasmazellen sowohl aus neu diagnostizierten als auch aus stark vorbehandelten Individuen, während die meisten T-Zellen und myeloiden Zellen verschont blieben und normale B-Zellen nur mittelstark betroffen waren. Bei Mäusen mit humanen Myelomtumoren verlangsamte wiederholte Gabe von RTA408 das Tumorwachstum deutlich oder verhinderte es, was sein Potenzial als realweltliche Therapie stützt.
Ein unerwarteter Weg zum Zelltod
Da angenommen wurde, dass die Blockade von ERAD Proteinstaus und innerzellulären Stress verursacht, gingen viele Wissenschaftler davon aus, dass der daraus resultierende Zelltod durch einen bekannten Stressweg, die UPR (unfolded protein response), ausgelöst würde. Die Autorinnen und Autoren bestätigten, dass diese Stressantwort nach RTA408-Behandlung aktiviert wurde, doch sorgfältige Experimente zeigten, dass sie nicht der Hauptauslöser für die rasche Welle des Zelltods war. Stattdessen aktivierte der Wirkstoff schnell einen anderen Weg: den sogenannten extrinsischen Todesweg, der normalerweise auf Gefährdungssignale an der Zelloberfläche reagiert. RTA408 schaltete rasch das Enzym Caspase-8 und dessen nachgeschaltete Partner ein; die chemische Hemmung dieser Enzyme oder das Entfernen wichtiger Adapterproteine (FADD und RIPK1) schützte die Zellen vor dem Tod. Überraschenderweise rettete das Entfernen einzelner Todesrezeptoren an der Zelloberfläche die Zellen nicht, was auf eine umfassendere Störung der Organisation dieser Rezeptoren hinweist.
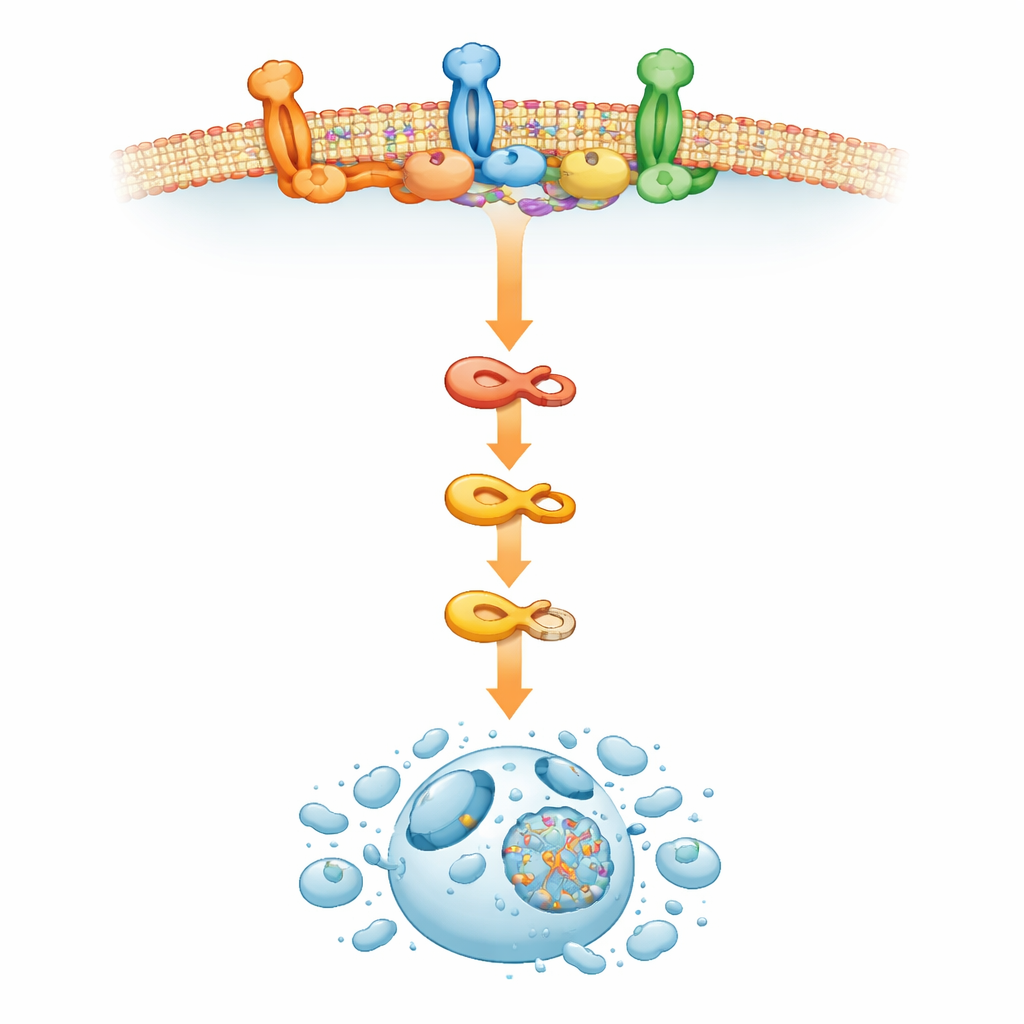
Wie Membran‑„Inseln“ Zellen über die Kante treiben
Um zu verstehen, was diese ungewöhnliche Aktivierung der Todesmaschinerie antrieb, richtete das Team den Blick auf die äußere Zellmembran. Dort dienen spezialisierte cholesterinreiche Bereiche, die als lipid rafts bekannt sind, als winzige Signalverarbeitungsplattformen. Die Studie fand, dass die ERAD-Hemmung durch RTA408 diese Rafts umgestaltete, wodurch sich Raft-Marker ansammelten und die Assemblierung des todesauslösenden Signalkomplexes gefördert wurde, der Caspase-8 aktiviert. Als Forschende lipid rafts störten oder die Cholesterinbildung blockierten, konnte RTA408 den frühen Zelltod nicht mehr auslösen, obwohl Hinweise auf inneren Stress in der Zelle weiterhin vorhanden waren. Das deutet darauf hin, dass die Störung von ERAD in Myelomzellen wellenartige Veränderungen auslöst, die die Membran neu organisieren und so Komponenten des Todeswegs zusammenbringen, wodurch die Krebszelle zur Selbstzerstörung getrieben wird.
Was das für Patientinnen und Patienten bedeuten könnte
Kurz gesagt identifiziert diese Arbeit ein zugelassenes Medikament, das selektiv ein entscheidendes Hausputzsystem in Myelomzellen sabotieren kann und sie in eine Form des programmierten Zelltods treibt, die davon abhängt, wie Proteine und Lipide in ihrer äußeren Membran angeordnet sind. Da RTA408 anders wirkt als die derzeitigen Proteasom‑blockierenden Medikamente und in resistenten Zellen sowie in Tiermodellen wirksam bleibt, bietet es einen vielversprechenden neuen Ansatz zur Behandlung dieses nach wie vor nicht heilbaren Krebses. Gleichzeitig offenbart die Studie eine unerwartete Verbindung zwischen der inneren Qualitätskontrolle der Zelle und der Organisation von oberflächenbasierten „Todes-Schaltern“ und eröffnet neue Wege für die Entwicklung von Therapien, die die speziellen Belastungen ausnutzen, denen antikörperproduzierende Krebszellen ausgesetzt sind.
Zitation: Kropp, E.M., Matono, S., Wang, O.Y. et al. Small molecule screening identifies cytotoxic endoplasmic reticulum-associated degradation inhibitors in multiple myeloma. Cell Death Dis 17, 303 (2026). https://doi.org/10.1038/s41419-026-08526-2
Schlüsselwörter: multiples Myelom, Protein-Qualitätskontrolle, ER-assoziierter Abbau, Caspase-8-Apoptose, Wirkstoff-Neuzuweisung