Clear Sky Science · sv
Framsteg inom icke-faradaiska impedansbiosensorer: strategier för känslighetsförbättring med mikrofluidik, flerskalig märkning och CMOS-teknik
Smartare blodtester på ett chip
Föreställ dig ett medicinskt test som bara kräver ett stick i fingret, ger svar inom några minuter och ryms på en glasyta mindre än ett frimärke. Denna översiktsartikel undersöker hur en viss klass av ”elektroniska näsor” för biologi — kallade icke-faradaiska impedansbiosensorer — snabbt närmar sig den visionen. Genom en smart kombination av små partiklar, mikrofluidiska ledningar och samma chipteknik som används i smartphones förbättrar forskare dessa sensorers känslighet med upp till en miljon gånger, vilket gör det möjligt att upptäcka sjukdomsmarkörer på extremt låga nivåer.
Hur dessa små elektroniska näsor fungerar
I kärnan av dessa sensorer finns mönstrade metallfingrar, kända som interdigitala elektroder, tryckta på glas eller kisel. När ett vätskeprov täcker dem känner elektroderna hur lätt elektrisk laddning byggs upp och omfördelas vid deras yta. Om målmolekyler — till exempel ett protein kopplat till cancer eller en bakterie i förorenat vatten — binder till en preparerad yta mellan elektroderna förändrar de detta elektriska beteende något. Icke-faradaiska sensorer fokuserar på dessa subtila skift i kapacitans och resistans, utan att förlita sig på kemiska reaktioner eller tillsatta färgämnen. Det gör dem enklare, mer robusta och lättare att krympa än många traditionella elektrochemiska eller optiska tester. Men eftersom råsignalen från några få molekyler är mycket liten har känsligheten länge varit det största hindret.
Bygga bättre sensorytor
För att göra dessa chip selektiva täcks metallen och glaset runt elektroderna med noggrant utvalda ytskikt som fungerar som molekylärt kardborreband. På glaslika områden bildar silanmolekyler ultratunna filmer som exponerar kemiska grupper redo att fånga antikroppar, DNA-strängar eller andra biologiska ”krokar”. På guldelektroder fäster svavelinnehållande molekyler i ordnade monoskikt som kan blandas för att styra avstånd, motverka ospecifik bindning och hålla bakgrundssignalen stabil. Nya elektrodesmaterial — såsom grafen, laseretsat poröst kol, ledande polymerer och tvådimensionella föreningar kallade MXener — ökar den effektiva ytan dramatiskt och ändrar hur laddning lagras i gränsskiktet. Dessa avancerade material kan förstärka den elektriska responsen när ett biomolekyl binder, men de riskerar också att lägga till extra brus och isolerande skikt, så ytkemins parametrar måste ställas in mycket noggrant.
Förstärka signaler med partiklar och flöde
En kraftfull strategi är att fästa målmolekylerna vid mikro- eller nanopartiklar. Isolerande pärlor, som plast- eller kiselala kulor, fungerar som stenar i en ström: de blockerar och omdirigerar joniska strömmar nära elektroderna, vilket ökar resistansen och minskar kapacitansen på ett mätbart sätt. Ledande partiklar, särskilt guldnanopartiklar, gör det motsatta: de skapar nya laddningsvägar och heta punkter i det elektriska fältet, vilket ökar kapacitans och minskar resistans. Eftersom en enda pärla är mycket större än ett protein orsakar varje bindningshändelse en mycket större elektrisk förändring — ofta förbättras detektionsgränserna med 10 till 15 gånger eller mer. Mikrofluidiska kanaler tillför ett andra förstärkningslager genom att föra provet över sensorn på ett kontrollerat sätt, snabba upp hur snabbt mål hittar sina bindningsställen och skölja bort löst bundna föroreningar. Kloka konstruktioner med recirkulerande flöde, kapillärdrivna kanaler och finjusterade hydrodynamiska krafter kan koncentrera sällsynta molekyler och rensa bort bakgrundsbrus, vilket sänker detektionsgränserna från nanomolära nivåer mot pikomolära och till och med attomolära nivåer.
Sätta laboratoriet på ett CMOS-chip
Den tredje ingrediensen kommer från den konventionella elektroniken: komplementär metall-oxid-halvledare (CMOS)-teknik. Genom att integrera täta arrayer av interdigitala elektroder direkt på CMOS-chip placerar ingenjörer varje sensorisk ”pixel” bara några mikrometer från ombordgeneratorer och avläsningskretsar. Detta förkortar alla elektriska vägar, dämpar parasitkapacitanser och extern brus. Anpassade kretsar på chippet genererar rena sinusformade testsignaler och separerar sedan sensorresponsernas reella och imaginära delar, eller extraherar direkt magnitud och fas. Moderna designer packar tiotusentals pixlar i en enda enhet, vilket gör det möjligt att övervaka enskilda partiklar, individuella celler eller många olika biomarkörer parallellt. Demonstrerade system kan redan detektera viralt DNA vid attomolära koncentrationer, cancerrelaterade microRNA vid femtomolära nivåer och till och med enskilda bakterier på pixel-för-pixel-basis.
Vart tekniken är på väg
Genom att kombinera partikelmärken, mikrofluidisk kontroll och CMOS-integration har forskare visat att icke-faradaiska impedanssensorer kan mäta sig med eller överträffa mer komplexa elektrochemiska metoder och uppnå kumulativa känslighetsvinster större än en miljonfaldigt. 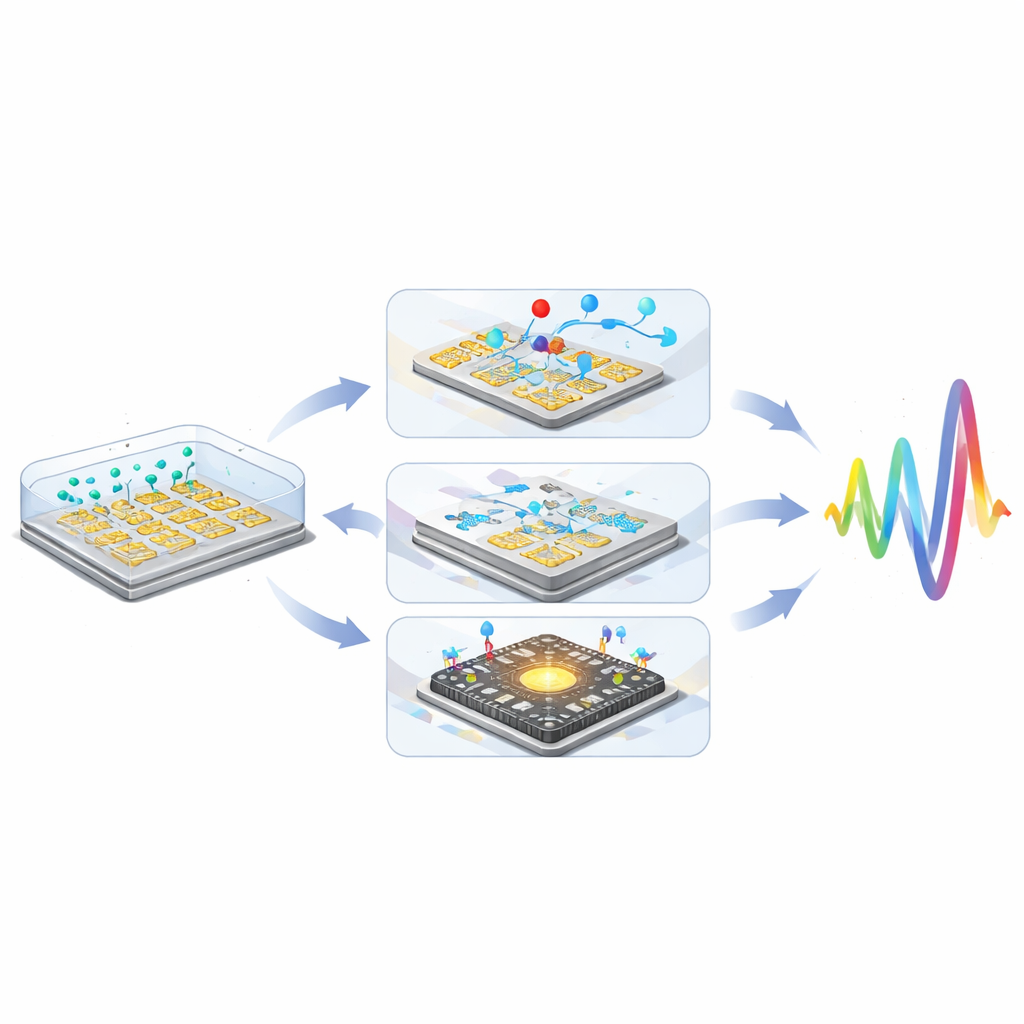
Från forskningschip till verklig diagnostik
Framåtblickande skisserar artikeln en ny generation av ”smart” biosensorer som förenar fysisk ingenjörskonst med avancerade algoritmer och nya material. Tredimensionella elektrodestrukturer och exotiska 2D-material lovar starkare koppling till elektriska fält; mikrofluidisk förkoncentration och separering av blodplasma syftar till att rengöra och berika prov på chipet; och maskininlärningsmodeller tränade på komplexa impedansspektra skulle kunna automatiskt korrigera drift och urskilja subtila sjukdomsmönster. 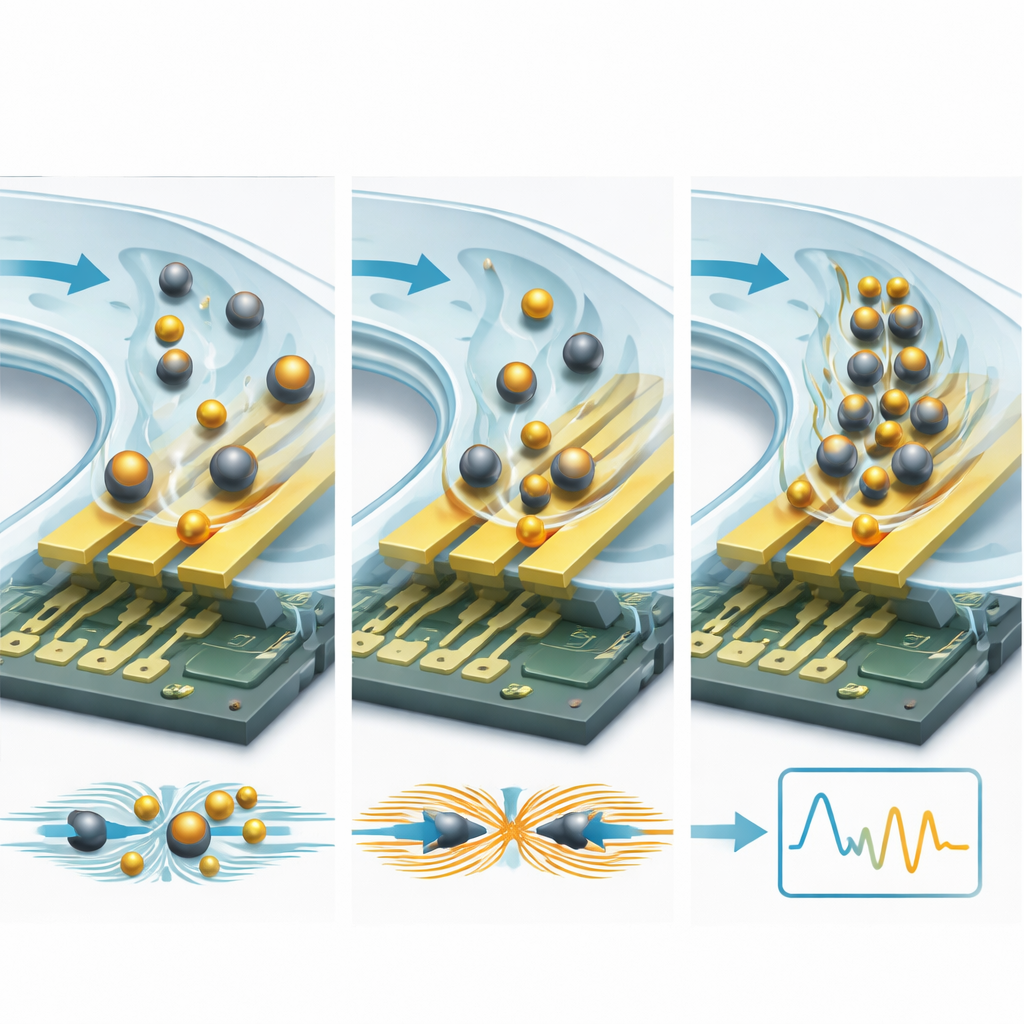
Citering: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Nyckelord: impedansbiosensorer, mikrofluidik, nanopartikelmärkning, CMOS-biosensorer, punktvårdsdiagnostik