Clear Sky Science · nl
Verbetering van niet-faradaïsche impedantie-biosensoren: strategieën voor gevoeligheidsverhoging met microfluidica, multiscale labeling en CMOS-technologie
Slimmere bloedtests op een chip
Stel je een medische test voor die slechts een prikje bloed nodig heeft, binnen enkele minuten een antwoord geeft en op een dun plaatje glas past dat kleiner is dan een postzegel. Dit overzichtsartikel onderzoekt hoe een bepaalde klasse van ‘elektronische neuzen’ voor biologie — genaamd niet-faradaïsche impedantie-biosensoren — snel naar die visie toewerkt. Door slim gebruik te maken van kleine deeltjes, microfluidische leidingen en dezelfde chiptechnologie die in smartphones zit, breken onderzoekers de gevoeligheid van deze sensoren met tot wel een miljoenvoud, waardoor het mogelijk wordt ziektemarkers op uiterst lage concentraties te detecteren.
Hoe deze kleine elektronische neuzen werken
In het hart van deze sensoren bevinden zich gepatroneerde metalen vingertjes, bekend als interdigiterende elektroden, gedrukt op glas of silicium. Wanneer een vloeibaar monster hen bedekt, voelen de elektroden hoe gemakkelijk elektrische lading zich op hun oppervlak opbouwt en herschikt. Binden doelmoleculen — zoals een eiwit geassocieerd met kanker of een bacterie in vervuild water — aan een voorbereide laag tussen de elektroden, dan veranderen ze deze elektrische eigenschappen licht. Niet-faradaïsche sensoren richten zich op die subtiele verschuivingen in capaciteit en weerstand, zonder te steunen op chemische reacties of toegevoegde kleurstoffen. Dat maakt ze eenvoudiger, robuuster en makkelijker te verkleinen dan veel traditionele elektrochemische of optische tests. Maar omdat het ruwe signaal van enkele moleculen klein is, is gevoeligheid lange tijd de belangrijkste drempel geweest.
Betere sensoroppervlakken bouwen
Om deze chips selectief te maken worden metaal en glas rond de elektroden gecoat met zorgvuldig gekozen oppervlaktelagen die als moleculair klittenband werken. Op glasachtige regio’s vormen silaanmoleculen ultradunne films die chemische groepen blootleggen die klaar zijn om antilichamen, DNA-strengen of andere biologische ‘haken’ vast te grijpen. Op gouden elektroden klikken zwavelhoudende moleculen in ordelijke monolagen die kunnen worden gemengd om de tussenruimtes te regelen, niet-specifieke hechting te weerstaan en het achtergrondsignaal stabiel te houden. Nieuwe elektrodematerialen — zoals grafeen, laser-geëtst poreus koolstof, geleidende polymeren en tweedimensionale verbindingen genaamd MXenes — vergroten het effectieve oppervlak aanzienlijk en veranderen hoe lading aan het grensvlak wordt opgeslagen. Deze geavanceerde materialen kunnen de elektrische respons bij biomolecuulbinding versterken, maar ze brengen ook extra ruis en isolerende lagen in, dus de oppervlaktechemie moet zeer nauwkeurig worden afgestemd.
Signaleringen versterken met deeltjes en stroming
Een krachtige strategie is om doelmoleculen aan micro- of nanodeeltjes te koppelen. Isolerende bolletjes, zoals plastic of silica-sferen, werken als stenen in een stroom: ze blokkeren en herleiden ionische stromingen nabij de elektroden, waardoor de weerstand toeneemt en de capaciteit afneemt op een meetbare manier. Geleidende deeltjes, vooral goudnanodeeltjes, doen het tegenovergestelde: ze creëren nieuwe ladingspaden en hotspots in het elektrische veld, verhogen de capaciteit en verlagen de weerstand. Omdat een enkel bolletje veel groter is dan een eiwit, veroorzaakt elk bindingsgebeuren een veel grotere elektrische verandering — vaak een verbetering van de detectielimiet met een factor 10 tot 15 of meer. Microfluidische kanalen voegen een tweede versterkingslaag toe door het monster gecontroleerd over de sensor te voeren, waardoor targets sneller hun bindplaatsen vinden en loszittende verontreinigingen worden weggespoeld. Slimme ontwerpen met recirculerende stroming, capillair aangedreven kanalen en fijn afgestelde hydrodynamische krachten kunnen zeldzame moleculen concentreren en achtergrondruis verwijderen, waardoor detectielimieten van nanomolaire niveaus naar picomolaire en zelfs attomolaire bereiken dalen.
Het lab op een CMOS-chip plaatsen
Het derde ingrediënt komt uit de reguliere elektronica: complementary metal–oxide–semiconductor (CMOS)-technologie. Door dichte arrays van interdigiterende elektroden direct op CMOS-chips te integreren, plaatsen ingenieurs elk sensorisch ‘pixel’ slechts micrometers van ingebouwde signaalgeneratoren en uitleescircuits. Dit verkort elke elektrische route, onderdrukt parasitaire capaciteiten en externe ruis. Aangepaste on-chip schakelingen genereren zuivere sinusoïdale testsignalen en scheiden vervolgens de reële en imaginaire delen van de sensorrespons, of extraheren direct amplitude en fase. Moderne ontwerpen pakken tienduizenden pixels in één apparaat, waardoor het mogelijk wordt individuele deeltjes, afzonderlijke cellen of veel verschillende biomarkers parallel te monitoren. Gedemonstreerde systemen detecteren al viraal DNA op attomolaire concentraties, kankergeassocieerde microRNA’s op femtomolaire niveaus, en zelfs individuele bacteriën pixel voor pixel.
Waar deze technologie naartoe gaat
Door de combinatie van deeltjeslabels, microfluidische controle en CMOS-integratie hebben onderzoekers aangetoond dat niet-faradaïsche impedantie-sensoren kunnen concurreren met of zelfs complexere elektrochemische benaderingen kunnen overtreffen, met cumulatieve gevoeligheidsverbeteringen van meer dan een miljoenvoud. 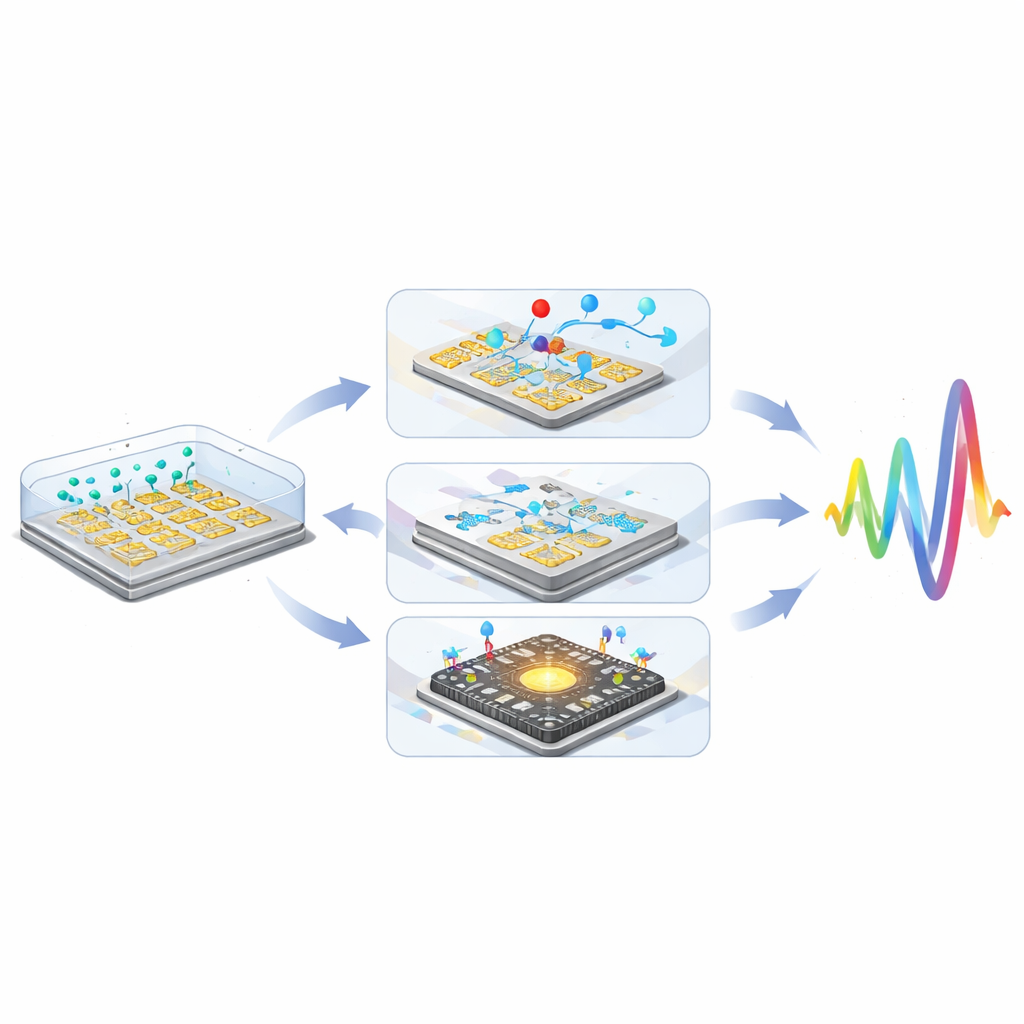
Van onderzoekschips naar diagnostiek in de echte wereld
Vooruitkijkend voorziet het artikel een nieuwe generatie ‘slimme’ biosensoren die fysieke engineering verenigen met geavanceerde algoritmen en nieuwe materialen. Drie-dimensionale elektrodestructuren en exotische 2D-materialen beloven sterkere koppeling met het elektrische veld; microfluidische voorconcentratie en bloed-plasma scheiding zijn bedoeld om monsters on-chip te reinigen en te verrijken; en machine-learningmodellen getraind op complexe impedantiespectra zouden driften automatisch kunnen corrigeren en subtiele ziektepatronen kunnen onderscheiden. 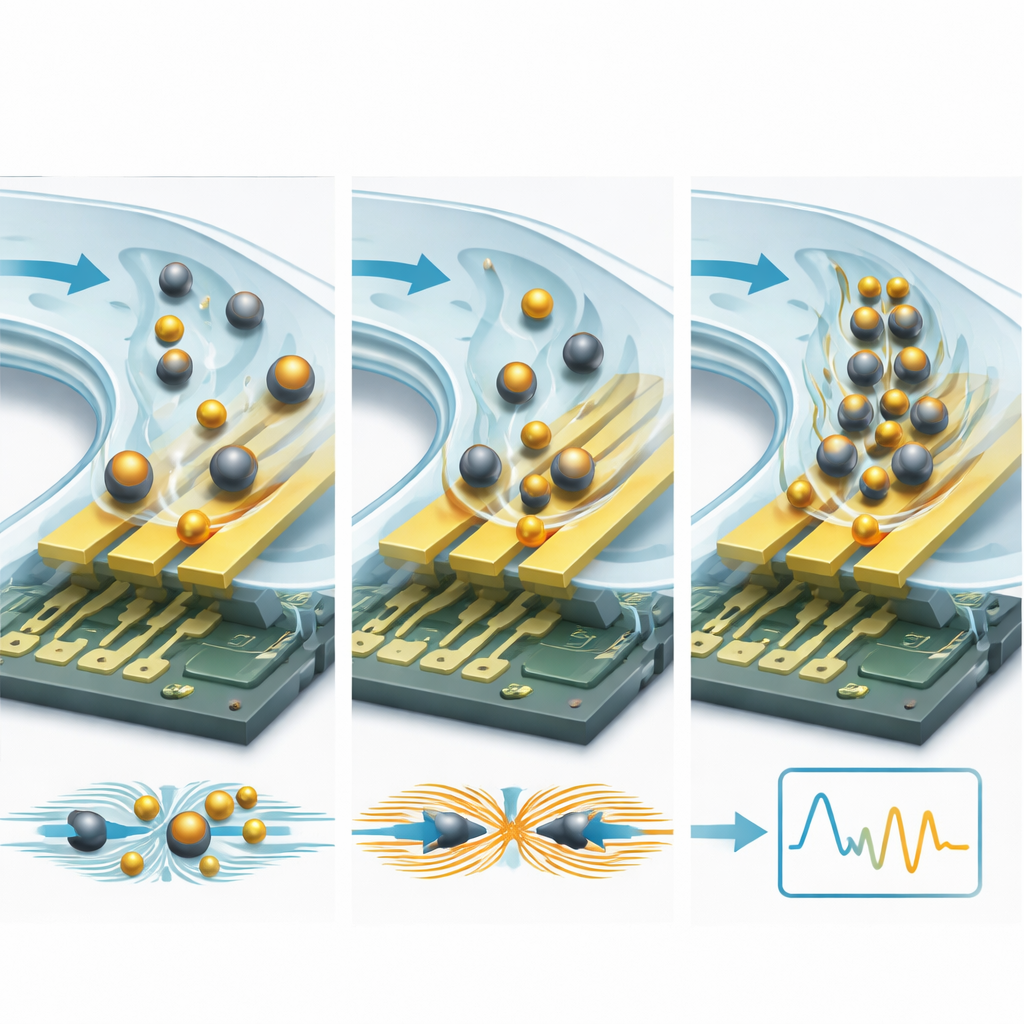
Bronvermelding: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Trefwoorden: impedantie-biosensoren, microfluidica, nanopartikellijning, CMOS-biosensing, point-of-care diagnostiek