Clear Sky Science · it
Avanzare i biosensori di impedenza non-faradaica: strategie per migliorare la sensibilità con microfluidica, marcatura multiscala e tecnologia CMOS
Test del sangue più intelligenti su chip
Immaginate un test medico che richiede solo una goccia di sangue, fornisce risposte in pochi minuti e sta su una lastra di vetro più piccola di un francobollo. Questa review esplora come una particolare classe di “nasi elettronici” per la biologia — chiamati biosensori di impedenza non-faradaici — si stia rapidamente avvicinando a quella visione. Combinando in modo intelligente particelle minuscole, circuiteria microfluidica e la stessa tecnologia a chip usata negli smartphone, i ricercatori stanno aumentando la sensibilità di questi sensori fino a un milione di volte, rendendo possibile rilevare marcatori di malattia a livelli estremamente bassi.
Come funzionano questi piccoli nasi elettronici
Al cuore di questi sensori ci sono dita metalliche stampate, note come elettrodi interdigitati, applicate su vetro o silicio. Quando un campione liquido li ricopre, gli elettrodi percepiscono con quale facilità la carica elettrica si accumula e si riorganizza sulla loro superficie. Se molecole target — come una proteina legata al cancro o un batterio nell’acqua contaminata — si legano a una superficie funzionalizzata tra gli elettrodi, modificano lievemente questo comportamento elettrico. I sensori non-faradaici si concentrano su questi sottili spostamenti di capacitanza e resistenza, senza fare affidamento su reazioni chimiche o coloranti aggiunti. Questo li rende più semplici, più robusti e più facili da miniaturizzare rispetto a molti test elettrochimici o ottici tradizionali. Tuttavia, poiché il segnale grezzo dovuto a poche molecole è minuscolo, la sensibilità è stata a lungo il principale ostacolo.
Costruire superfici sensibili migliori
Per rendere questi chip selettivi, il metallo e il vetro intorno agli elettrodi vengono rivestiti con strati superficiali studiati che agiscono come un Velcro molecolare. Su regioni simili al vetro, molecole silaniche formano film ultra-sottili che espongono gruppi chimici pronti ad agganciare anticorpi, filamenti di DNA o altri “ganci” biologici. Sugli elettrodi d’oro, molecole contenenti zolfo si legano in monostrati ordinati che possono essere miscelati per controllare la spaziatura, resistere all’adesione non specifica e mantenere stabile il segnale di fondo. Nuovi materiali per elettrodi — come grafene, carbonio poroso inciso con laser, polimeri conduttivi e composti bidimensionali chiamati MXene — aumentano drasticamente l’area superficiale effettiva e modificano il modo in cui la carica è immagazzinata all’interfaccia. Questi materiali avanzati possono rafforzare la risposta elettrica quando una biomolecola si lega, ma rischiano anche di aggiungere rumore extra e strati isolanti, quindi la chimica superficiale deve essere messa a punto con molta attenzione.
Amplificare i segnali con particelle e flusso
Una strategia potente è legare le molecole target a micro- o nanoparticelle. Sfere isolanti, come particelle di plastica o silice, agiscono come massi in un ruscello: ostruiscono e deviano le correnti ioniche vicino agli elettrodi, aumentando la resistenza e riducendo la capacitanza in modo misurabile. Le particelle conduttive, in particolare le nanoparticelle d’oro, fanno l’opposto: creano nuovi percorsi di carica e punti caldi nel campo elettrico, incrementando la capacitanza e abbassando la resistenza. Poiché una singola sfera è molto più grande di una proteina, ogni evento di legame provoca un cambiamento elettrico molto più ampio — migliorando spesso i limiti di rilevamento di 10–15 volte o più. I canali microfluidici aggiungono un secondo livello di amplificazione spingendo il campione attraverso il sensore in modo controllato, accelerando la velocità con cui i target trovano i siti di legame e lavando via contaminanti debolmente legati. Progetti ingegnosi che utilizzano flussi ricircolanti, canali a movimento capillare e forze idrodinamiche finemente regolate possono concentrare molecole rare e ridurre il rumore di fondo, abbassando i limiti di rilevamento dalla gamma nanomolare verso livelli picomolari e persino attomolari.
Mettere il laboratorio su un chip CMOS
Il terzo ingrediente proviene dall’elettronica di massa: la tecnologia CMOS (complementary metal–oxide–semiconductor). Integrando dense matrici di elettrodi interdigitati direttamente su chip CMOS, gli ingegneri posizionano ogni “pixel” sensoriale a poche micrometri dai generatori di segnale e dai circuiti di lettura a bordo. Questo accorcia ogni percorso elettrico, sopprimendo le capacitance parassite e il rumore esterno. Circuiti personalizzati on-chip generano segnali di prova sinusoidali puliti e poi separano le parti reale e immaginaria della risposta del sensore, o estraggono direttamente magnitudo e fase. I design moderni impaccano decine di migliaia di pixel in un singolo dispositivo, rendendo possibile monitorare singole particelle, cellule individuali o molti diversi biomarcatori in parallelo. Sistemi dimostrati rilevano già DNA virale a concentrazioni attomolari, microRNA legati al cancro a livelli femtomolari e persino singoli batteri su base pixel-per-pixel.
Dove sta andando questa tecnologia
Combinando marcatori particellari, controllo microfluidico e integrazione CMOS, i ricercatori hanno dimostrato che i sensori di impedenza non-faradaici possono competere o superare approcci elettrochimici più complessi, raggiungendo guadagni di sensibilità cumulativi superiori a un milione di volte. 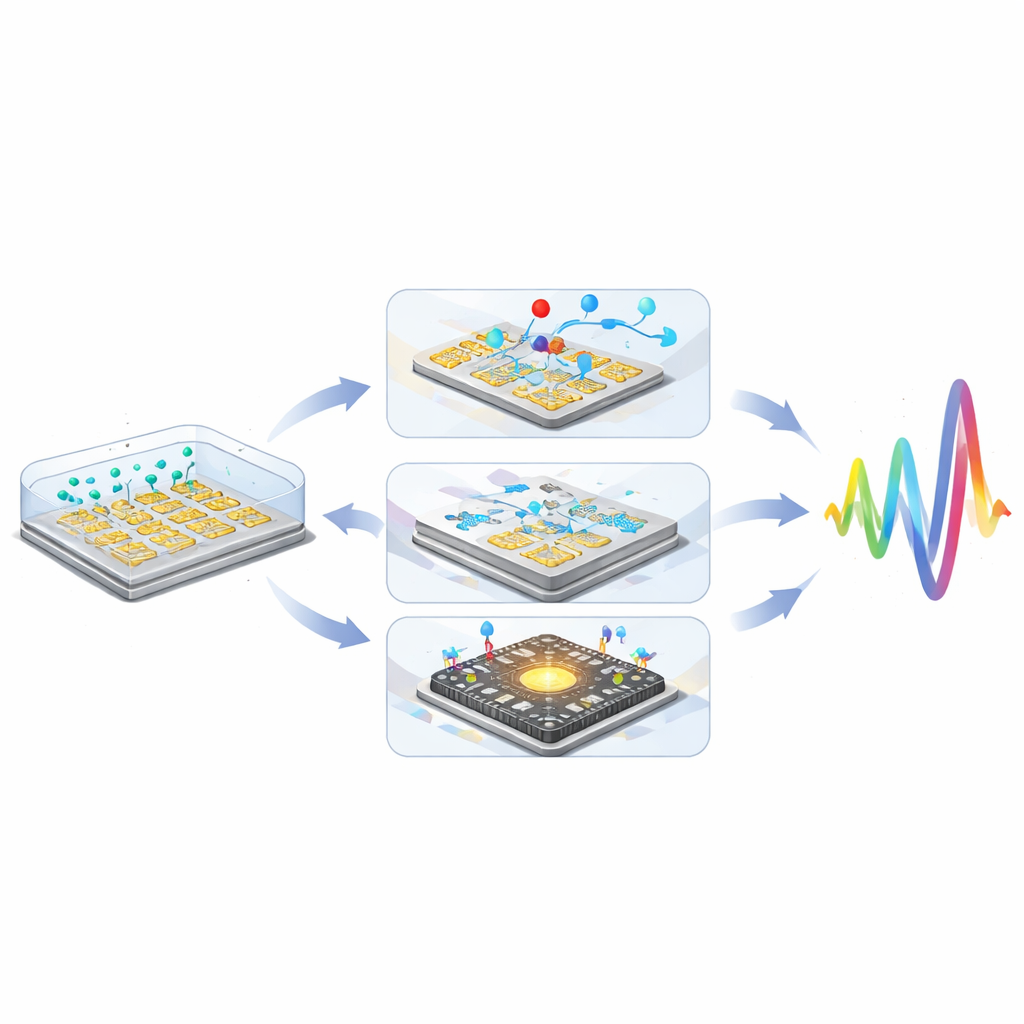
Dai chip di ricerca alla diagnostica del mondo reale
Guardando avanti, l’articolo immagina una nuova generazione di biosensori “intelligenti” che fondono ingegneria fisica con algoritmi avanzati e materiali innovativi. Strutture elettrodiche tridimensionali e materiali 2D esotici promettono un accoppiamento del campo elettrico più forte; preconcentrazione microfluidica e separazione del plasma dal sangue mirano a pulire e arricchire i campioni sul chip; e modelli di apprendimento automatico addestrati su spettri di impedenza complessi potrebbero correggere automaticamente derive e distinguere modelli sottili di malattia. 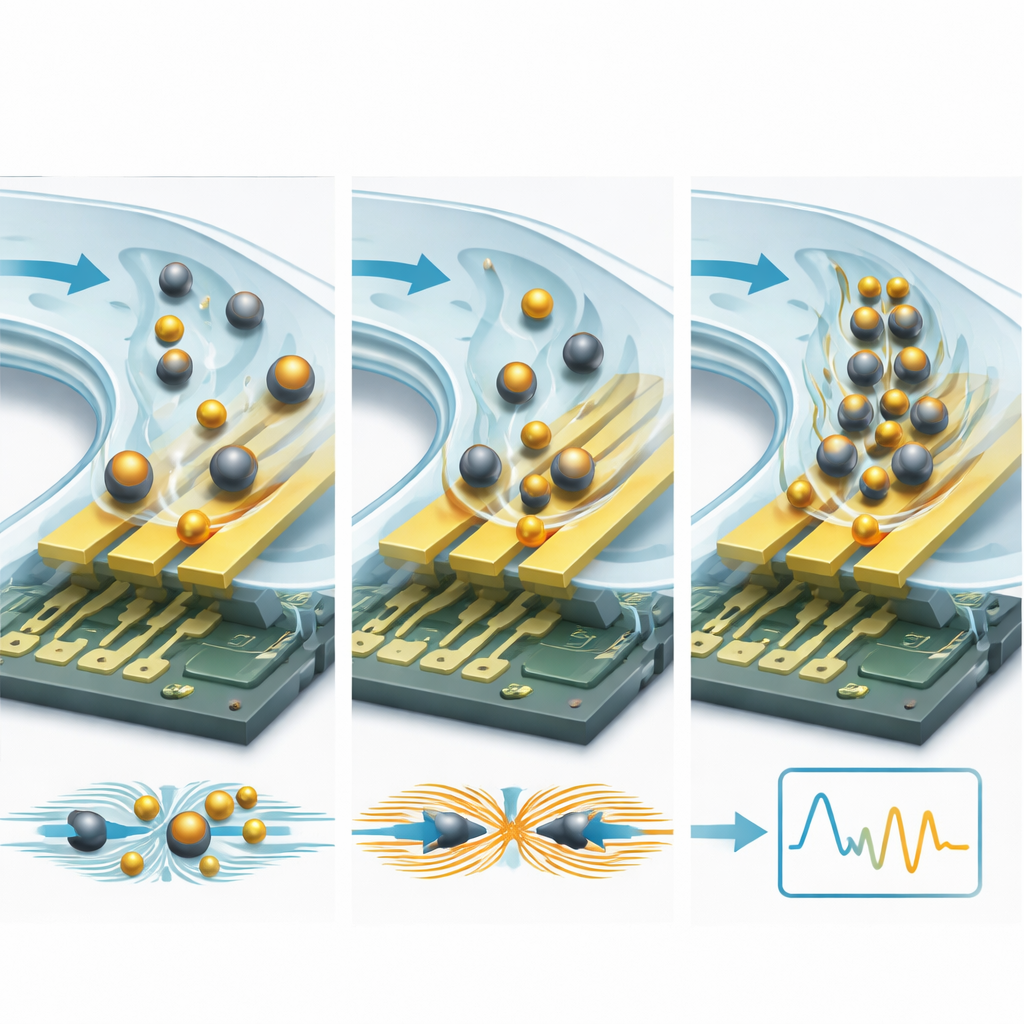
Citazione: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Parole chiave: biosensori di impedenza, microfluidica, marcatura con nanoparticelle, biosensori CMOS, diagnostica point-of-care