Clear Sky Science · he
התקדמות בחיישנים ביולוגיים למדדי התנגדות לא-פראדיים: אסטרטגיות להגברת הרגישות באמצעות מיקרו-נזילות, תיוג רב-קנה מידה וטכנולוגיית CMOS
בדיקות דם חכמות על שבב
דמיינו בדיקה רפואית שדורשת רק עקיצה קטנה של דם, מספקת תשובות תוך דקות ומתאימה על רצועת זכוכית קטנה יותר בחתיכת בול דואר. מאמר סקירה זה בוחן כיצד קבוצה מסוימת של "אף אלקטרוני" ביולוגי — המכונה חיישני התנגדות לא-פראדיים — מתקרבת במהירות לחזון הזה. על ידי שילוב חכם של חלקיקים זעירים, צנרת מיקרו-נזילות וטכנולוגיית השבבים שבה משתמשים בסמארטפונים, חוקרים משפרים את הרגישות של חיישנים אלה בעד סדרי גודל של מיליון, והופכים אפשרי לזהות סמני מחלה ברמות זעירות מאוד.
כיצד עובדים האפים האלקטרוניים הקטנים האלה
בלב החיישנים האלה נמצאות אצבעות מתכת ממוספרות, הידועות כרכיבים אינטרדיגיטטיים, המודפסות על זכוכית או סיליקון. כאשר דוגמה נוזלית מכסה אותן, האלקטרודות חוות כמה קל לטעון ולהסדר מטענים במשטחן. אם מולקולות המטרה — כגון חלבון קשור לסרטן או חיידק במים מזוהמים — נקשרות למשטח מוכוון בין האלקטרודות, הן משנות במעט את ההתנהגות החשמלית הזו. חיישנים לא-פראדיים מתמקדים בשינויים העדינים בקיבול ובמוליכות, מבלי להסתמך על תגובות כימיות או צבעים מוספים. זה הופך אותם לפשוטים יותר, עמידים יותר וקל להקטין אותם לעומת בדיקות אלקטרוכימיות או אופטיות מסורתיות. אך מכיוון שהאות הגולמי ממספר מולקולות בודדות קטן מאוד, הרגישות הייתה עד היום המכשול העיקרי.
שיפור משטחים של חיישנים
כדי לגרום לשבבים אלה להיות סלקטיביים, המתכת והזכוכית סביב האלקטרודות מצופים בשכבות משטח נבחרות בקפידה המתפקדות כמו סקוץ' מולקולרי. באזורי דמויי זכוכית, מולקולות סילאן יוצרות סרטים דקים מאוד שמציגים קבוצות כימיות המוכנות לתפוס נוגדנים, גדילי DNA או "ווים" ביולוגיים אחרים. על אלקטרודות זהב, מולקולות נושאות גופרית מתחברות למונולאיירים מסודרים שניתן לערבב כדי לשלוט ברווחים, לעמוד בפני הידבקות לא-ספציפית ולשמור על יציבות האות ברקע. חומרים חדשים לאלקטרודות — כגון גרפן, פחמן נקבובי שנחרט בלייזר, פולימרים מוליכי-חשמל ומוליכים דו-ממדיים שנקראים MXenes — מגדילים באופן דרמטי את שטח הפנים היעיל ומשנים את אופן אגירת המטען בממשק. חומרים מתקדמים אלה יכולים להעצים את התגובה החשמלית כאשר מולקולת ביולוגיה נקשרת, אך הם גם עלולים להוסיף רעש שכבות מבודדות, ולכן כימיית המשטח חייבת להיות מכוונת בקפידה.
הגברה של אותות באמצעות חלקיקים וזרימה
אסטרטגיה חזקה אחת היא לקשור את מולקולות המטרה לחלקיקים מיקרו- או ננו-חלקיקים. חרוזים מבודדים, כגון כדורי פלסטיק או סיליקה, פועלים כמו סלעים בנחל: הם חוסמים ומעבירים מחדש זרמי יונים סמוך לאלקטרודות, מה שמעלה את ההתנגדות ומפחית את הקיבול באופן מדיד. חלקיקים מוליכי-חשמליים, ובמיוחד ננוחלקיקים מזהב, עושים את ההפך: הם יוצרים מסלולי מטען חדשים ונקודות חמות בשדה החשמלי, מה שמגביר את הקיבול ומפחית את ההתנגדות. מאחר שחרוז בודד גדול בהרבה מחלבון, כל אירוע קשירה יוצר שינוי חשמלי גדול בהרבה — לעתים משפר את סף הזיהוי בעד 10–15 פעם או יותר. ערוצים מיקרו-נזיליים מוסיפים שכבת הגברה שנייה על ידי דחיפת הדוגמה על פני החיישן בצורה מבוקרת, מה שמאיץ את קצב מציאת אתרי הקשירה ושוטף מזהמים המוחזקים ברפיון. עיצובים חכמים שמשתמשים בזרימה מחזרת, ערוצי קפילריות וכוחות הידרודינמיים מכוונים יכולים לרכז מולקולות נדירות ולהסיר רעשי רקע, והורידו את גבולות הגילוי מטווח הננומולרי לקראת פיקומולרי ואפילו אטומולרי.
להכניס את המעבדה על שבב CMOS
המרכיב השלישי מגיע מאלקטרוניקה המיינסטרים: טכנולוגיית CMOS (מוליך-מתכת-תחמוצת משלים). על ידי שילוב מערכי אלקטרודות אינטרדיגיטטיות צפופות ישירות על שבבי CMOS, מהנדסים מציבים כל "פיקסל" חיישני במיקרומטרים ספורים בלבד מהמוליטי-מחוללי האות והמעגלי הקריאה על השבב. זה מקצר כל נתיב חשמלי, מדכא קיבוליות פרועה ורעש חיצוני. מעגלים מותאמים על השבב מייצרים אותות בדיקה סינוסואידליים נקיים ואז מפצלים את החלקים הממשיים והמדוּמיים של תגובת החיישן, או מחלצים ישירות משרעת ושלב. עיצובים מודרניים אורזים עשרות אלפי פיקסלים במכשיר יחיד, מה שמאפשר לנטר חלקיקים בודדים, תאים בודדים או סמנים ביולוגיים רבים במקביל. מערכות שהודגמו כבר מזהות DNA ויראלי בריכוזים אטומולריים, microRNA קשור בסרטן ברמות פמטומרליות ואפילו חיידק יחיד על בסיס פיקסל-פי-פיקסל.
לאן הטכנולוגיה הזו מתקדמת
על ידי שילוב של תוויות חלקיקים, בקרה מיקרו-נזילית ואינטגרציה ב-CMOS, הראו חוקרים שחיישני התנגדות לא-פראדיים יכולים להתחרות או לעלות על גישות אלקטרוכימיות מורכבות יותר, בהשגת שיפורי רגישות מצטברים העולים על סדר גודל של מיליון. 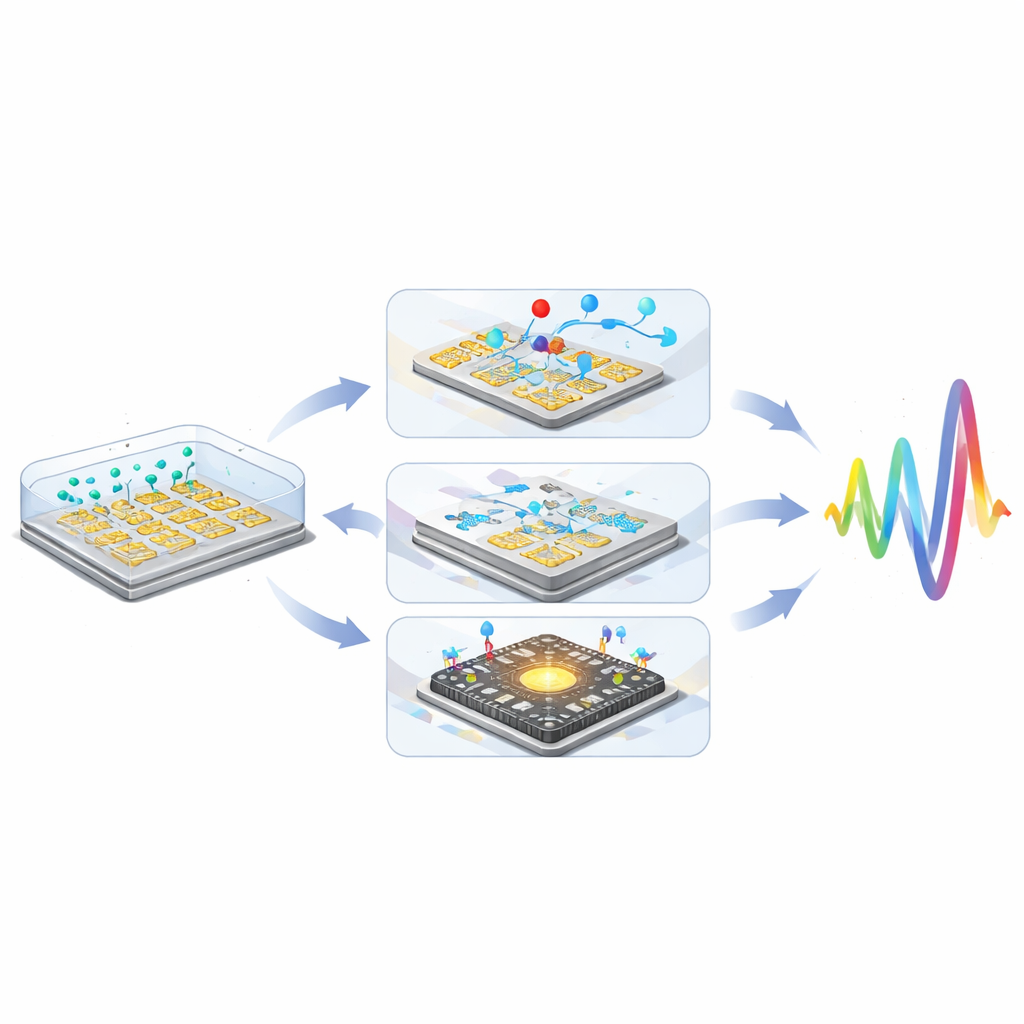
משבבי מחקר לאבחון בעולם האמיתי
מבט קדימה, המאמר צופה דור חדש של חיישנים ביולוגיים "חכמים" הממזגים הנדסה פיזית עם אלגוריתמים מתקדמים וחומרים חדשים. מבני אלקטרודות תלת‑ממדיים וחומרים דו־ממדיים אקזוטיים מבטיחים קפלינג חזק יותר של שדה חשמלי; ריכוז מוקדם מיקרו-נזיליי והפרדת פלזמת דם שואפים לנקות ולהעשר דגימות על השבב; ודגמי למידת מכונה המאומנים על ספקטרות התנגדות מורכבות יוכלו לתקן באופן אוטומטי סטיות ולהבחין בדפוסים מחלתיים עדינים. 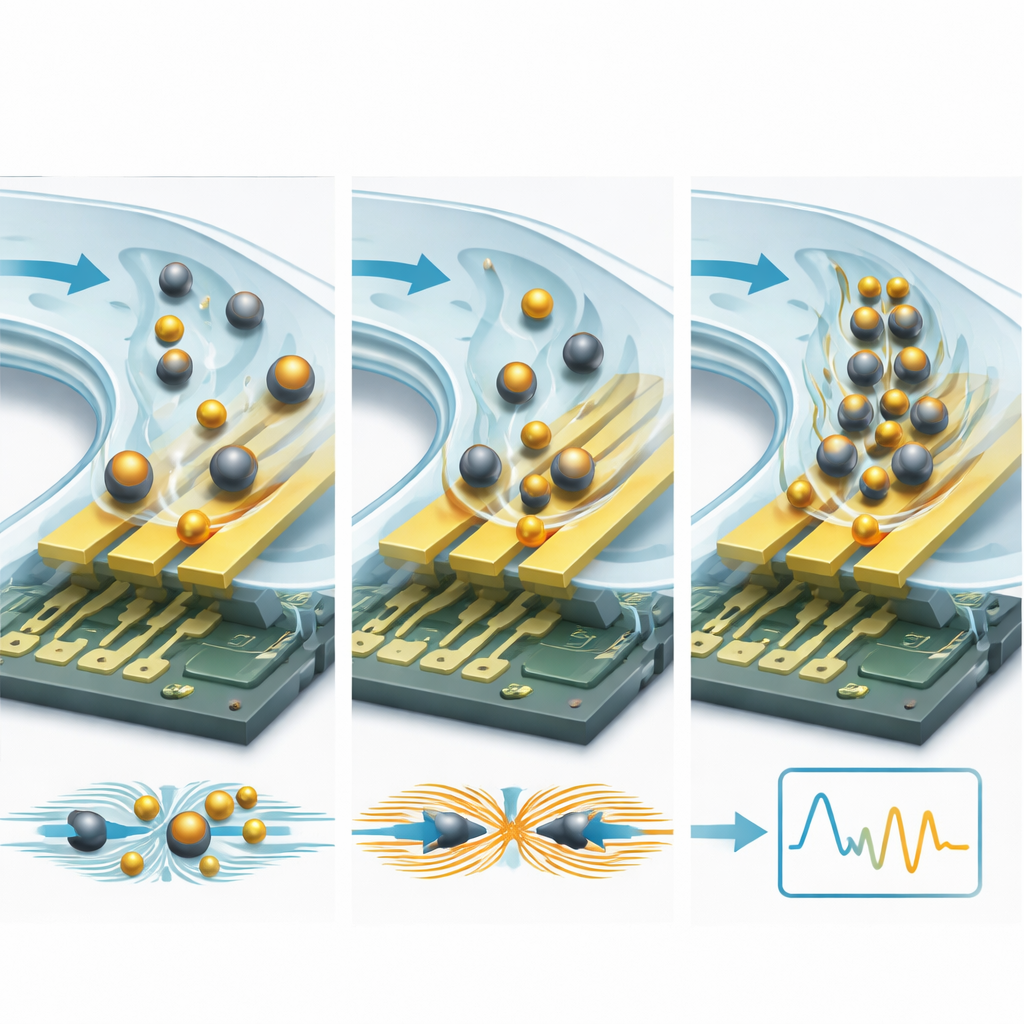
ציטוט: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
מילות מפתח: חיישני התנגדות, מיקרו-נזילות, תיוג בננוחלקיקים, גלאוי CMOS, אבחון ליד המיטה