Clear Sky Science · de
Fortschritte bei nicht-faradayschen Impedanz-Biosensoren: Strategien zur Empfindlichkeitssteigerung mittels Mikrofluidik, multiskaliger Markierung und CMOS-Technologie
Intelligentere Bluttests auf einem Chip
Stellen Sie sich einen medizinischen Test vor, der nur einen Nadelstich Blut benötigt, innerhalb von Minuten Ergebnis liefert und auf einem Glasstreifen kleiner als eine Briefmarke Platz findet. Dieser Übersichtsartikel untersucht, wie eine besondere Klasse biologischer „elektronischer Nasen“ – sogenannte nicht-faradaysche Impedanz-Biosensoren – schnell dieser Vision näherkommt. Durch die clevere Kombination winziger Partikel, mikrofluidischer Leitungen und der gleichen Chip-Technik wie in Smartphones erhöhen Forschende die Empfindlichkeit dieser Sensoren um bis zu eine Millionfach, sodass Krankheitssignale auf verschwindend geringen Konzentrationen nachweisbar werden.
Wie diese winzigen elektronischen Nasen funktionieren
Im Kern dieser Sensoren stehen gemusterte Metallfinger, bekannt als interdigitalisierte Elektroden, die auf Glas oder Silizium gedruckt sind. Bedeckt eine Flüssigkeitsprobe diese Elektroden, messen sie, wie leicht sich elektrische Ladung an ihrer Oberfläche aufbaut und neu anordnet. Binden Zielmoleküle – etwa ein krebsassoziiertes Protein oder ein Bakterium in verunreinigtem Wasser – an eine vorbereitete Fläche zwischen den Elektroden, verändern sie dieses elektrische Verhalten geringfügig. Nicht-faradaysche Sensoren konzentrieren sich auf diese subtilen Verschiebungen in Kapazität und Widerstand, ohne auf chemische Reaktionen oder Farbstoffe zurückzugreifen. Das macht sie einfacher, robuster und leichter zu verkleinern als viele klassische elektrochemische oder optische Tests. Da das Rohsignal von wenigen Molekülen jedoch sehr klein ist, war die Empfindlichkeit lange Zeit das größte Hindernis.
Verbesserung der Sensoroberflächen
Um diese Chips selektiv zu machen, werden Metall und Glas rund um die Elektroden mit sorgsam gewählten Oberflächenschichten überzogen, die wie molekulares Klett wirken. Auf glasähnlichen Regionen bilden Silanmoleküle ultradünne Filme, die chemische Gruppen bereitstellen, um Antikörper, DNA-Stränge oder andere biologische „Haken“ zu binden. Auf Goldelektroden fügen sich schwefelhaltige Moleküle zu geordneten Monolayern zusammen, die gemischt werden können, um Abstände zu steuern, unspezifisches Anhaften zu hemmen und das Hintergrundsignal stabil zu halten. Neue Elektrodenmaterialien – wie Graphen, lasergeätzter poröser Kohlenstoff, leitfähige Polymere und zweidimensionale Verbindungen namens MXene – vergrößern die effektive Oberfläche und verändern, wie Ladung an der Schnittstelle gespeichert wird. Diese fortschrittlichen Materialien können die elektrische Antwort beim Biomolekül-Binden verstärken, bergen jedoch auch das Risiko zusätzlicher Störsignale und isolierender Schichten, weshalb die Oberflächenchemie sehr fein abgestimmt werden muss.
Signalverstärkung mit Partikeln und Strömung
Eine wirkungsvolle Strategie besteht darin, Zielmoleküle an Mikro- oder Nanopartikel zu koppeln. Isolierende Kügelchen, etwa aus Kunststoff oder Siliziumdioxid, wirken wie Steine in einem Bach: Sie blockieren und lenken ionische Ströme in der Nähe der Elektroden um, erhöhen den Widerstand und verringern die Kapazität messbar. Leitfähige Partikel, besonders Goldnanopartikel, bewirken das Gegenteil: Sie schaffen neue Ladungspfade und Hotspots im elektrischen Feld, erhöhen die Kapazität und senken den Widerstand. Da ein einzelnes Kügelchen deutlich größer ist als ein Protein, führt jedes Bindungsereignis zu einer wesentlich größeren elektrischen Veränderung – oft verbessern sich die Nachweisgrenzen um den Faktor 10 bis 15 oder mehr. Mikrofluidische Kanäle fügen eine zweite Verstärkungsebene hinzu, indem sie die Probe kontrolliert über den Sensor treiben, die Geschwindigkeit erhöhen, mit der Targets ihre Bindungsstellen finden, und locker gebundene Kontaminationen wegspülen. Clevere Designs mit Umlaufströmung, kapillargetriebenen Kanälen und fein abgestimmten hydrodynamischen Kräften können seltene Moleküle konzentrieren und Hintergrundrauschen reduzieren, wodurch Nachweisgrenzen vom Nanomolarbereich hinunter zu Pikomolar- und sogar Attomolarkonzentrationen sinken.
Das Labor auf einem CMOS-Chip
Die dritte Zutat stammt aus der Mainstream‑Elektronik: die CMOS-Technologie (komplementärer Metall‑Oxid‑Halbleiter). Durch die Integration dichter Arrays interdigitalisierter Elektroden direkt auf CMOS‑Chips platzieren Ingenieure jeden Sensings‑„Pixel“ nur wenige Mikrometer entfernt von onboard Signalgebern und Ausleseschaltungen. Das verkürzt jede elektrische Strecke und unterdrückt Streukapazitäten sowie externes Rauschen. Spezielle On‑Chip‑Schaltungen erzeugen saubere Sinusprüfsignale und trennen dann die Real‑ und Imaginärteile der Sensorantwort oder extrahieren direkt Magnitude und Phase. Moderne Designs packen Zehntausende Pixel in ein einziges Gerät, sodass es möglich wird, einzelne Partikel, einzelne Zellen oder viele verschiedene Biomarker parallel zu überwachen. Gezeigte Systeme detektieren bereits virale DNA in Attomolarkonzentrationen, krebsassoziierte microRNAs im Femtomolarbereich und sogar einzelne Bakterien pixelweise.
Wohin sich diese Technologie entwickelt
Durch die Kombination von Partikelmarkern, mikrofluidischer Kontrolle und CMOS‑Integration haben Forschende nachgewiesen, dass nicht-faradaysche Impedanzsensoren komplexe elektrochemische Verfahren erreichen oder übertreffen können und kumulative Empfindlichkeitsgewinne von mehr als einer Millionfach erzielen. 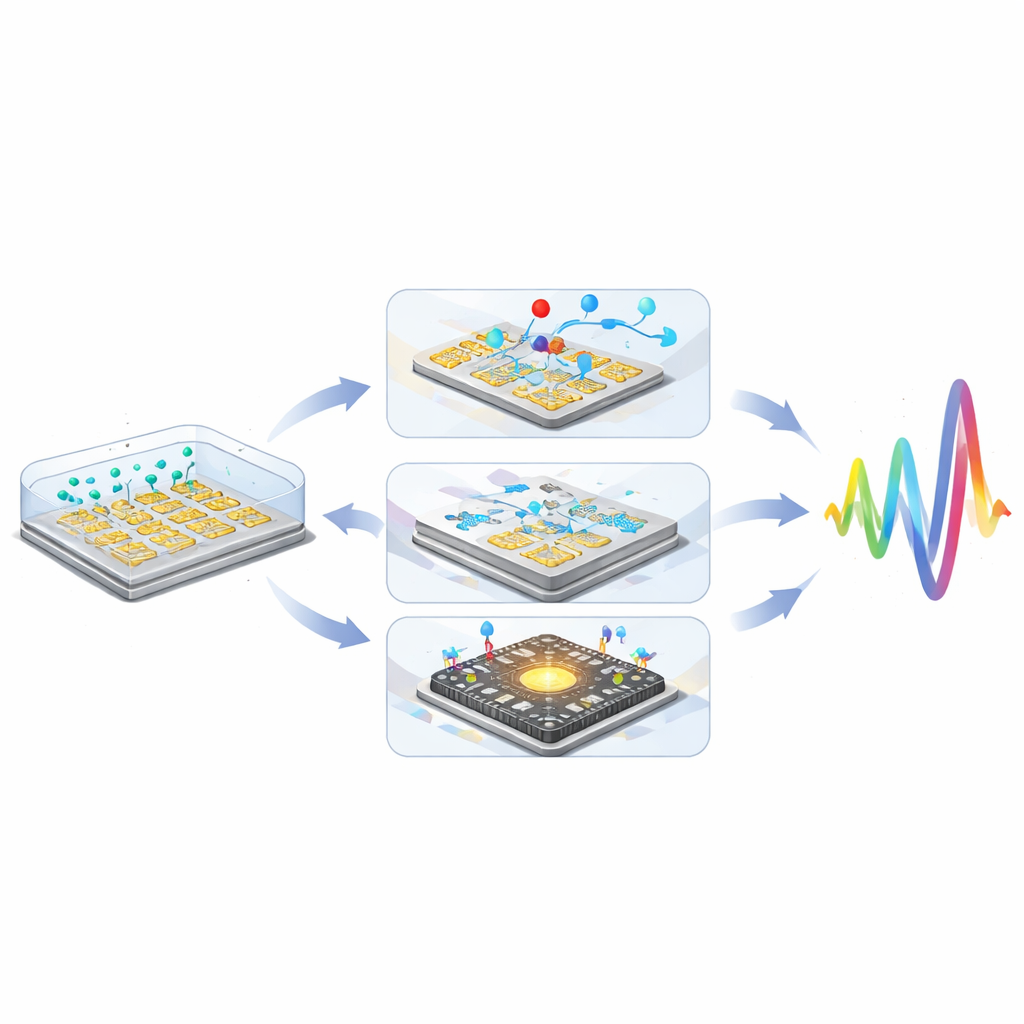
Von Forschungschips zu Diagnostik im Alltag
Mit Blick nach vorn skizziert der Artikel eine neue Generation „intelligenter" Biosensoren, die physikalisches Engineering mit fortschrittlichen Algorithmen und neuartigen Materialien verbinden. Dreidimensionale Elektrodenstrukturen und exotische 2D‑Materialien versprechen stärkere Kopplung an das elektrische Feld; mikrofluidische Vorkonzentration und Blut‑Plasma‑Trennung zielen darauf ab, Proben on‑chip zu reinigen und anzureichern; und maschinelle Lernmodelle, trainiert an komplexen Impedanzspektren, könnten Drift automatisch korrigieren und subtile Krankheitsmuster unterscheiden. 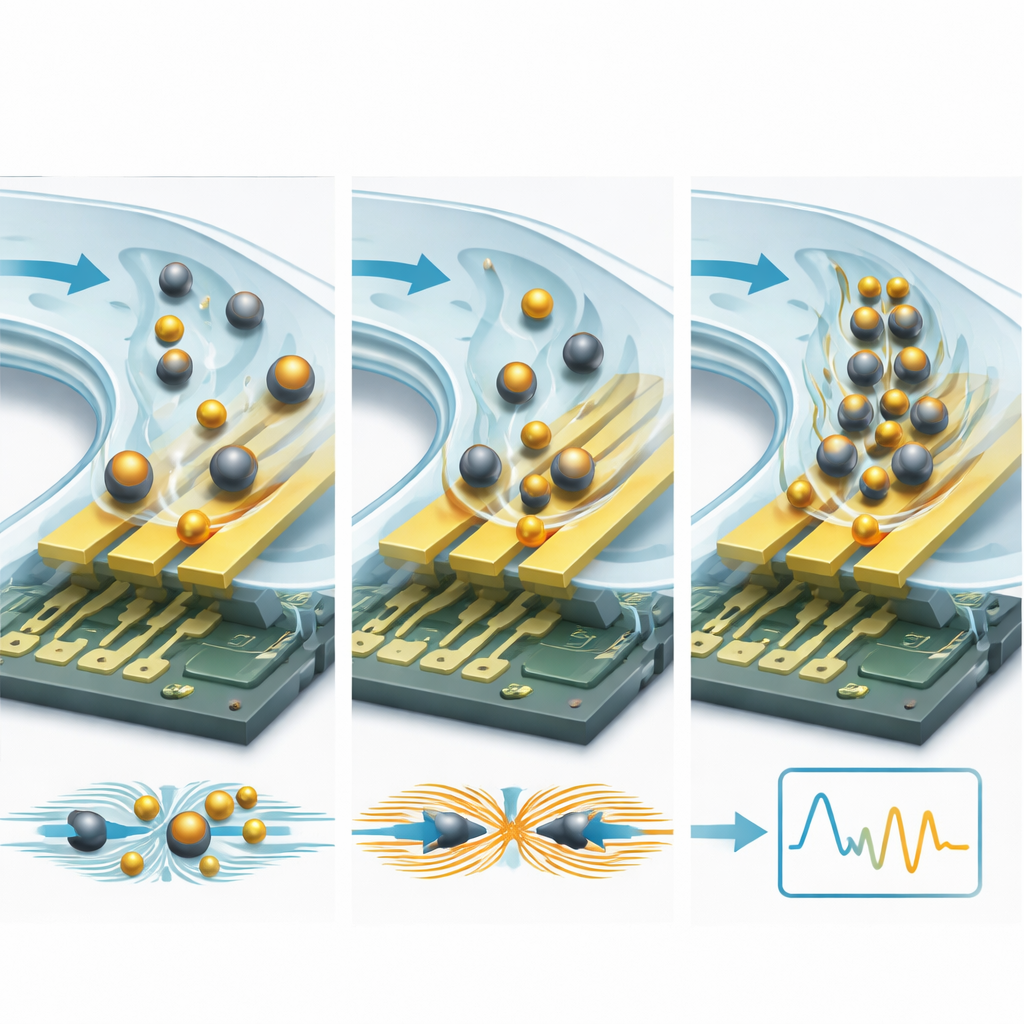
Zitation: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Schlüsselwörter: Impedanz-Biosensoren, Mikrofluidik, Nanopartikel-Markierung, CMOS-Biosensorik, Point-of-Care-Diagnostik