Clear Sky Science · pt
Avanços em biossensores de impedância não faradaicos: estratégias para aumentar sensibilidade usando microfluídica, marcação multiescala e tecnologia CMOS
Exames de sangue mais inteligentes em um chip
Imagine um teste médico que precisa apenas de uma picada no dedo, fornece respostas em minutos e cabe em um fragmento de vidro menor que um selo postal. Este artigo de revisão explora como uma classe particular de “narizes eletrônicos” para a biologia — chamados biossensores de impedância não faradaicos — está rapidamente se aproximando dessa visão. Ao combinar de forma inteligente partículas minúsculas, encanamento microfluídico e a mesma tecnologia de chip usada em smartphones, pesquisadores estão aumentando a sensibilidade desses sensores em até um milhão de vezes, possibilitando detectar marcadores de doença em níveis extremamente baixos.
Como esses minúsculos narizes eletrônicos funcionam
No coração desses sensores estão “dedos” metálicos padronizados, conhecidos como eletrodos interdigitados, impressos em vidro ou silício. Quando uma amostra líquida os cobre, os eletrodos percebem com que facilidade a carga elétrica se acumula e se reorganiza em sua superfície. Se moléculas-alvo — como uma proteína associada ao câncer ou uma bactéria em água contaminada — se ligam a uma superfície preparada entre os eletrodos, elas alteram levemente esse comportamento elétrico. Sensores não faradaicos focalizam essas sutis variações na capacitância e resistência, sem depender de reações químicas ou corantes adicionados. Isso os torna mais simples, mais robustos e mais fáceis de miniaturizar do que muitos testes eletroquímicos ou ópticos tradicionais. Mas, como o sinal bruto de poucas moléculas é ínfimo, a sensibilidade tem sido por muito tempo o principal obstáculo.
Construindo superfícies de sensor melhores
Para tornar esses chips seletivos, o metal e o vidro ao redor dos eletrodos são revestidos com camadas de superfície cuidadosamente escolhidas que atuam como velcro molecular. Em regiões tipo vidro, moléculas de silano formam filmes ultrafinos que expõem grupos químicos prontos para agarrar anticorpos, fitas de DNA ou outros “ganchos” biológicos. Em eletrodos de ouro, moléculas contendo enxofre se encaixam em monocamadas ordenadas que podem ser misturadas para controlar o espaçamento, resistir à aderência inespecífica e manter o sinal de fundo estável. Novos materiais para eletrodos — como grafeno, carbono poroso gravado a laser, polímeros condutores e compostos bidimensionais chamados MXenes — aumentam dramaticamente a área de superfície efetiva e modificam como a carga é armazenada na interface. Esses materiais avançados podem fortalecer a resposta elétrica quando um biomolécula se liga, mas também correm o risco de adicionar ruído extra e camadas isolantes, de modo que a química da superfície deve ser ajustada com muito cuidado.
Amplificando sinais com partículas e fluxo
Uma estratégia poderosa é prender as moléculas-alvo a micro- ou nanopartículas. Esferas isolantes, como contas plásticas ou de sílica, agem como pedras em um riacho: bloqueiam e redirecionam correntes iônicas próximas aos eletrodos, aumentando a resistência e reduzindo a capacitância de maneira mensurável. Partículas condutoras, especialmente nanopartículas de ouro, fazem o oposto: criam novos caminhos de carga e pontos quentes no campo elétrico, aumentando a capacitância e diminuindo a resistência. Como uma única partícula é muito maior que uma proteína, cada evento de ligação provoca uma mudança elétrica muito maior — frequentemente melhorando os limites de detecção em 10 a 15 vezes ou mais. Canais microfluídicos acrescentam uma segunda camada de amplificação ao empurrar a amostra sobre o sensor de forma controlada, acelerando a velocidade com que os alvos encontram seus locais de ligação e lavando contaminantes fracamente aderidos. Projetos engenhosos que usam fluxo de recirculação, canais impulsionados por capilaridade e forças hidrodinâmicas finamente ajustadas podem concentrar moléculas raras e eliminar ruído de fundo, reduzindo limites de detecção da faixa nanomolar para picomolar e até attomolar.
Colocando o laboratório em um chip CMOS
O terceiro ingrediente vem da eletrônica convencional: tecnologia complementar metal-óxido-semicondutor (CMOS). Ao integrar matrizes densas de eletrodos interdigitados diretamente em chips CMOS, engenheiros posicionam cada “pixel” sensorial a apenas micrômetros de geradores de sinais e circuitos de leitura a bordo. Isso encurta todos os caminhos elétricos, suprimindo capacitâncias parasitas e ruído externo. Circuitos customizados no chip geram sinais de teste senoidais limpos e então separam as partes real e imaginária da resposta do sensor, ou extraem diretamente magnitude e fase. Projetos modernos acomodam dezenas de milhares de pixels em um único dispositivo, tornando possível monitorar partículas individuais, células isoladas ou muitos biomarcadores diferentes em paralelo. Sistemas demonstrados já detectam DNA viral em concentrações attomolares, microRNAs relacionados ao câncer em níveis femtomolares e até bactérias únicas pixel a pixel.
Para onde essa tecnologia caminha
Ao combinar rótulos por partículas, controle microfluídico e integração CMOS, pesquisadores demonstraram que sensores de impedância não faradaicos podem rivalizar ou superar abordagens eletroquímicas mais complexas, alcançando ganhos cumulativos de sensibilidade superiores a um milhão de vezes. 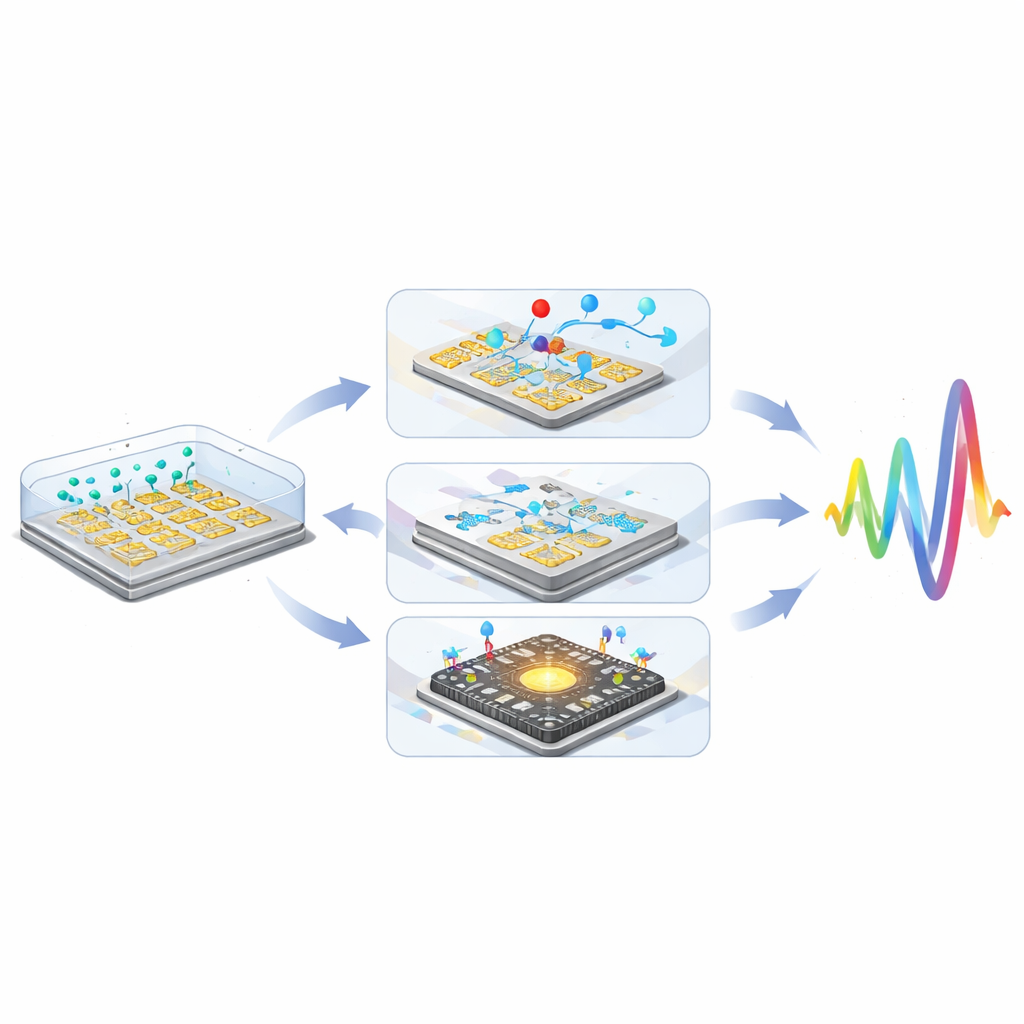
De chips de pesquisa a diagnósticos do mundo real
Olhando adiante, o artigo prevê uma nova geração de biossensores “inteligentes” que unem engenharia física com algoritmos avançados e materiais inovadores. Estruturas de eletrodos tridimensionais e materiais 2D exóticos prometem maior acoplamento do campo elétrico; pré-concentração microfluídica e separação de plasma sanguíneo visam limpar e enriquecer amostras no chip; e modelos de aprendizado de máquina treinados em espectros de impedância complexos poderiam corrigir automaticamente deriva e distinguir padrões sutis de doença. 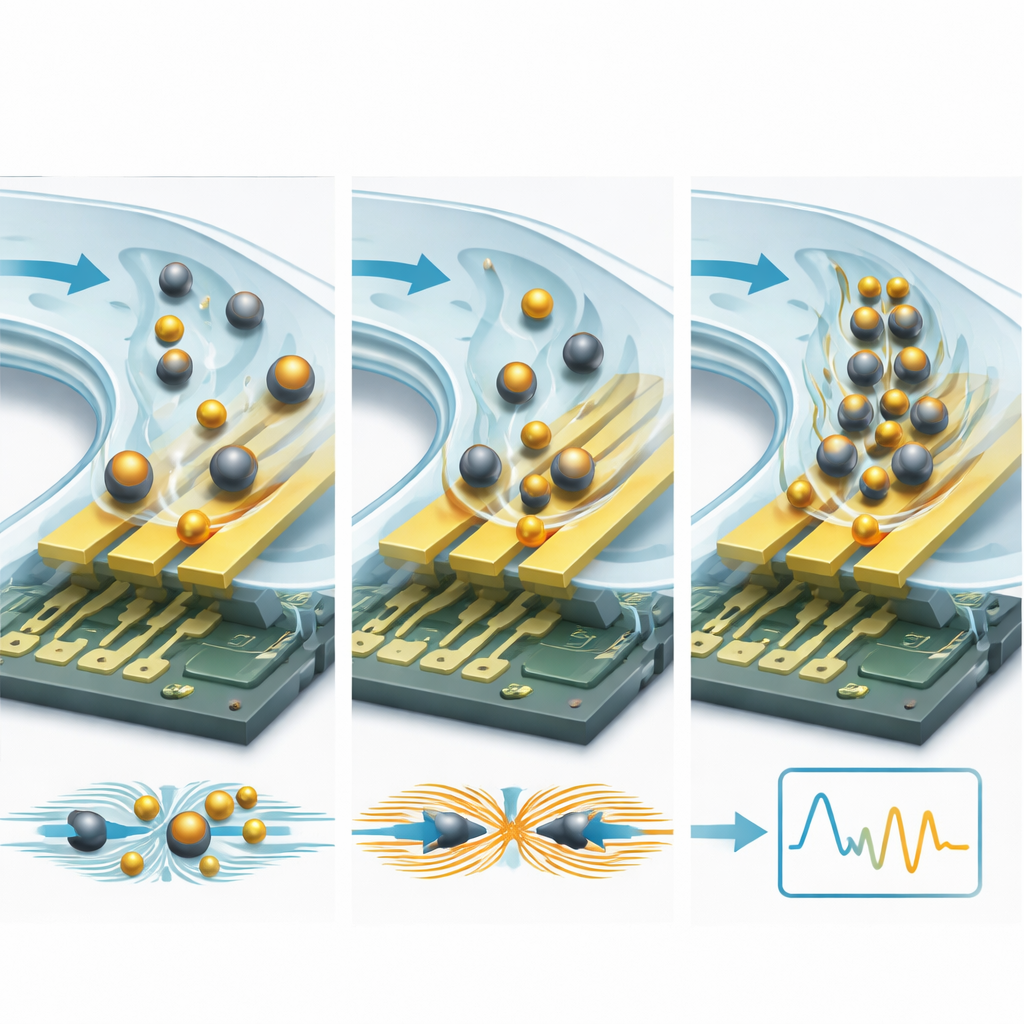
Citação: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Palavras-chave: biossensores de impedância, microfluídica, marcação com nanopartículas, biossensoriamento CMOS, diagnóstico ponto de atendimento