Clear Sky Science · pl
Postępy w niefaradajnych biosensorach impedancyjnych: strategie zwiększania czułości z użyciem mikrofluidyki, oznaczania wieloskalowego i technologii CMOS
Inteligentniejsze testy krwi na chipie
Wyobraź sobie test medyczny, który wymaga jedynie nakłucia palca, daje wyniki w ciągu kilku minut i mieści się na skrawku szkła mniejszym niż znaczek pocztowy. Ten artykuł przeglądowy bada, jak pewna klasa „elektronicznych nosów” biologicznych — zwanych niefaradajnymi biosensorami impedancyjnymi — szybko zbliża się do tej wizji. Dzięki sprytnemu łączeniu maleńkich cząstek, mikrofluidycznych kanałów i tej samej technologii układów scalonych, co w smartfonach, naukowcy zwiększają czułość tych sensorów nawet o milion razy, umożliwiając wykrywanie markerów chorób na bardzo niskich poziomach.
Jak działają te miniaturowe elektroniczne nosy
U podstaw tych sensorów leżą wzorcowane metalowe palce, znane jako elektrody interdyszowe, nadrukowane na szkle lub krzemie. Gdy próbka ciekła je pokrywa, elektrody „odczuwają”, jak łatwo ładunek elektryczny gromadzi się i reorganizuje na ich powierzchni. Jeśli docelowe cząsteczki — na przykład białko związane z rakiem lub bakteria w zanieczyszczonej wodzie — wiążą się z przygotowaną powierzchnią między elektrodami, nieznacznie zmieniają to zachowanie elektryczne. Sensory niefaradajne koncentrują się na tych subtelnych zmianach pojemności i oporu, bez polegania na reakcjach chemicznych czy dodatkowych barwnikach. Dzięki temu są prostsze, bardziej odporne i łatwiejsze do miniaturyzacji niż wiele tradycyjnych testów elektrochemicznych czy optycznych. Jednak surowy sygnał od kilku cząsteczek jest bardzo słaby, dlatego czułość od dawna stanowi główną przeszkodę.
Budowanie lepszych powierzchni sensorów
Aby uczynić te chipy selektywnymi, metal i szkło wokół elektrod pokrywa się starannie dobranymi warstwami powierzchniowymi działającymi jak molekularne rzepy. Na obszarach podobnych do szkła cząsteczki silanowe tworzą ultracienkie warstwy, które eksponują grupy chemiczne gotowe do chwytania przeciwciał, nici DNA lub innych biologicznych „haczykóww”. Na złotych elektrodach związki zawierające siarkę wpinają się w uporządkowane monowarstwy, które można mieszać, aby kontrolować odstępy, zapobiegać niespecyficznemu przywieraniu i utrzymywać stabilne tło sygnału. Nowe materiały elektrodowe — takie jak grafen, laserowo wytrawiany porowaty węgiel, przewodzące polimery oraz dwuwymiarowe związki zwane MXenami — znacząco zwiększają efektywną powierzchnię i zmieniają sposób przechowywania ładunku na granicy faz. Te zaawansowane materiały mogą wzmocnić odpowiedź elektryczną przy wiązaniu biomolekuły, ale równocześnie mogą dodawać dodatkowy szum i warstwy izolujące, dlatego chemię powierzchni trzeba bardzo precyzyjnie dostroić.
Wzmacnianie sygnałów za pomocą cząstek i przepływu
Jedną z potężnych strategii jest przyłączenie celów do mikro- lub nanocząstek. Izolujące kuleczki, takie jak plastikowe lub krzemionkowe sfery, działają jak kamienie w strumieniu: blokują i przekierowują prądy jonowe w pobliżu elektrod, zwiększając opór i obniżając pojemność w mierzalny sposób. Cząstki przewodzące, zwłaszcza nanocząstki złota, robią odwrotnie: tworzą nowe ścieżki dla ładunku i „gorące punkty” w polu elektrycznym, zwiększając pojemność i obniżając opór. Ponieważ pojedyncza kulka jest znacznie większa niż białko, każde wiązanie powoduje dużo większą zmianę elektryczną — często poprawiając granice wykrywania 10–15-krotnie lub więcej. Kanały mikrofluidyczne dodają drugą warstwę wzmocnienia, przesuwając próbkę przez sensor w kontrolowany sposób, przyspieszając, jak szybko cele znajdują miejsca wiązania i spłukując słabo związane zanieczyszczenia. Sprytne projekty wykorzystujące przepływ obiegowy, kanały napędzane kapilarnie i precyzyjnie dobrane siły hydrodynamiczne mogą skoncentrować rzadkie cząsteczki i wyeliminować szumy tła, obniżając granice wykrywania z zakresu nanomolowego w kierunku pikomolowego, a nawet attomolowego.
Umieszczenie laboratorium na układzie CMOS
Trzeci składnik pochodzi z elektroniki użytkowej: technologia komplementarnych metal-tlenek-półprzewodnik (CMOS). Integrując gęste matryce elektrod interdyszowych bezpośrednio na chipach CMOS, inżynierowie umieszczają każdy „piksel” czujnikowy zaledwie kilka mikrometrów od wbudowanych generatorów sygnału i układów odczytowych. To skraca wszystkie ścieżki elektryczne, tłumiąc pojemności pasożytnicze i zewnętrzny szum. Dostosowane układy na chipie generują czyste sinusoidalne sygnały testowe, a następnie rozdzielają części rzeczywiste i urojone odpowiedzi sensora lub bezpośrednio wyciągają wielkość i fazę. Nowoczesne projekty mieszczą dziesiątki tysięcy pikseli w jednym urządzeniu, co umożliwia równoległe monitorowanie pojedynczych cząstek, pojedynczych komórek lub wielu różnych biomarkerów. Pokazane systemy już wykrywają wirusowe DNA w stężeniach attomolowych, mikroRNA związane z rakiem na poziomach femtomolowych, a nawet pojedyncze bakterie piksel po pikselu.
Dokąd zmierza ta technologia
Łącząc znaczniki cząstek, kontrolę mikrofluidyczną i integrację CMOS, badacze wykazali, że niefaradajne sensory impedancyjne mogą konkurować z bardziej złożonymi metodami elektrochemicznymi, osiągając skumulowane przyrosty czułości większe niż milion razy. 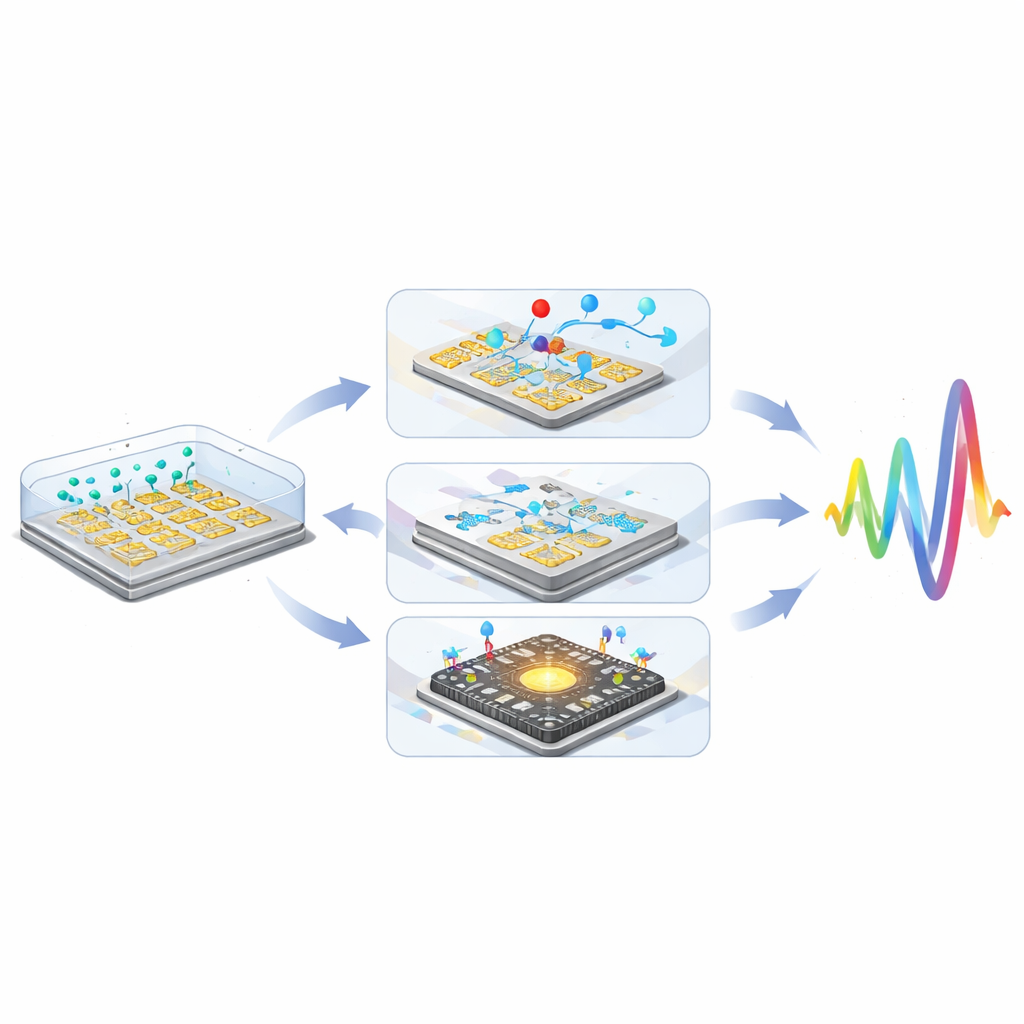
Od chipów badawczych do diagnostyki w świecie rzeczywistym
Spoglądając w przyszłość, artykuł wyobraża sobie nową generację „inteligentnych” biosensorów łączących inżynierię fizyczną z zaawansowanymi algorytmami i nowymi materiałami. Trójwymiarowe struktury elektrod i egzotyczne materiały 2D obiecują silniejsze sprzężenie z polem elektrycznym; mikrofluidyczne wstępne koncentratory i separacja osocza od krwi mają czyścić i wzbogacać próbki na chipie; a modele uczenia maszynowego trenowane na złożonych widmach impedancyjnych mogłyby automatycznie korygować dryfy i rozróżniać subtelne wzorce chorobowe. 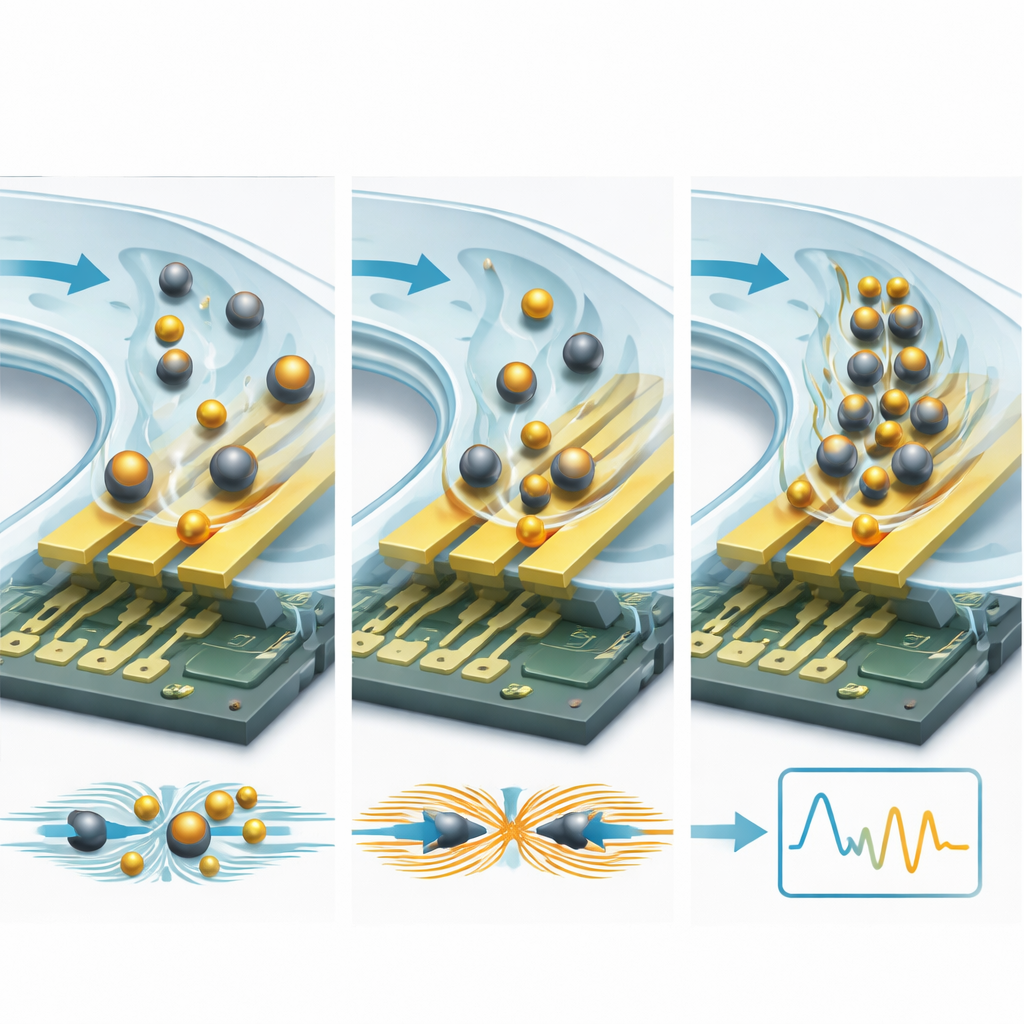
Cytowanie: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Słowa kluczowe: biosensory impedancyjne, mikrofluidyka, oznaczanie nanopomiarowe, biosensory CMOS, diagnostyka przyłóżkowa