Clear Sky Science · fr
Faire progresser les biocapteurs d’impédance non faradaïques : stratégies d’amélioration de la sensibilité utilisant la microfluidique, l’étiquetage multi-échelle et la technologie CMOS
Tests sanguins plus intelligents sur puce
Imaginez un test médical qui ne nécessite qu’une goutte de sang, fournit des résultats en quelques minutes et tient sur un fragment de verre plus petit qu’un timbre-poste. Cet article de synthèse examine comment une catégorie particulière de « nez électroniques » pour la biologie — appelés biocapteurs d’impédance non faradaïques — se rapproche rapidement de cette vision. En combinant astucieusement de petites particules, des réseaux microfluidiques et la même technologie de puce utilisée dans les smartphones, les chercheurs augmentent la sensibilité de ces capteurs jusqu’à un million de fois, rendant possible la détection de marqueurs de maladie à des niveaux extrêmement faibles.
Comment fonctionnent ces petits nez électroniques
Au cœur de ces capteurs se trouvent des doigts métalliques imprimés, appelés électrodes interdigitées, déposés sur du verre ou du silicium. Lorsqu’un échantillon liquide les recouvre, les électrodes détectent la facilité avec laquelle la charge électrique se constitue et se réarrange à leur surface. Si des molécules cibles — comme une protéine liée au cancer ou une bactérie dans de l’eau contaminée — se lient à une surface préparée entre les électrodes, elles modifient légèrement ce comportement électrique. Les capteurs non faradaïques se concentrent sur ces variations subtiles de capacitance et de résistance, sans dépendre de réactions chimiques ou de colorants ajoutés. Cela les rend plus simples, plus robustes et plus faciles à miniaturiser que beaucoup de tests électrochimiques ou optiques traditionnels. Mais parce que le signal brut provenant de quelques molécules est minime, la sensibilité a longtemps constitué le principal obstacle.
Concevoir de meilleures surfaces de capteur
Pour rendre ces puces sélectives, le métal et le verre autour des électrodes sont recouverts de couches de surface soigneusement choisies qui jouent le rôle d’un Velcro moléculaire. Sur les régions verreux, des molécules silanes forment des films ultra-fins exposant des groupes chimiques prêts à capturer des anticorps, des brins d’ADN ou d’autres « crochets » biologiques. Sur les électrodes en or, des molécules porteuses de soufre s’assemblent en monocouches ordonnées qui peuvent être mélangées pour contrôler l’espacement, résister aux adhésions non spécifiques et stabiliser le signal de fond. De nouveaux matériaux d’électrode — tels que le graphène, le carbone poreux gravé au laser, les polymères conducteurs et des composés bidimensionnels appelés MXènes — augmentent considérablement la surface effective et modifient la façon dont la charge est stockée à l’interface. Ces matériaux avancés peuvent renforcer la réponse électrique lorsqu’une biomolécule se lie, mais ils risquent aussi d’ajouter du bruit et des couches isolantes ; la chimie de surface doit donc être ajustée avec beaucoup de soin.
Amplifier les signaux avec des particules et l’écoulement
Une stratégie puissante consiste à attacher les molécules cibles à des micro- ou nanoparticules. Des billes isolantes, comme des sphères en plastique ou en silice, agissent comme des rochers dans un courant : elles bloquent et redirigent les courants ioniques proches des électrodes, augmentant la résistance et diminuant la capacitance de façon mesurable. Les particules conductrices, en particulier les nanoparticules d’or, font l’inverse : elles créent de nouvelles voies de charge et des points chauds dans le champ électrique, augmentant la capacitance et abaissant la résistance. Parce qu’une bille est bien plus grande qu’une protéine, chaque événement de liaison provoque un changement électrique beaucoup plus important — améliorant souvent les limites de détection par un facteur de 10 à 15 ou plus. Les canaux microfluidiques ajoutent une seconde couche d’amplification en faisant circuler l’échantillon sur le capteur de manière contrôlée, accélérant la rencontre des cibles avec leurs sites de liaison et éliminant les contaminants faiblement attachés. Des conceptions ingénieuses utilisant l’écoulement en recirculation, des canaux à capillarité et des forces hydrodynamiques finement réglées peuvent concentrer des molécules rares et éliminer le bruit de fond, réduisant les limites de détection de la gamme nanomolaire vers les picomolaires et même les attomolaires.
Intégrer le laboratoire sur une puce CMOS
Le troisième ingrédient provient de l’électronique grand public : la technologie CMOS (complementary metal–oxide–semiconductor). En intégrant des matrices denses d’électrodes interdigitées directement sur des puces CMOS, les ingénieurs placent chaque « pixel » de détection à seulement quelques micromètres des générateurs de signal et circuits de lecture embarqués. Cela raccourcit tous les trajets électriques, supprimant les capacités parasites et le bruit externe. Des circuits personnalisés sur puce fournissent des signaux de test sinusoïdaux propres puis séparent les parties réelle et imaginaire de la réponse du capteur, ou extraient directement la magnitude et la phase. Les conceptions modernes intègrent des dizaines de milliers de pixels dans un seul dispositif, permettant de surveiller des particules uniques, des cellules individuelles ou de nombreux biomarqueurs en parallèle. Des systèmes démontrés détectent déjà de l’ADN viral à des concentrations attomolaires, des microARN liés au cancer à des niveaux fémtomolaires, et même des bactéries individuelles pixel par pixel.
Vers où va cette technologie
En combinant étiquettes particulaires, contrôle microfluidique et intégration CMOS, les chercheurs ont montré que les capteurs d’impédance non faradaïques peuvent rivaliser avec des approches électrochimiques plus complexes, atteignant des gains de sensibilité cumulatifs supérieurs à un million. 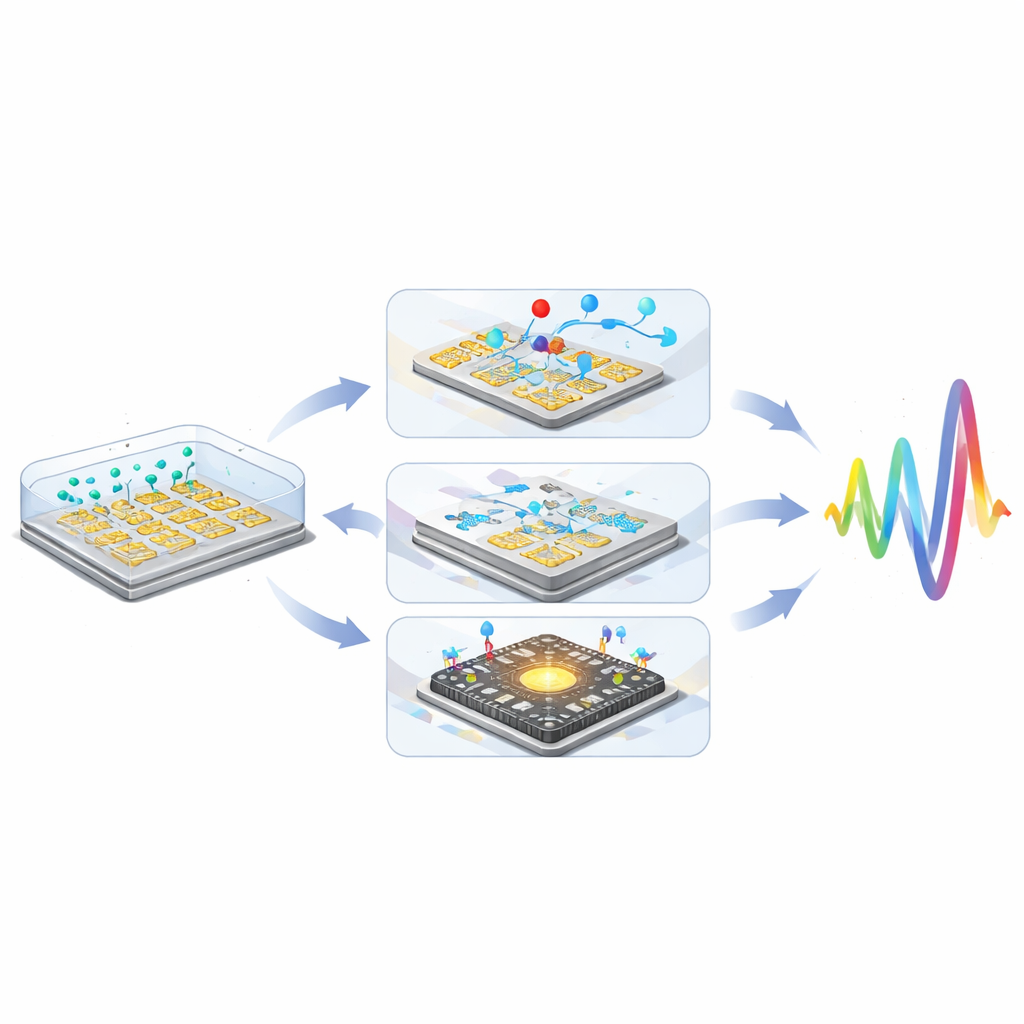
Des puces de recherche aux diagnostics du monde réel
En regardant vers l’avenir, l’article envisage une nouvelle génération de biocapteurs « intelligents » qui fusionnent l’ingénierie physique, des algorithmes avancés et des matériaux innovants. Des structures d’électrodes tridimensionnelles et des matériaux 2D exotiques promettent un couplage champ-électrique plus fort ; la préconcentration microfluidique et la séparation plasma-sang visent à nettoyer et enrichir les échantillons sur puce ; et des modèles d’apprentissage automatique entraînés sur des spectres d’impédance complexes pourraient corriger automatiquement les dérives et distinguer des signatures subtiles de maladie. 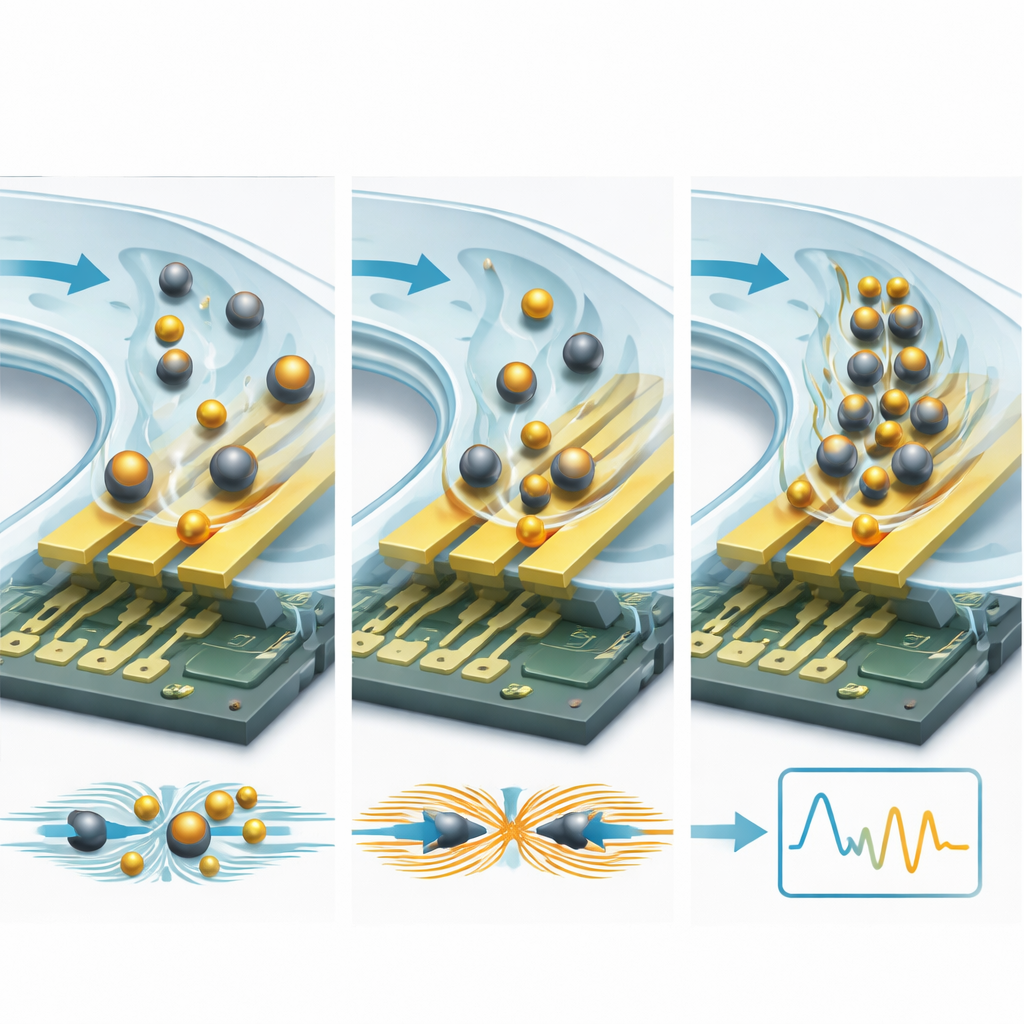
Citation: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Mots-clés: biocapteurs d’impédance, microfluidique, étiquetage par nanoparticules, détection CMOS, diagnostic au point de soin