Clear Sky Science · ru
Продвижение необратных (non-faradaic) импедансных биосенсоров: стратегии повышения чувствительности с использованием микрофлюидики, многомасштабной маркировки и технологии CMOS
Умные анализы крови на чипе
Представьте медицинский тест, которому требуется лишь укол крови, результаты появляются за считанные минуты, а сам тест помещается на кусочек стекла меньше почтовой марки. В этом обзоре рассматривается класс «электронных носов» для биологии — так называемые необратные (non-faradaic) импедансные биосенсоры — и то, как они быстро приближаются к этой картине. За счёт хитроумного сочетания крошечных частиц, микрофлюидной разводки и той же чиповой технологии, что используется в смартфонах, исследователи повышают чувствительность этих сенсоров порой до миллиона раз, что делает возможным обнаружение маркеров заболеваний на крайне низких концентрациях.
Как работают эти крошечные «электронные носы»
В основе таких сенсоров — узорчатые металлические «пальцы», известные как межпальцевые электроды, напечатанные на стекле или кремнии. Когда образец жидкости покрывает их, электроды «ощущают», как легко на их поверхности накапливаются и перераспределяются заряды. Если целевые молекулы — например белок, связанный с раком, или бактерия в загрязнённой воде — связываются с подготовленной поверхностью между электродами, они слегка изменяют это электрическое поведение. Необратные сенсоры фокусируются на тонких сдвигах в ёмкости и сопротивлении, не полагаясь на химические реакции или добавленные красители. Это делает их проще, надёжнее и легче масштабируемыми по сравнению со многими традиционными электрохимическими или оптическими тестами. Однако сырой сигнал от нескольких молекул очень слаб, поэтому чувствительность долгое время была главным ограничением.
Создание лучших чувствительных поверхностей
Чтобы сделать чипы селективными, металл и стекло вокруг электродов покрывают тщательно подобранными поверхностными слоями, действующими как молекулярный велкро. На стекловидных областях с помощью силановых молекул формируются ультратонкие плёнки, раскрывающие химические группы, готовые захватить антитела, молекулы ДНК или другие биологические «зацепки». На золотых электродах серосодержащие молекулы образуют упорядоченные мономолекулярные слои, которые можно смешивать для контроля пространственного распределения, сопротивления неспецифическому прилипанию и стабилизации фонового сигнала. Новые материалы электродов — такие как графен, лазерно-травлёный пористый углерод, проводящие полимеры и двумерные соединения MXene — значительно увеличивают эффективную площадь поверхности и меняют способ хранения заряда на интерфейсе. Эти продвинутые материалы могут усиливать электрическую реакцию при связывании биомолекулы, но они также могут вносить дополнительный шум и изолирующие слои, поэтому химия поверхности должна быть настроена очень аккуратно.
Усиление сигналов с помощью частиц и потока
Одна из эффективных стратегий — присоединять целевые молекулы к микро- или наночастицам. Изолирующие шарики, такие как пластиковые или кремнезёмные сферы, ведут себя как камни в струе: они блокируют и перенаправляют ионные токи возле электродов, увеличивая сопротивление и снижая ёмкость в измеряемой степени. Проводящие частицы, особенно золотые наночастицы, действуют наоборот: они создают новые пути тока и «горячие точки» в электрическом поле, увеличивая ёмкость и уменьшая сопротивление. Поскольку одна частица намного крупнее белка, каждое событие связывания вызывает гораздо более заметное электрическое изменение — часто улучшая пороги обнаружения в 10–15 раз и более. Микрофлюидные каналы добавляют второй уровень усиления, проталкивая образец через сенсор контролируемым образом, ускоряя поиск участков связывания целью и смывая слабо связанные загрязнения. Искусно спроектированные схемы с рециркулирующим потоком, капиллярно-управляемыми каналами и тонко настроенными гидродинамическими силами могут концентрировать редкие молекулы и отфильтровывать фоновый шум, снижая пределы обнаружения с наномолярного уровня к пикoмолярному и даже аттомолярному.
Лаборатория на CMOS-чипе
Третьим ингредиентом является массовая электроника: технология комплементарных металл-оксид-полупроводников (CMOS). Интегрируя плотные матрицы межпальцевых электродов прямо на CMOS-чипы, инженеры размещают каждую сенсорную «пиксель» в нескольких микрометрах от встроенных генераторов сигналов и схем считывания. Это сокращает длину электрических путей, подавляет паразитные ёмкости и внешний шум. Специализированные он-чип схемы генерируют чистые синусоидальные тестовые сигналы, затем разделяют действительную и мнимую части отклика сенсора или напрямую извлекают величину и фазу. Современные разработки собирают десятки тысяч пикселей в одном устройстве, что позволяет одновременно отслеживать отдельные частицы, индивидуальные клетки или множество разных биомаркеров. Демонстрированные системы уже обнаруживают вирусную ДНК на аттомолярных концентрациях, связанные с раком микроРНК на фемтомолярных уровнях и даже отдельные бактерии на уровне отдельного пикселя.
Куда движется эта технология
Сочетая маркировку частицами, управление микрофлюдикой и интеграцию CMOS, исследователи показали, что необратные импедансные сенсоры могут соперничать с более сложными электрохимическими подходами и даже превосходить их, достигая суммарных приростов чувствительности более чем в миллион раз. 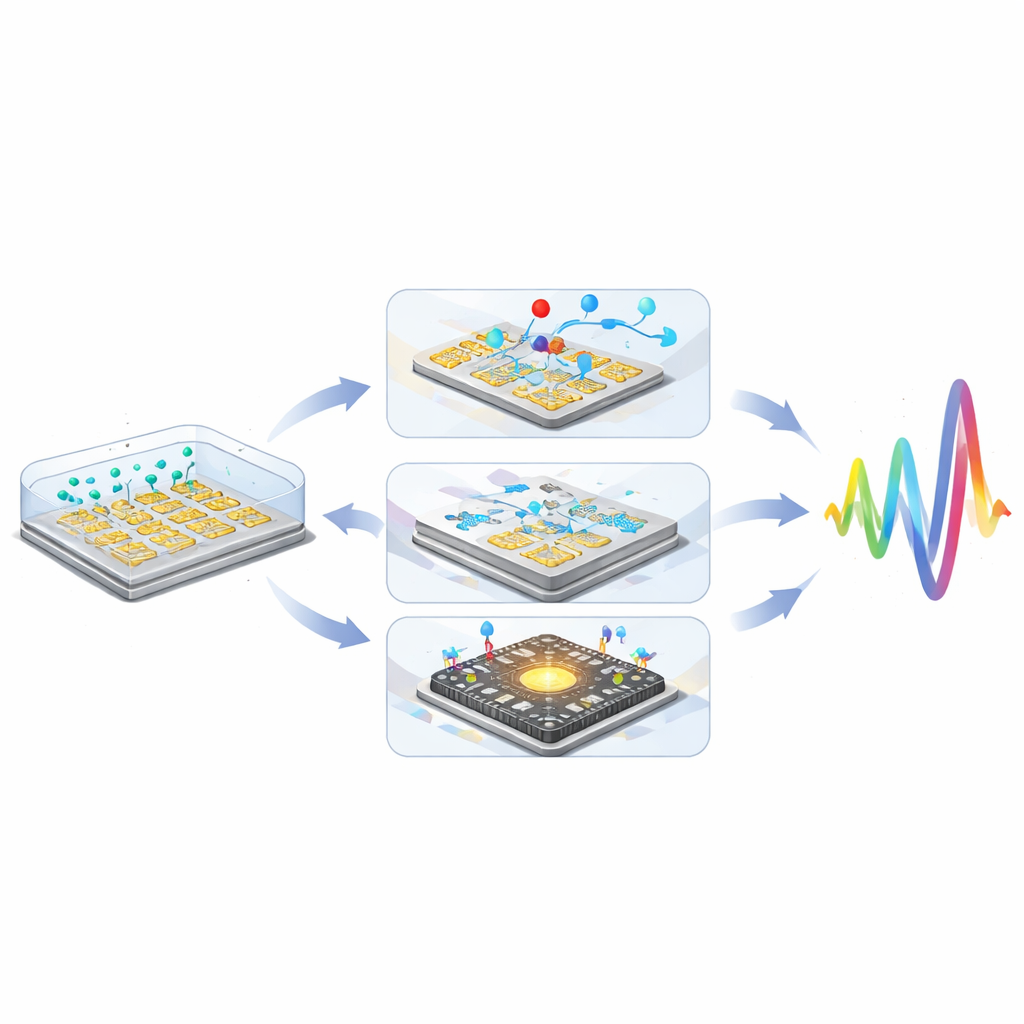
От исследовательских чипов к реальной диагностике
Смотрев в будущее, статья представляет поколение «умных» биосенсоров, которые объединяют физическое проектирование с продвинутыми алгоритмами и новыми материалами. Трёхмерные структуры электродов и экзотические двумерные материалы обещают более сильное электронное поле; микрофлюидное предконцентрирование и разделение плазмы крови на чипе призваны очищать и обогащать образцы; а модели машинного обучения, обученные на сложных спектрах импеданса, смогут автоматически корректировать дрейф и распознавать тонкие паттерны заболеваний. 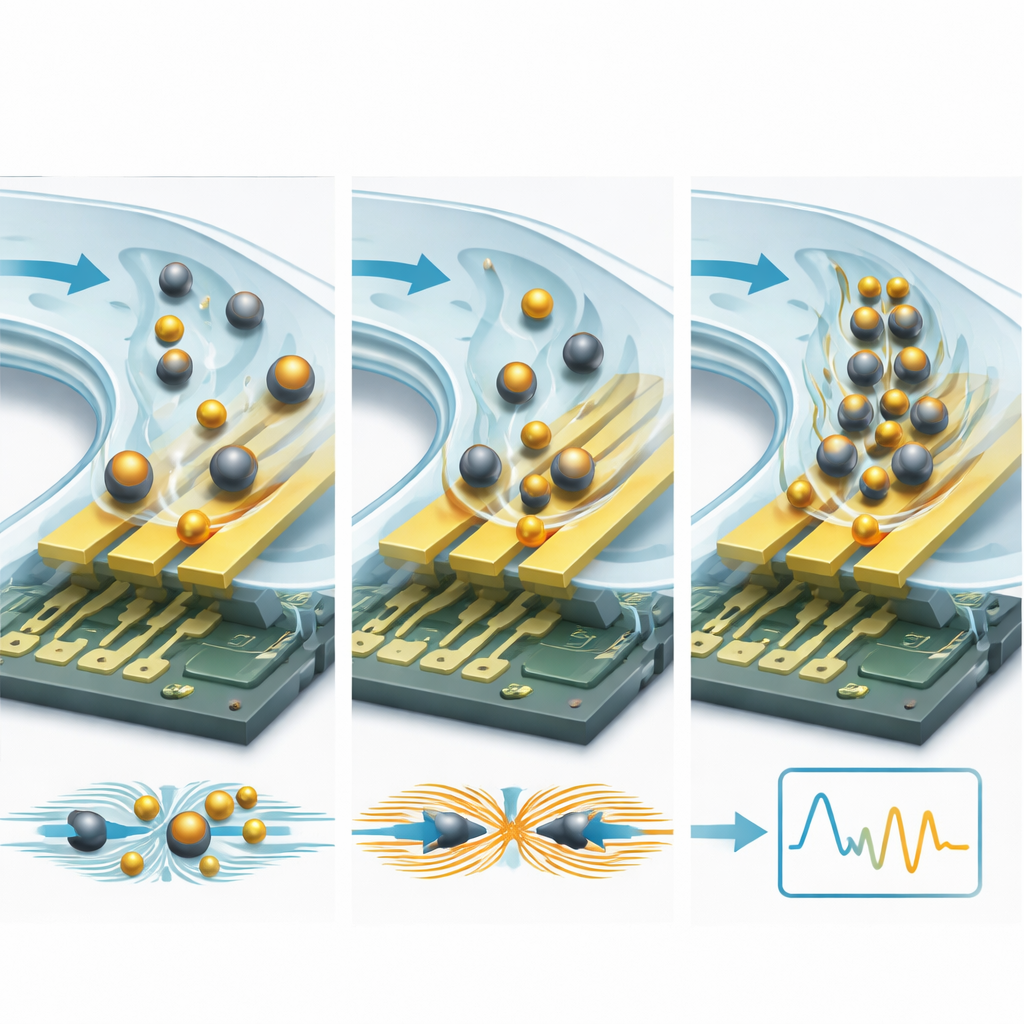
Цитирование: Kim, NS., Kim, J. Advancing non-faradaic impedance biosensors: sensitivity enhancement strategies using microfluidics, multiscale labeling, and CMOS technology. Microsyst Nanoeng 12, 117 (2026). https://doi.org/10.1038/s41378-026-01211-6
Ключевые слова: импедансные биосенсоры, микрофлюидика, маркировка наночастицами, CMOS-биосенсинг, диагностика у постели больного